-
氰化钾K4Fe(CN)6俗名黄血盐,可溶于水,不溶于乙醇。以某电镀厂排放的含NaCN 度液为主要原料制备黄血盐的流程如下:

请回答下列问题:
(1)常温下,HCN 的电离常数Ka=62×10-10。
①实验室配制一定浓度的NaCN溶液时,将NaCN 溶解于一定浓度的NaOH 溶液中,加水稀释至指定浓度,其操作的目的是__________________________。
②浓度均为0.5mol/L的NaCN和HCN的混合溶液显___________(填“酸”“碱”或“中”)性,通过计算说明:_________________________。
(2)转化池中发生复分解反应生成K4Fe(CN)6,说明该反应能发生的理由:_________________。
(3)系列操作B 为_____________________。
(4)实验室中,K4Fe(CN)6可用于检验Fe3+,生成的难溶盐KFe[Fe(CN)6]可用于治疗Tl2SO4中毒,试写出上述治疗Tl2SO4中毒的离子方程式:______________________。
(5)一种太阳能电池的工作原理如图所示,电解质为铁氰化钾K3Fe(CN)6和亚铁氰化钾K4Fe(CN)6的混合溶液。

①K+移 向 催 化 剂___________(填“a”或“b”)。
②催化剂a 表面发生的反应为_____________________。
-
亚铁氰化钾K4Fe(CN)6俗名黄血盐,可溶于水,不溶于乙醇。以某电镀厂排放的含NaCN废液为主要原料制备黄血盐的流程如下:
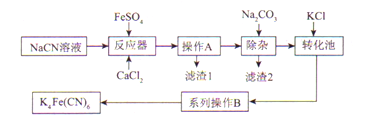
请回答下列问题:
(1)常温下,HCN的电离常数Ka=6.2×10-10。
①实验室配制一定浓度的NaCN溶液时,将NaCN溶解于一定浓度的NaOH溶液中,加水稀释至指定浓度,其操作的目的是_____________。
②浓度均为0.5 mol/L的NaCN和HCN的混合溶液显_________(填“酸”“碱”或“中”)性,通过计算说明:___________________________________。
(2)滤渣1的主要成分是______________(填化学式)。
(3)转化池中发生复分解反应生成K4Fe(CN)6,说明该反应能发生的理由:_____________。
(4)系列操作B为_________________。
(5)实验室中,K4Fe(CN)6可用于检验Fe3+,生成的难溶盐KFe[Fe(CN)6]可用于治疗Tl2SO4中毒,试写出上述治疗Tl2SO4中毒的离子方程式:_______________。
(6)一种太阳能电池的工作原理如图所示,电解质为铁氰化钾K3Fe(CN)6和亚铁氰化钾K4Fe(CN)6的混合溶液。
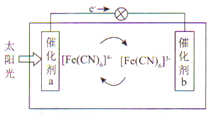
①K+移向催化剂____________(填“a”或“b”)。
②催化剂a表面发生的反应为____________________。
-
亚铁氰化钾K4Fe(CN)6俗名黄血盐,可溶于水,不溶于乙醇。以某电镀厂排放的含NaCN度液为主要原料制备黄血盐的流程如下:
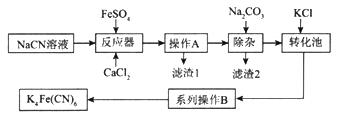
请回答下列问题:
(1)常温下,HCN的电离常数Ka=6.2×10-10。
①实验室配制一定浓度的NaCN溶液时,将NaCN溶解于一定浓度的NaOH溶液中,加水稀释至指定浓度,其操作的目的是__________________________。
②浓度均为0.5mol/L的NaCN和HCN的混合溶液显______(填“酸”“碱”或“中”)性,通过计算说明:_________________________。
(2)转化池中发生复分解反应生成K4Fe(CN)6,说明该反应能发生的理由:__________。
(3)系列操作B为_____________________。
(4)实验室中,K4Fe(CN)6可用于检验Fe3+,生成的难溶盐KFe[Fe(CN)6]可用于治疗可溶性盐Tl2SO4中毒,得到K2SO4及另外一种复杂难溶物,试写出上述治疗Tl2SO4中毒的离子方程式:______________________。
(5)一种太阳能电池的工作原理如图所示,电解质为铁氰化钾K3Fe(CN)6和亚铁氰化钾K4Fe(CN)6的混合溶液。
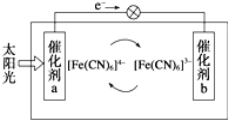
①K+移向催化剂___________(填“a”或“b”)。
②催化剂a表面发生的反应为_________________。
-
K4Fe(CN)6(亚铁氰化钾)可溶于水,不溶于乙醇,在电镀、食品添加剂等方面有广泛应用。以某电镀厂排放的含NaCN废液为主要原料制备K4Fe(CN)6的流程如下。已知:常温下,HCN的Ka=6.2×10-10,回答下列问题:
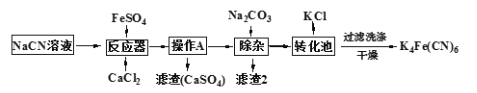
(1)HCN的电离方程式为______________;实验室配制一定浓度的NaCN溶液时,常将NaCN溶解于一定浓度的_______溶液中,加水稀释至指定浓度。
(2)反应器中发生的主要反应的化学方程式为______________。
(3)过滤后,洗涤K4Fe(CN)6使用的试剂为__________。
(4)实验室常用K4[Fe(CN)6]检验Fe3+,生成难溶盐KFe[Fe(CN)6],生成的盐又可用于治疗Ti2SO4中毒,试写出上述治疗Ti2SO4中毒反应的离子方程式为_____________。
(5)一种太阳能电池的工作原理如图,电解质为K3Fe(CN)6和K4Fe(CN)6的混合溶液。
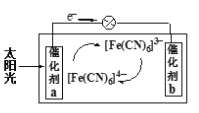
①则K+移向催化剂_________(填“a”或“b”);
②催化剂a表面发生的电极反应为____________。
-
亚铁氰化钾K4[Fe(CN)6],俗名黄血盐,可溶于水,不溶于乙醇。在化学实验、电镀、食品添加剂、烧制青花瓷时可用于绘画等方面有广泛用途。已知HCN是一种极弱的酸,现有一种用含NaCN的废水合成黄血盐的主要工艺流程如下:
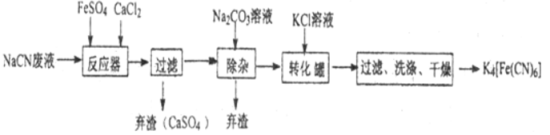
(1)常温下,NaCN水溶液的pH 7(填“>”、“<”、“ = ”),实验室用NaCN固体配制NaCN溶液时,应先将其溶于 溶液,再用蒸馏水稀释。
(2)反应器中发生的主要反应的化学方程式为 。
(3)流程中加入Na2CO3溶液后过滤除去弃渣,过滤需要的玻璃仪器有烧杯、漏斗、 。
(4)转化器中生成K4[Fe(CN)6]的反应类型是 ,相同温度下,溶解度:K4[Fe(CN)6] Na4[Fe(CN)6](填“>”“ = ”“<”),过滤后洗涤K4[Fe(CN)6]使用的试剂是 。
(5)实验室常用K4[Fe(CN)6]检验Fe3+,生成难溶盐KFe[Fe(CN)6],试写出上述反应的离子方程式为 。
(6)含有14.7kgNaCN的工业废水可生产出9.2kg的K4[Fe(CN)6],则K4[Fe(CN)6]的产率是 。
-
亚铁氰化钾K4[Fe(CN)6],俗名黄血盐,可溶于水,不溶于乙醇。在化学实验、电镀、食品添加剂、烧制青花瓷时可用于绘画等方面有广泛用途。已知HCN是一种极弱的酸,现有一种用含NaCN的废水合成黄血盐的主要工艺流程如下:
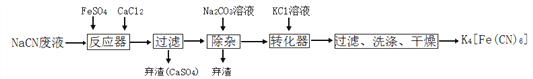
(1)常温下,NaCN水溶液的pH _______ 7(填“>”、“=”、“<”),实验室用NaCN固体配制NaCN溶液时,应先将其溶于_______溶液,再用蒸馏水稀释。
(2)反应器中发生的主要反应的化学方程式为 _____________________________。
(3)流程中加入Na2CO3溶液后过滤除去弃渣,过滤需要的玻璃仪器有烧杯、漏斗、______。
(4)转化器中生成K4[Fe(CN)6]的反应类型是________________,相同温度下,溶解度:K4[Fe(CN)6] _______ Na4[Fe(CN)6](填“>”、“=”、“<”) ,过滤后洗涤K4[Fe(CN)6]使用的试剂是________________。
(5)实验室常用K4[Fe(CN)6]检验Fe3+,生成难溶盐KFe[Fe(CN)6],试写出上述反应的离子方程式为 _________________________。
(6)含有14.7kg NaCN的工业废水可生产出9.2kg的K4[Fe(CN)6],则K4[Fe(CN)6]的产率是_______。
-
亚铁氰化钾的化学式为K4Fe(CN)6,一种用含NaCN废水合成该化合物的主要工艺流程如下:
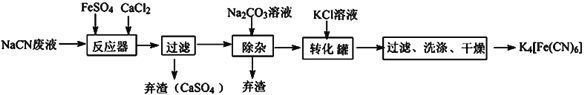
(1)请依据工艺流程图中的信息,回答下列问题:
①在“除杂”步骤中弃渣的主要成分为__________________(填化学式)。
②在“反应器“中发生的主要反应的化学方程式为:________________________________;
③相同温度下溶解度:Na4[Fe(CN)6]________K4[Fe(CN)6] (选填“>”、“<”或“=”)
(2)氰化钠(NaCN)是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。NaCN 的电子式为__________________________;实验室用NaCN固体配制NaCN溶液时,应先将其溶于氢氧化钠溶液中,再用蒸馏水稀释。NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是______________________________________。
(3)已知:氢氰酸是一种有苦杏仁气味的无色剧毒液体,易挥发,25℃时,Ka(HCN)=6.25×10-10。
①处理含CN-废水的方法是:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN-;第二步控制pH为7.5-8.5,用NaClO完全氧化OCN-生成N2和两种盐。
请写出第二步反应的离子方程式:_________________________________________。
②反应CN-+H2O HCN+OH-在25℃时的平衡常数K=_____________(填数值)。
HCN+OH-在25℃时的平衡常数K=_____________(填数值)。
(4)K4Fe(CN)6与高锰酸钾溶液反应,其方程式为:
K4Fe(CN)6+KMnO4 +H2SO4=KHSO4+Fe2(SO4)3+MnSO4+HNO3+CO2↑+H2O(未配平), 若有1mol K4Fe(CN)6被高锰酸钾氧化时,则消耗KMnO4的物质的量为________mol。
-
氰化钠(NaCN)是一种重要化工原料,用于化学合成、电镀、冶金等方面。NaCN有剧毒,含氰废水需经无害化处理才能排放,某电镀厂含氰废水的一种工业处理流程如下:
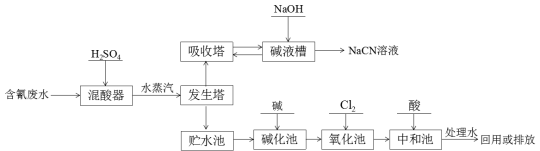
已知:HCNO的结构式是:H-O-C≡N
HCN的Ka = 6.02×10-10
[Ag(CN)2]-(aq)  Ag+(aq) + 2CN-(aq) K = 1.3×10-21
Ag+(aq) + 2CN-(aq) K = 1.3×10-21
回答下列问题:
(1)CN-中两原子均为8电子稳定结构,请写出CN-的电子式_____________________。
(2)氰化钠遇水会产生剧毒氢氰酸,请写出相应的离子方程式 。
(3)向发生塔中通水蒸汽的目的是 。
(4)氧化池中氰化物的降解分两步进行
CN-被氯气氧化成低毒的CNO- ,写出相应的离子方程式 ,
CNO-被氯气氧化成无毒的两种气体,写出相应的离子方程式
(5)贮水池中废水须先经碱化后再进行氧化的原因___________________________。
(6)电镀厂电镀银时需要降低镀层金属的沉积速度,使镀层更加致密。电解液使用Na[Ag(CN)2],请写出阴极反应式 ,解释工业电镀中使用氰离子(CN-)的原因 。
-
氰化钠(NaCN)是一种重要化工原料,用于化学合成、电镀、冶金等方面。NaCN有剧毒,含氰废水需经无害化处理才能排放,某电镀厂含氰废水的一种工业处理流程如下: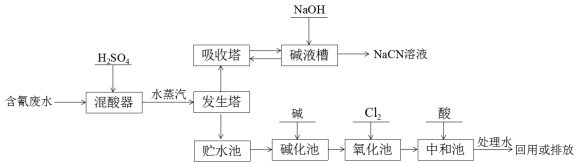
已知:HCNO的结构式是:H-O-C≡N
HCN的Ka= 6.02×10-10
[Ag(CN)2]-(aq) Ag+(aq) + 2CN-(aq) K = 1.3×10-21
Ag+(aq) + 2CN-(aq) K = 1.3×10-21
回答下列问题:
(1)CN-中两原子均为8电子稳定结构,请写出CN-的电子式_______________。
(2)氰化钠遇水会产生剧毒氢氰酸,请写出相应的离子方程式_______________。
(3)向发生塔中通水蒸汽的目的是____________。
(4)氧化池中氰化物的降解分两步进行
CN-被氯气氧化成低毒的CNO- ,写出相应的离子方程式____________________,
CNO-被氯气氧化成无毒的两种气体,写出相应的离子方程式________________。
(5)贮水池中废水须先经碱化后再进行氧化的原因_______________________。
(6)电镀厂电镀银时需要降低镀层金属的沉积速度,使镀层更加致密。电解液使用Na[Ag(CN)2],请写出阴极反应式 ,解释工业电镀中使用氰离子(CN-)的原因 。
-
(14分)亚铁氰化钾(K4Fe(CN)6 ,黄血盐)在实验室、电镀、食品添加剂及医学上可用于冶疗铊(Tl)中毒、烧制青花瓷时可用于绘画等有广泛用途。已知HCN是一种极弱的酸。现有一种用含NaCN废水合成黄血盐的主要工艺流程如下:
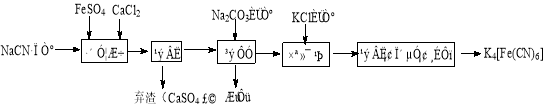
(1)实验室用NaCN固体配制NaCN溶液时,为避免其水解,应先将其溶于 溶液,再用蒸馏水稀释,NaCN水解的离子方程式为_________。
(2)实验室K4Fe(CN)6可用于检验Fe3+,生成的难溶盐KFe[Fe(CN)6],生成的盐又可用于治疗Tl2SO4中毒,试写出上述检验Fe3+反应的离子方程式为 。
(3)流程图中加入碳酸钠溶液主要目的是 。
(4)相同温度下溶解度:Na4[Fe(CN)6] K4[Fe(CN)6](选填:“>”、“=”、“<”)。
(5)长期火炒添加有亚铁氰化钾的食盐,这时会发生分解反应,试配平下列方程式:3K4Fe(CN)6=□KCN+□Fe3C+□C+□(CN)2↑+□N2↑
(6)电镀银时,电镀液不能直接用硝酸银溶液,可将其转变为K4[Ag2 (CN)6],写出AgCl与黄血盐制取电镀液的离子方程式 。













