-
某同学探究同周期元素性质的递变规律,并讨论影响化学反应速率的因素。设计的实验及部分现象如下:
【实验1】将一小块钠和镁片分别放入滴有酚酞溶液的冷水中
【实验2】将表面积大致相同的镁片和铝片(均已预处理),分别投入足量相同体积的0.5 mol/L盐酸中
【实验3】将相同质量的镁片(已预处理)和铝粉分别投入到足量相同体积的0.5 mol/L盐酸和3 mol/L盐酸中
(1)实验1中钠和水反应的化学方程式是_______________________________________。
(2)下列操作能达到实验2中“预处理”效果的是________________(填序号)。
a.用砂纸打磨镁片和铝片
b.用盐酸浸泡镁片和铝片片刻
c.用烧碱溶液浸泡镁片和铝片片刻
(3)由实验2可得出决定化学反应速率的主要因素是___________________________。
(4)实验3中铝粉消失所用的时间短。由此该同学得出结论:铝比镁的金属性强。你认为该结论是否正确并说明原因____________________________________________。
高一化学实验题简单题查看答案及解析
-
某同学探究同周期元素性质的递变规律,并讨论影响化学反应速率的因素.选用的试剂如下:镁条、铝条、铝粉、钠、新制Na2S溶液、新制氯水、0.5mol•L-1盐酸、3mol•L-1盐酸、酚酞试液;其设计的实验方案及部分实验现象如下表:
请回答下列问题:实验步骤 实验现象 ①将一小块金属钠投入滴有酚酞试液的冷水中 钠块浮在水面上,熔化成闪亮的小球,做不定向移动,随之消失,溶液变红色 ②将表面积大致相同的镁条和铝条(均已用砂纸打磨过)分别投入足量的相同体积0.5mo1•L-1盐酸中 镁条剧烈反应,迅速产生大量的无色气体,而铝条反应不十分剧烈,产生无色气体,镁条消失比铝条快 ③将新制氯水滴加到新制的Na2S溶液中 ④将相同质量的镁条(已用砂纸打磨过)和铝粉分别投入到足量的相同体积的0.5mol•L-1盐酸和3mol•L-1盐酸中 剧烈反应产生气体,但铝粉消失比镁条快
(1)实验①中可以说明该反应是放热反应的现象是________
(2)由实验②可得出决定化学反应快慢的主要因素是________
(3)实验③的现象是产生浅黄色沉淀,离子方程式为________
由实验③可以得出非金属性氯________硫(填“强于”、“弱于”、“无法比较”).
(4)实验④中,因为铝粉消失所用的时间短,因此,该同学得出结论:铝比镁易失电子,该结论是否正确?________(填“是”或“否”),通过实验④说明要加快化学反应速率可采取的措施可以是________或________.高一化学填空题中等难度题查看答案及解析
-
某同学探究同周期元素性质的递变规律,并讨论影响化学反应速率的因素,选用的试剂如下,镁条、铝条、铝粉、钠、新制的Na2S溶液,新制的氯水,0.5mol/L的盐酸,3mol/L的盐酸,酚酞试液,其设计的实验方案及部分实验现象如下表:
实验步骤
实验现象
①将一小块金属钠放入滴有酚酞试液的冷水中
钠块浮在水面上,熔化成闪亮的小球,做不定向移动,随之消失,溶液变红色
②将表面积大致相同的镁条和铝条(均已用砂纸打磨过,分别投入足量的相同体积的0.5mol/L的盐酸中
镁条剧烈反应,迅速产生大量的无色气体,而铝条反应不十分剧烈,产生无色气体,镁条消失比铝条快
③将新制的氯水滴加到新制的Na2S溶液中
④将相同质量的镁条(已用砂纸打磨过)和铝粉分别投入到足量的相同体积的0.5mol/L的盐酸和3mol/L的盐酸中
剧烈反应产生气体,但铝粉消失比镁条快
请回答下列问题:
(1)实验③的现象是 ,
该反应的离子方程式为 。
(2)由实验③得出的实验结论是 。
(3)由实验②可得出决定化学反应快慢的主要因素是 。
(4)实验④中,因为铝粉消失所用的时间短,因此,该同学得出结论:铝比镁易失电
子,该结论是否正确并说明原因 。
高一化学实验题中等难度题查看答案及解析
-
某同学探究同周期元素性质的递变规律,并讨论影响化学反应速率的因素,选用的试剂如下,镁条、铝条、铝粉、钠、新制的Na2S溶液,新制的氯水,0.5mol/L的盐酸,3mol/L的盐酸,酚酞试液,其设计的实验方案及部分实验现象如下表:
请回答下列问题:实验步骤 实验现象 ①将一小块金属钠放入滴有酚酞试液的冷水中 钠块浮在水面上,熔化成闪亮的小球,做不定向移动,随之消失,溶液变红色 ②将表面积大致相同的镁条和铝条(均已用砂纸打磨过,分别投入足量的相同体积的0.5mol/L的盐酸中 镁条剧烈反应,迅速产生大量的无色气体,而铝条反应不十分剧烈,产生无色气体,镁条消失比铝条快 ③将新制的氯水滴加到新制的Na2S溶液中 ④将相同质量的镁条(已用砂纸打磨过)和铝粉分别投入到足量的相同体积的0.5mol/L的盐酸和3mol/L的盐酸中 剧烈反应产生气体,但铝粉消失比镁条快
(1)实验③的现象是______,该反应的离子方程式为______,
(2)由实验③得出的实验结论是______;
(3)由实验②可得出决定化学反应快慢的主要因素是______;
(4)实验④中,因为铝粉消失所用的时间短,因此,该同学得出结论:铝比镁易失电子,该结论是否正确?______ (填是或否)
(5)通过实验④说明要加快化学反应速率可______或______.高一化学解答题中等难度题查看答案及解析
-
某学习小组同学探究同周期元素性质的递变规律,并讨论影响化学反应速率的因素,选用的试剂如下:镁条、铝条、铝粉、钠、新制的Na2S溶液,新制的氯水,0.5mol/L的盐酸,3mol/L的盐酸,酚酞试液。其设计的实验方案及部分实验现象如下表:
实验步骤
实验现象
①将一小块金属钠放入滴有酚酞试液的冷水中
钠块浮在水面上,熔化成闪亮的小球,四处游动,随之消失,溶液变红色
②将表面积大致相同的镁条和铝条(均已用砂纸打磨过),分别投入足量的相同体积的0.5mol/L的盐酸中
镁条剧烈反应,迅速产生大量的无色气体,而铝条反应不十分剧烈,产生无色气体,镁条消失比铝条快
③将新制的氯水滴加到新制的Na2S溶液中
④将相同质量的镁条(已用砂纸打磨过)和铝粉分别投入到足量的相同体积的0.5mol/L的盐酸和3mol/L的盐酸中
均剧烈反应产生气体,但铝粉消失比镁条快
请回答下列问题:
(1)实验①中可以说明该反应是放热反应的现象是_____。
(2)实验③的现象是______,该反应的离子方程式为______。
(3)由实验②③得出的结论是______。
(4)由实验②可得出决定化学反应快慢的主要因素是______。
(5)通过实验④说明要加快化学反应速率可______。
高一化学综合题中等难度题查看答案及解析
-
(9分)某同学探究同周期元素性质的递变规律,并讨论影响化学反应速率的因素,选用的试剂如下:镁条、铝条、铝粉、钠、新制的Na2S溶液、新制的氯水、0.5mol/L的盐酸、3mol/L的盐酸、酚酞试液,其设计的实验方案及部分实验现象如下表:
实验步骤
实验现象
①将一小块金属钠放入滴有酚酞试液的冷水中
钠块浮在水面上,熔化成闪亮的小球,做不定向移动,随之消失,溶液变红色
②将表面积大致相同的镁条和铝条(均已用砂纸打磨过,分别投入足量的相同体积的0.5mol/L的盐酸中
镁条剧烈反应,迅速产生大量的无色气体,而铝条反应不十分剧烈,产生无色气体,镁条消失比铝条快
③将新制的氯水滴加到新制的Na2S溶液中
④将相同质量的镁条(已用砂纸打磨过)和铝粉分别投入到足量的相同体积的0.5mol/L的盐酸和3mol/L的盐酸中
剧烈反应产生气体,但铝粉消失比镁条快
请回答下列问题:
(1)实验③的现象是,该反应的离子方程式为________,
(2)由实验③得出的实验结论是________
(3)由实验②可得出决定化学反应快慢的主要因素是________
(4)实验④中,因为铝粉消失所用的时间短,因此,该同学得出结论:铝比镁易失电子,该结论是否正确?________ (填是或否)
(5)通过实验④说明要加快化学反应速率可________或________。
高一化学实验题简单题查看答案及解析
-
甲同学拟通过实验探究同主族元素性质的递变规律,以及影响化学反应速率的因素。其设计的实验方案如下,请你帮他填写完整,并做出评价。
实验室提供的试剂:锌块、锌粉、铁条、铁粉、铜条、NaBr溶液、NaI溶液、新制的氯水、1mol/盐酸、3mol/L的盐酸
(1)探究同主族元素性质的递变规律
实验步骤
实验现象
实验结论及离子反应方程式
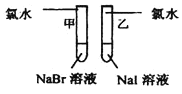
甲:___
乙:___
离子反应方程式
甲:___
乙:___
结论:卤素单质的氧化性由强到弱的顺序为Cl2>Br2>I2
评价:甲同学设计的实验方案的合理性是___(填序号)
A.非常合理 B.完全不合理 C.部分合理
补充和完善:上一项若填A,则此项不用再作答,若填B或C,则完成实验还需要的试剂后,有关反应的离子反应方程式为:___。
(2)探究影响化学反应速率的因素
实验步骤
实验现象
实验依据和结论
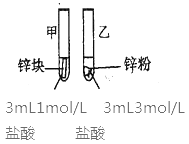
(金属质量相同,盐酸均过量)
均有气体生成,锌粉先消失,锌块后消失
因为乙试管中的反应更快,所以反应物浓度越大,反应速率越快。
甲同学所得实验依据和结论有明显问题,问题是___。
(3)请你利用原电池原理,设计实验,比较铜和铁的金属活动性。画出实验装置图,标出正负极、电子流动方向___,写出电极反应式。电极反应式:____、____。
装置图
高一化学实验题简单题查看答案及解析
-
(12分)甲同学拟通过实验探究同主族元素性质的递变规律,以及影响化学反应速率的因素。其设计的实验方案如下,请你帮他填写完整,并做出评价。
实验室提供的试剂:锌块、锌粉、铁条、铁粉、铜条、NaBr溶液、NaI溶液、新制的氯水、1mol/L盐酸、3mol/L的盐酸
(1)探究同主族元素性质的递变规律
①写出下列实验报告中的实验现象和离子方程式

②【评价】甲同学设计的实验方案的合理性是___________(填序号)
A. 非常合理 B. 部分合理 C. 完全不合理
③【补充和完善】上一题②中若选A,则此项不用再作答,若选B或C,则完成实验还需要的试剂是___________。
(2)探究影响化学反应速率的因素
实验步骤
实验现象
实验依据和结论

3mL1mol/L 3mL3mol/L
盐酸 盐酸
(金属质量相同,盐酸均过量)
均有气体生成,锌粉先消失,锌块后消失
因为乙试管中的反应更快,所以反应物浓度越大,反应速率越快。
甲同学所得实验依据和结论有明显问题,问题是 。
(3)请你利用原电池原理,设计实验,比较铜和铁的金属活动性。画出实验装置图,标出正负极、电子流动方向,写出电极反应式。
高一化学填空题中等难度题查看答案及解析
-
(14分)某同学探究同周期元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验步骤”与“实验现象”前后不一定是对应关系)。
实验步骤
实验现象
①将一小块金属钠放入滴有酚酞的冷水中
A.剧烈反应,产生大量无色气体。
②将镁条用砂纸打磨后,放入沸水中,再向溶液中滴加酚酞溶液
B.浮在水面,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。
③将镁条放入稀盐酸中
C.生成淡黄色沉淀。
④将铝条放入稀盐酸中
D.反应较快,产生无色气体。
⑤向AlCl3 溶液中 滴加NaOH 溶液至过量
E.有气体产生,溶液变成浅红色。
⑥向新制的Na2S溶液中滴加新制的氯水
F.产生白色胶状沉淀,继而沉淀消失。
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究同周期元素性质递变规律。
(2)实验药品:金属钠、镁条、铝条、稀盐酸、新制氯水、新制Na2S溶液、AlCl3 溶液、NaOH 溶液等。
实验仪器:试管、试管夹、酒精灯、胶头滴管、镊子、小刀、玻璃片、砂纸等。
(3)实验内容(填写与实验步骤对应的实验现象的标号和化学方程式)
实验内容
实验现象
化学方程式
①
B
②
Mg + 2H2O
Mg(OH)2 + 2H2 ↑
③
Mg + 2HCl = MgCl2 + H2↑
④
D
⑤
AlCl3 + 3NaOH = Al(OH)3↓+ 3NaCl
Al(OH)3 + NaOH = NaAlO2 + 2H2O
⑥
Na2S + Cl2 = 2NaCl + S↓
(4)实验结论: 。
高一化学实验题简单题查看答案及解析
-
下面是某化学兴趣小组的同学学习元素周期律时设计的两套实验方案。
(实验一)实验步骤如下:
向新制的Na2S溶液中滴加新制的氯水
设计该实验方案的目的是:探究同周期元素的性质递变规律。
(1)实验①的现象是_____________________,反应的离子方程式是_________________。
(实验二)为验证Cl、Br的非金属性强弱,设计了如下实验:(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)实验步骤如图.
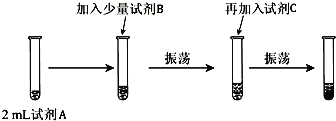
(2)试剂A是NaBr溶液,试剂B是氯水,加C后出现分层,则试剂C是____________.
(3)加入C振荡、静置后看到的现象是:______________________________________。以上反应可以证明Cl的非金属性__________(填“强于”或“弱于”)Br的非金属性。
高一化学实验题中等难度题查看答案及解析