-
(1)某温度(t℃)时,测得0.01 mol·L-1 的NaOH溶液的pH=13,请回答下列问题:
①该温度下水的Kw= 。
②此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合(忽略体积变化),若所得混合液为中性,且a=12,b=2,则Va︰Vb= 。
(2)已知25°C时Ksp(Mg(OH)2)=1.8×10-11,为除去某食盐溶液中的Mg2+,可用NaOH为除杂试剂,当控制溶液PH=12时,可确保Mg2+除尽,此时溶液中Mg2+的物质的量浓度为________.________
高二化学选择题简单题查看答案及解析
-
回答下列问题:
(1)某温度时,测得0.01mol/L的NaOH溶液pH=13,该温度下水的Kw=__。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-25.0kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-48.0kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:__。
(3)已知25℃时Ksp(Mg(OH)2)=1.8×10-11,为除去某食盐溶液中的Mg2+,可用NaOH为除杂试剂,当控制溶液pH=12时,可确保Mg2+除尽,此时溶液中Mg2+的物质的量浓度为__mol/L。
(4)生活中明矾常作净水剂,其净水的原理是__(用离子方程式表示)。
(5)常温下,取0.2mol/LHCl溶液与0.2mol/LMOH溶液等体积混合,测得混合溶液后的pH=5,写出MOH的电离方程式:__。
(6)0.1mol/L的NaHA溶液中,已知有关粒子浓度由大到小的顺序为:c(Na+)>c(HA-)>c(H2A)>c(A2-)
①该溶液中c(H+)__c(OH-)(填“>”、“<”或“=”)
②作出上述判断的依据是__(用文字解释)。
高二化学综合题中等难度题查看答案及解析
-
(1)某温度(t℃)时,测得0.01 mol·L-1 的NaOH溶液的pH=13,请回答下列问题:
①该温度下水的Kw=________
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)== 2Fe(s)+3CO2(g) △H=―24.8kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H=―47.2kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H=+640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:_________________________
(3)已知25°C时Ksp(Mg(OH)2)=1.8×10-11,为除去某食盐溶液中的Mg2+,可用NaOH为除杂试剂,当控制溶液pH=12时,可确保Mg2+ 除尽,此时溶液中Mg2+的物质的量浓度为
________mol·L-1
高二化学填空题简单题查看答案及解析
-
列式并计算下列各小题:
(1)某温度时,测得0.01 mol/L的NaOH溶液pH为11,求该温度下水的离子积常数Kw
(2)在此温度下,将pH=a的NaOH溶液Va L与pH=b的硫酸Vb L混合。
①若所得混合溶液为中性,且a=12,b=2,求Va ∶Vb 。
②若所得混合溶液的pH=10,且a=12,b=2,求Va∶Vb 。
高二化学计算题中等难度题查看答案及解析
-
某温度(T℃)时,测得0.01mol·L-1的NaOH溶液的pH为11,该温度下水的KW= 。该温度(填“大于”、“小于”或“等于”) 25℃,其理由是 。
此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合,通过计算填写以下不同情况时两溶液的体积比:
(1)若所得混合溶液为中性,且a=12,b=2,则Va:Vb= 。
(2)若所得混合溶液为中性,且a+b=12,则Va:Vb= 。
(3)若所得混合溶液的pH=10,且a=12,b=2,Va:Vb= 。
高二化学填空题中等难度题查看答案及解析
-
某温度(t°C)时,测得0.01mol•L-1的NaOH溶液的pH为11,则该温度下水的Kw=________.
高二化学填空题中等难度题查看答案及解析
-
(4分)某温度下的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L。x与y的关系如图所示:

(1)该温度下水的离子积为 。
(2) 该温度下0.01 mol/L NaOH溶液的pH为 。
高二化学填空题简单题查看答案及解析
-
(1)常温下,0.05mol/L硫酸溶液中, pH值为 ,水电离出的c(H+)= mol/L。
(2)某温度时,测得0.01 mol·L-1的NaOH溶液的pH为11,则该温度下水的离子积常数为________________。
在此温度下,将pH=a的H2SO4溶液VaL与pH=b的NaOH溶液VbL混合。
①若所得混合液为中性,且a=2,b=12,则Va:Vb=____________。
②若所得混合液的pH=10,且a=2,b=12,则Va:Vb=____________。
高二化学填空题中等难度题查看答案及解析
-
已知某温度下水的离子积KW=3.4×10-15.取该温度下浓度相同的NaOH和HCl溶液,以3∶2体积比相混合,所得溶液的pH等于12,则原溶液的浓度为
A.0.01mol·L-1 B.0.017mol·L-1
C.0.05mol·L-1 D.0.50mol·L-1
高二化学选择题中等难度题查看答案及解析
-
某温度下的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L。x与y的关系如图所示:
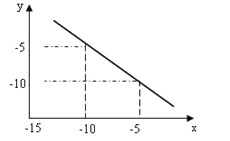
(1)该温度下水的离子积为______。
(2)该温度下0.01 mol/L NaOH溶液的pH为____。
(3)该温度下,将pH=12的NaOH溶液Va L与pH=2的H2SO4溶液Vb L混合,混合溶液呈中性,则Va﹕Vb=_______
高二化学填空题中等难度题查看答案及解析