-
下列关于实验的误差分析不正确的是
A.用已经潮解的烧碱配制标准NaOH溶液,测得盐酸含量偏高
B.用浓硫酸配制一定物质的量浓度稀硫酸时,用量筒量取浓溶液的体积时仰视读数,所得溶液的浓度偏低
C.用盐酸滴定含Na2O的NaOH样品,所得结果偏高
D.用移液管取盐酸待测液时没有润洗,测得盐酸含量偏低
高二化学选择题简单题查看答案及解析
-
下列有关实验误差分析中,正确的是( )
A. 用湿润的pH试纸测稀碱液的pH值,测定值偏小
B. 用容量瓶配制溶液,定容时仰视刻度线,所配溶液浓度偏大
C. 用盐酸标准溶液滴定未知浓度的NaOH溶液时,若滴定前滴定管内无气泡,终点读数时有气泡,则所测NaOH溶液的浓度偏大
D. 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏高
高二化学null中等难度题查看答案及解析
-
下列实验操作过程能引起实验结果偏高的是( )
①用已知浓度的盐酸滴定未知浓度的NaOH溶液时,酸式滴定管未用标准液润洗
②用量筒量取5.0 mL溶液时,俯视读数
③配制一定物质的量浓度的硫酸溶液,定容时仰视容量瓶的刻度线
④质量分数为10%和90%的两种硫酸等体积混合配制50%的硫酸溶液A. ①③ B. ①④ C. ②③ D. ②④
高二化学选择题中等难度题查看答案及解析
-
下列实验操作过程能引起结果偏高的是
①用已知浓度的盐酸滴定未知浓度的NaOH溶液时,酸式滴定管未用标准液润洗.
②用量筒量取5.0mL溶液时,俯视读数.
③配制一定物质的量浓度的硫酸溶液,定容时仰视容量瓶的刻度线.
④用已知浓度的盐酸滴定未知浓度的NaOH溶液时,滴定前平视读数,滴定终点仰视读数.
A.③④ B.②③ C.①④ D.①②
高二化学选择题中等难度题查看答案及解析
-
某学生用已知物质的量浓度的标准盐酸测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制500mL溶液。除烧杯、量筒、胶头滴管和玻璃棒外,还需要的玻璃仪器是___________。取用25.00mL待测液时需要的仪器是_____________。
(2)滴定过程中,在锥形瓶底垫一张白纸的作用是_______________;若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50mL,滴定后液面如图(上面数字:22,下面数字:23)。,则此时消耗标准溶液的体积为_________mL
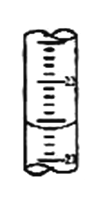
(3)下列操作中可能使所测NaOH溶液的浓度数值偏高的是________。
A.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净但没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
(4)用标准盐酸滴定上述待测NaOH溶液时,判定滴定终点的现象是:直到加入最后一滴盐酸,_____________________________为止。
(5)某学生根据3次实验分别记录有关数据如下表:
滴定次数
待测NaOH溶液的体积/mL
0.1000mol/L盐酸的体积/mL
滴定前刻度
滴定后刻度
溶液体积/mL
第一次
25.00
0.00
26.28
26.28
第二次
25.00
1.55
31.30
29.75
第三次
25.00
0.20
26.42
26.22
计算该NaOH溶液的物质的量浓度:c(NaOH)=__________mol/L。(保留四位有效数字)
高二化学实验题中等难度题查看答案及解析
-
某学生用已知物质的量浓度的标准盐酸测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制500mL溶液。除烧杯、量筒、胶头滴管和玻璃棒外,还需要的玻璃仪器是___________。取用25.00mL待测液时需要的仪器是_____________。
(2)滴定过程中,在锥形瓶底垫一张白纸的作用是_______________;若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50mL,滴定后液面如图(上面数字:22,下面数字:23)。,则此时消耗标准溶液的体积为_________mL
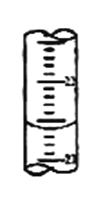
(3)下列操作中可能使所测NaOH溶液的浓度数值偏高的是________。
A.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净但没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
(4)用标准盐酸滴定上述待测NaOH溶液时,判定滴定终点的现象是:直到加入最后一滴盐酸,_____________________________为止。
(5)某学生根据3次实验分别记录有关数据如下表:
滴定次数
待测NaOH溶液的体积/mL
0.1000mol/L盐酸的体积/mL
滴定前刻度
滴定后刻度
溶液体积/mL
第一次
25.00
0.00
26.28
26.28
第二次
25.00
1.55
31.30
29.75
第三次
25.00
0.20
26.42
26.22
计算该NaOH溶液的物质的量浓度:c(NaOH)=__________mol/L。(保留四位有效数字)
高二化学实验题中等难度题查看答案及解析
-
下列有关实验操作,说法正确的是
A. 配制一定物质的量浓度溶液时,容量瓶中有少量的水会导致溶液浓度偏低
B. 用盐酸标准溶液滴定未知浓度氨水,选用酚酞做指示剂的结果比甲基橙更准确
C. 测定硫酸铜晶体中结晶水含量时,加热后的坩埚应直接放置在石棉网上冷却
D. 测定中和热时,应迅速将酸、碱稀溶液在有保温措施的容器内混合、搅拌,记录最高温度
高二化学单选题简单题查看答案及解析
-
某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
A.所用NaOH已经潮解
B.向容量瓶中加水未到刻度线
C.有少量NaOH溶液残留在烧杯里
D.用带游码的托盘天平称2.4gNaOH时误用了“左码右物”方法高二化学选择题中等难度题查看答案及解析
-
一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验。若要配制1 mol·L-1的稀硫酸标准溶液,用其滴定某未知浓度的NaOH溶液。下列有关说法错误的是( )
A. 实验中用到的滴定管和容量瓶仵使用前都需要检漏
B. 如果实验需用85 mL的稀硫酸标准溶液,配制时可选用100 mL容量瓶
C. 用甲基橙作指示剂,滴定终点时,溶液颜色从红色变为橙色
D. 酸式滴定管用蒸馏水洗涤后,即裝入标准浓度的稀硫酸滴定,会导致测定的NaOH溶液浓度偏大
高二化学选择题困难题查看答案及解析
-
下列实验过程能引起结果偏高的是
①配制100g l0%CuSO4溶液,称取l0g硫酸铜晶体溶于90g水中
②测定硫酸铜晶体中结晶水的百分含量时,所用的晶体已经受潮
③配制一定物质的量浓度的硫酸溶液时,定容时俯视容量瓶的刻度线
④质量分数为10%和90%的两种硫酸等质量混合配制50%的硫酸溶液
A.①④ B.②④ C.②③ D.②③④
高二化学选择题中等难度题查看答案及解析