-
(1)某兴趣小组在实验室探究工业合成硝酸的化学原理。
①氨的催化氧化:图a是探究氨的催化氧化的简易装置,实验中观察到锥形瓶中铂丝保持红热,有红棕色气体生成或白烟产生。白烟的成分是 (填化学式)。
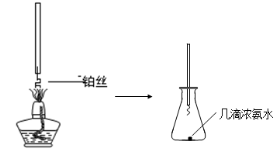
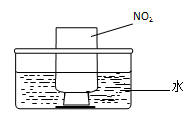
图a 图b
②NO2的吸收:如图b所示,将一瓶NO2倒置于水槽中,在水下移开玻璃片,可观察到的现象是 。
(2)三价铁盐溶液因Fe3+水解而显棕黄色,请以Fe(NO3)3溶液为例,设计实验探究影响盐类水解程度的因素。
①写出Fe(NO3)3水解的离子方程式 。
②参照示例完成下表实验方案的设计。
限选材料:0.05mol•L-1Fe(NO3)3、0.5mol•L-1Fe(NO3)3、1.0mol•L-1HNO3、1.0mol•L-1NaOH、NaHCO3固体、蒸馏水、冰水混合物;pH计及其他常见仪器。
| 可能影响因素 | 实验操作 | 预期现象和结论 |
| 溶液的酸碱性 | 取少量0.5mol•L-1Fe(NO3)3于试管中,加入几滴1mol•L-1HNO3。 | 棕黄色溶液颜色变浅,说明溶液酸性增强能抑制Fe(NO3)3的水解。 |
| 盐的浓度 | | |
| | |
-
硝酸是一种重要的化工原料,工业上通常采用氨氧化法制取。某校化学兴趣小组的同学以氯化铵和氢氧化钙为主要原料并设计了下列装置来制硝酸(三氧化二铬为催化剂,加热及夹持装置未画出):
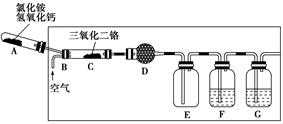
回答下列问题:
(1)实验时,A、C两装置均需加热,应先加热________装置,原因是
________________________________________________________________________。
(2)D装置中应填充的物质是________,该物质的主要作用是____________________。
(3)E装置的作用是__________________,F、G装置中的物质分别是________、________。
(4)若保留上图中黑色粗线框内的装置但去掉通空气的导管B,将C装置中的双孔橡皮塞换成单孔橡皮塞,请你用图示的方法设计一个最简单的实验方案同样完成硝酸的制取(在下面的方框中画出装置图并注明所用药品的名称)。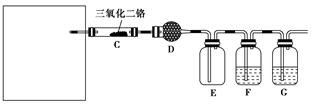
-
某化学兴趣小组的同学们对SO2的有关反应进行实验探究:
【实验I】探究SO2催化氧化的反应:

(1)装置 A模拟工业生产中SO2催化氧化的反应,其化学方程式是_________________________。〇
(2)为检验反应后的气体成分,将上图装置依次连接的合理顺序为A、(按气流方向,用字母表示)_______。
(3)能证明气体中有SO2的实验现象是_____________,有SO3的实验现象是_____________。
【实验II】探究SO2与Fe(NO3)3,溶液的反应:

(4)X中滴加浓硫酸之前应进行的操作是打开弹簧夹,通入一段时间N2,再关闭弹簧夹,目的是 ___________________________。
(5)装置Y中产生了白色沉淀,其成分是_________;该研究小组对产生白色沉淀的原因进行了假设:
假设1:在酸性条件下SO2与NO3-反应;
假设2:SO2与Fe3+反应;
假设3:___________________________。
(6)某同学设计实验验证假设1,请帮他完成下表中内容。
| 实验步骤 | 现象和结论 |
| ①测定Y中混合溶液的pH; ②配制与步骤①有相同pH的________,并通入适量N2; ③将SO2通入步骤②中溶液。 | 若出现白色沉淀则假设1成立,若不出现白色沉淀则假设1不成立。 |
经验证假设1成立,则验证过程中发生反应的离子方程式是_______________(提示:此条件下未见气体产生)。
-
(11分)某种催化剂为铁的氧化物。化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少许样品中,加热溶解;取少许溶液,滴加KSCN溶液后出现红色。一位同学由此得出该催化剂中铁元素价态为+3的结论。
(1)请指出该结论是否合理并说明理由________ ________。
(2)请完成对铁元素价态的探究:
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹:3 mol·L-1H2SO4、3% H2O2、6 mol·L-1HNO3、0.01 mol·L-1KMnO4、NaOH稀溶液、0.1 mol·L-1Kl、20% KSCN、蒸馏水。
提出合理假设
假设1: ________;
假设2: ;
假设3: ________。
设计实验方案证明你的假设(不要在答题卡上作答)
实验过程
根据②的实验方案,进行实验。请在答题卡上按下表格式写出实验操作步骤、预期现象与结论。
| 实验操作 | 预期现象与结论 |
| 步骤1: | |
| 步骤2: | |
| 步骤3: | |
| … | |
-
某种催化剂为铁的氧化物.化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少许样品中,加热溶解;取少许溶液,滴加KSCN溶液后出现红色.一位同学由此得出该催化剂中铁元素价态为+3的结论.
(1)请指出该结论是否合理并说明理由______
(2)请完成对铁元素价态的探究:
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹:3mol•L-1H2SO4/
3% H2O2、6mol•L-1HNO3/0.01mol•L-1KMnO4、NaOH稀溶液、0.1mol•L-1KI、20% KSCN、蒸馏水.
①提出合理假设
假设1:______;
假设2:______;
假设3:______.
②设计实验方案证明你的假设(不要在答题卡上作答)
③实验过程:根据②的实验方案,进行实验.请在答题卡上按下表格式写出实验操作步骤、预期现象与结论.
| 实验操作 | 预期现象与结论 |
| 步骤1: | |
| 步骤2: | |
| 步骤3: | |
| … | |
-
氨气是一种重要化合物,在工农业生产、生活中有着重要应用。
(1)“氨的催化氧化”是工业生产硝酸的重要步骤。某化学课外活动小组设计了如下装置模拟该实验过程,并用水吸收制取硝酸(固定装置略去):
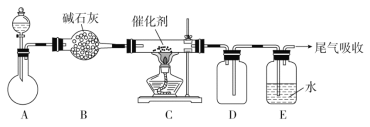
①检查装置气密性的方法是__________________________,D的作用是________。
A装置的分液漏斗中盛放浓氨水,则烧瓶中盛放的药品应该是________(填化学式)。
②反应后,装置E中除存在较多的H+外,还可能存在的一种阳离子是____________,试设计实验证明这种离子的存在:__________________________________________。
③下列哪个装置可以同时起到装置D和E的作用________(填代号)。
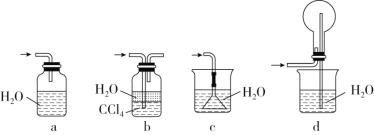
(2)若将氯气和氨气在集气瓶中混合,会出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出反应的化学方程式:________________________,该反应生成的还原产物的化学键类型是________。
-
某校学生活动小组设计如图所示装置探究工业制硫酸接触室的反应,并测定此条件下二氧化硫的转化率。实验时,装置D锥形瓶中溶液产生白色沉淀,装置E中溶液褪色。

试填空:
(1)装置B有三个作用:除了通过观察气泡控制氧气和二氧化硫的速率和比例外,还可以_______和_____。
(2)实验过程中,当V2O5表面红热后,应将酒精灯移开一会儿后再继续加热,其原因是___________。
(3)D中锥形瓶中盛放的溶液可以是(选填序号)____
a、澄清石灰水 b、小苏打溶液 c、氯化钡溶液 d、硝酸钡溶液
反应停止后,要根据装置D锥形瓶中产生的白色沉淀的量,测定已被氧化的二氧化硫的量时,在滤出沉淀前必须进行的一步操作是____________________。
(4)若从锥形瓶溶液中得到的沉淀质量为mg,要测定该条件下SO2的转化率,实验时还需要测定的数据是(选填序号)______。SO2的转化率是_______(用含有m、a、b、c、d中的一种或几种字母的代数式表示)。
①装置F增加的质量ag ②装置A中亚硫酸钠减少的质量bg
③装置B增加的质量cg ④装置E增加的质量dg
-
氨气是一种重要化合物,在工农业生产、生活中有着重要作用。
(1)“氨的催化氧化”是工业生产硝酸的重要步骤。某化学课外活动小组设计了如下装置模拟该实验过程,并用水吸收制取硝酸(固定装置略去):
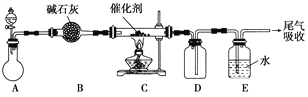
①A装置的分液漏斗中盛放浓氨水,则烧瓶中盛放的药品应该是________。
②C装置中发生反应的化学方程式为________________。
③反应后,装置E中除存在较多的H+外,还可能存在的一种离子是________,试设计实验证明这种离子的存在_____________________。
④下列哪些装置可以同时起到装置D和E的作用________(填代号)。
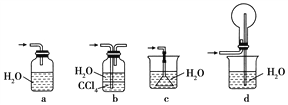
(2)若将氯气和氨气在集气瓶中混合,会出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出反应的化学方程式:________________(不必配平),该反应生成的还原产物的化学键类型是________。
-
 可用作食品添加剂。
可用作食品添加剂。 能发生以下反应:
能发生以下反应:

 淡黄色
淡黄色
某化学兴趣小组进行以下探究。回答有关问题:
 制取
制取
反应原理:

用如图所示装置进行实验。
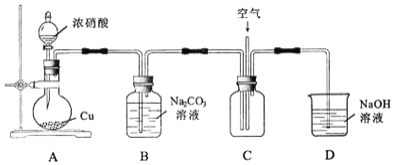
 铜与浓硝酸反应的离子方程式为______。
铜与浓硝酸反应的离子方程式为______。
 实验过程中,需控制B中溶液的
实验过程中,需控制B中溶液的 ,否则产率会下降,理由是______。
,否则产率会下降,理由是______。
 往C中通入空气的目的是______
往C中通入空气的目的是______ 用化学方程式表示
用化学方程式表示 。
。
 反应结束后,B中溶液经蒸发浓缩、冷却结品、______等操作,可得到粗产品晶体和母液。
反应结束后,B中溶液经蒸发浓缩、冷却结品、______等操作,可得到粗产品晶体和母液。
 测定粗产品中
测定粗产品中 的含量
的含量
称取mg粗产品,溶解后稀释至 取出
取出 溶液,用
溶液,用 酸性溶液平行滴定三次,平均消耗的体积为VmL。
酸性溶液平行滴定三次,平均消耗的体积为VmL。
已知:
 稀释溶液时,需使用的玻璃仪器除烧杯、玻璃棒外,还有______
稀释溶液时,需使用的玻璃仪器除烧杯、玻璃棒外,还有______ 填标号
填标号 。
。
A.容量瓶  量筒
量筒  胶头滴管
胶头滴管  锥形瓶
锥形瓶
 当观察到______时,滴定达到终点。
当观察到______时,滴定达到终点。
 粗产品中
粗产品中 的质量分数为______
的质量分数为______ 用代数式表示
用代数式表示 。
。
 设计实验方案证明母液中含有
设计实验方案证明母液中含有 ______
______ 限选用的试剂:硝酸、硝酸银溶液、硝酸钡溶液、氯化钡溶液
限选用的试剂:硝酸、硝酸银溶液、硝酸钡溶液、氯化钡溶液 。
。
-
某化学兴趣小组为了制取并探究氨气性质,按下列装置 部分夹持装置已略去
部分夹持装置已略去 进行实验。(制取氨气的反应原理:
进行实验。(制取氨气的反应原理: )
)

(实验探究)
(1)A装置N元素的化合价是_______该反应是否是氧化还原反应:_______。
(2)用 固体与足量
固体与足量 反应,最多可制得标准状况下氨气的体积为__________L。
反应,最多可制得标准状况下氨气的体积为__________L。 的摩尔质量为
的摩尔质量为
(3)气体通过C、D装置时,试纸颜色会发生变化的是D,原因是:___________________.
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入 滴浓盐酸,可观察到的现象是___________________.
滴浓盐酸,可观察到的现象是___________________.
(5)如果氨气泄漏,你应采取的急救措施是:___________________.
(6)检验氨气是否收集满的方法是__________________________________
(拓展应用)
(7)某同学用下图所示装置进行氨气的性质实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有_______性质 填序号
填序号 。
。

 还原性
还原性  极易溶于水
极易溶于水  与水反应生成碱性物质
与水反应生成碱性物质
(8)氨气的用途很广。如可用氨气处理二氧化氮: 该反应中氨气体现_______
该反应中氨气体现_______ 填“氧化性”或“还原性”
填“氧化性”或“还原性” 。
。
(9)请你列举出氨气的一种用途_________________________。













