-
实验室欲配制0.2 mol/L的Na2CO3溶液250 mL:
(1)配制溶液时必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、量筒、胶头滴管、___________。
(2)若用Na2CO3·10H2O晶体来配制该溶液,应称量晶体的的质量为__________g。
(3)容量瓶使用前必须进行的操作为_________________。
(4)在配制过程中,其他操作都是正确的,下列操作会引起所配浓度偏高的是___________。
①没有洗涤烧杯和玻璃棒
②容量瓶不干燥,含有少量蒸馏水
③定容时俯视刻度线
④定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
高一化学实验题简单题查看答案及解析
-
下图为配制250.0 mL 0.2 mol/L Na2CO3溶液过程的示意图。回答下列问题:
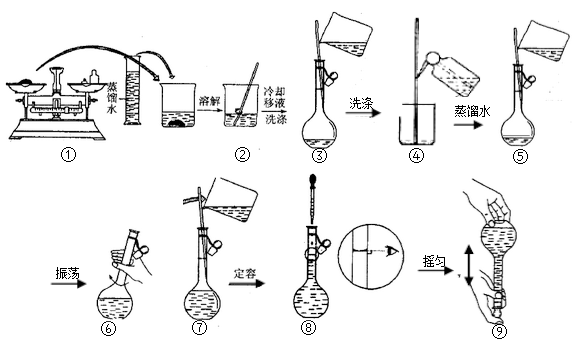
(1)实验时要用到的仪器有:烧杯、玻璃棒、托盘天平、药匙、量筒、 、 。
(2)在②③两步实验都用到玻璃棒,它的作用分别是 、加速溶解;引流、 。
(3)配制过程中,若其他操作都正确,下列操作会引起浓度偏大的是 :
A.容量瓶中原有少量的蒸馏水;
B.没有进行操作步骤④和⑤;
C.第⑧ 步观察液面时俯视刻度线;
D.如果加水超过了刻度线,取出少量水使液面恰好到刻度线
(4)由计算可知,在称量操作中,需用托盘天平称量Na2CO3固体的质量为 ,若用5mol·L-1 Na2CO3溶液配制该溶液,则应用量筒量取该溶液的体积为 。
高一化学实验题极难题查看答案及解析
-
用Na2CO3·10H2O晶体配制0.2mol·L-1Na2CO3溶液230mL。
(1)实验时要用到的玻璃仪器有:除托盘天平、量筒、烧杯、玻璃棒、胶头滴管外,至少还必须用到的一种玻璃仪器是__________,在使用该仪器前必须进行的操作是_______。
(2)应用托盘天平称取Na2CO3·10H2O晶体的质量为___________g。
(3)配制溶液时有多个操作,请简述定容的过程:________。
(4)配制过程中,下列操作会引起所配溶液的浓度偏大的有____(填序号)。
a.Na2CO3·10H2O晶体不纯,混有NaCl
b.用“左码右物”的称量方法称量晶体
c.容量瓶中洗净后未干燥,残留少量水
d.未冷却至室温就转移定容
e.加蒸馏水时不慎超过了刻度线,立即用胶头滴管将多余的水吸出
f.定容时,俯视刻度线
高一化学实验题简单题查看答案及解析
-
实验室欲配制90mL浓度为1.00mol·L-1的Na2CO3溶液:
(1)配制时的实验步骤为:计算、称量、溶解、转移(洗涤)、 ▲ 、摇匀;
(2)本实验中必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、量筒、胶头滴管、
________▲ (注明所需仪器的规格)。
(3)某同学欲称量Na2CO3的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。烧杯的实际质量为 ▲ g,要完成本实验该同学应称出 ▲ g Na2CO3。
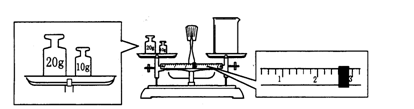
(4)使用容量瓶前必须进行的一步操作是▲ 。
(5)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)
①没有洗涤烧杯和玻璃棒________▲ ________;②容量瓶不干燥,含有少量蒸馏水________▲ ________;
高一化学实验题简单题查看答案及解析
-
实验室欲配制90mL浓度为1.00mol•L-1的Na2CO3溶液:
(1)配制时的实验步骤为:计算、称量、溶解、转移(洗涤)、______、摇匀;
(2)本实验中必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、量筒、胶头滴管、______(注明所需仪器的规格).
(3)某同学欲称量Na2CO3的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图.烧杯的实际质量为______g,要完成本实验该同学应称出______g Na2CO3.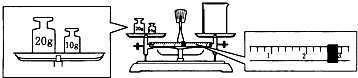
(4)使用容量瓶前必须进行的一步操作是______.
(5)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)
①没有洗涤烧杯和玻璃棒______;
②容量瓶不干燥,含有少量蒸馏水______.高一化学解答题中等难度题查看答案及解析
-
用Na2CO3·10H2O晶体配制0.20 mol/L Na2CO3溶液480 mL。
(1)实验时要用到的玻璃仪器有:除托盘天平、量筒、烧杯、玻璃棒、胶头滴管外,至少还必须用到的一种玻璃仪器是___________________,在使用该仪器前必须进行的操作是_______________________。
(2)应用托盘天平称取Na2CO3·10H2O晶体的质量为___________g。
(3)配制溶液时有以下几个操作:
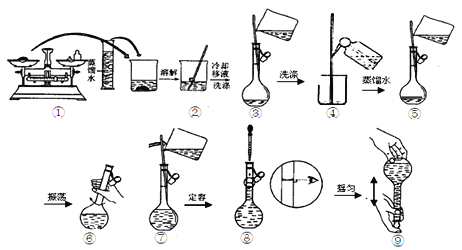
简述定容的过程:_______________________________。
(4)配制过程中,下列操作对所配溶液的浓度有什么影响,完成填空。
a.Na2CO3·10H2O晶体不纯,混有NaCl
b.用“左码右物”的称量方法称量晶体
c.容量瓶中洗净后未干燥,残留少量水
d.未冷却至室温就转移定容
e.加蒸馏水时不慎超过了刻度线,立即用胶头滴管将多余的水吸出
f.定容时,俯视刻度线
会引起所配溶液的浓度偏大的有________,无影响的有________。(填序号)
(5)如果直接使用浓度为2.00mol/L的Na2CO3溶液来配制100mL 1.00mol/L的Na2CO3溶液,需要量取2.00mol/L的Na2CO3溶液的体积为_________。
高一化学实验题中等难度题查看答案及解析
-
实验室欲配制90mL浓度为1.00mol•L﹣1的Na2CO3溶液:
(1)本实验中必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、量筒、胶
头滴管、__________(注明所需仪器的规格).
(2)使用容量瓶前必须进行的一步操作是__________.
(3)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)
①定容时俯视___________;
②容量瓶不干燥,含有少量蒸馏水__________.
高一化学填空题中等难度题查看答案及解析
-
用碳酸钠晶体(Na2CO3·10H2O)配制0.2 mol·L-1的Na2CO3溶液480 mL。
(1)本实验用到的仪器除托盘天平、烧杯、玻璃棒、胶头滴管外还需要______________,应称取Na2CO3·10H2O晶体的质量为________克。
(2)下列操作中,容量瓶所不具备的功能有________。
A.配制一定体积准确浓度的标准溶液 B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体 D.用来加热溶解固体溶质
(3)配制0.2 mol·L-1的Na2CO3溶液480 mL的主要步骤有:①溶解 ②计算 ③转移洗涤 ④定容摇匀 ⑤称量;正确的操作顺序是:_____________________。(填序号)
(4)根据下列操作对所配溶液浓度偏高的有(填序号)____________。
①碳酸钠晶体失去了部分结晶水 ②用“左码右物”的称量方法称量晶体
③碳酸钠晶体不纯,其中混有氯化钠 ④定容时俯视
⑤容量瓶未经干燥就使用 ⑥定容摇匀后,发现]液面低于刻度线,再加水到刻度线
高一化学实验题中等难度题查看答案及解析
-
(6分)实验室需配制500mL 0.2mol/L NaCl溶液
(1)本实验用到的仪器已有药匙、烧杯、量筒、托盘天平(砝码、镊子)、玻璃棒、胶头滴管,还缺少的玻璃仪器是 。
(2)配制时,需称取NaCl的质量是 g。
(3)在配制过程中,其他操作都正确的情况下,下列操作会导致所配制的溶液浓度偏高的是 。(选填序号)
①引流后没有洗涤烧杯和玻璃棒
②加蒸馏水时,不慎超过了刻度,取出少量水使液面恰好到刻度线
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视标线
⑤定容时仰视标线
高一化学填空题中等难度题查看答案及解析
-
实验室需要2.0 mol·L-1NaOH溶液90mL,请回答下列问题:
(1)配制该NaOH溶液时使用的仪器除托盘天平、烧杯、玻璃棒外,还必须用到的仪器有 、 等。
(2)用托盘天平称取氢氧化钠,其质量为 g;
(3)下列主要操作步骤的正确顺序是 (填序号);
①称取一定质量的氢氧化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶颈刻度线下1-2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③待冷却至室温后,将溶液转移到100mL容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量的蒸馏水洗涤烧杯内壁和玻璃棒2-3次,洗涤液转移到容量瓶中;
(4)在实验中其他操作均正确,如实验过程中缺少步骤⑤,会使配制出的NaOH溶液浓度 (填“偏高”或“偏低”或“不变”);若定容时仰视刻度线,则所得溶液浓度 2.0 mol·L-1(填“大于”或“小于”或“等于”)。
高一化学实验题简单题查看答案及解析