醇广泛存在于自然界中,是一类重要的有机化合物,请判断下列物质中不属于醇类的是
A. B.
C.CH3OH D.
高二化学选择题简单题
醇广泛存在于自然界中,是一类重要的有机化合物,请判断下列物质中不属于醇类的是
A. B.
C.CH3OH D.
高二化学选择题简单题
醇广泛存在于自然界中,是一类重要的有机化合物,请判断下列物质中不属于醇类的是
A. B.
C.CH3OH D.
高二化学选择题简单题查看答案及解析
卤素及其化合物广泛存在于自然界中。回答下列问题:
(1)光气(COCl2)是一种重要的有机中间体,在农药、医药、工程塑料、聚氨酯材料以及军事上都有许多用途。光气的分子立体构型为______________,其三种元素的电负性由小到大的顺序为______________。与COCl2互为等电子体的分子和离子(各写一种)__________。
(2)日常生活中,看到的许多可见光,如霓虹灯,试从原子结构角度解释这一现象?____________________________。
(3)区分晶态二氧化硅和非晶态二氧化硅最可靠的科学方法是_____________。
(4)一种铜的溴化物晶胞结构如图所示,若将图中的Cu去掉,再把所有的Br换成Cu,得到晶体铜的晶胞结构,则晶体铜的堆积方式为___________,某同学将基态铜原子价电子错误的写为3d94s2,违背了核外电子排布规律中的______。

(5)下列关于上述铜的溴化物晶胞结构说法正确的是_________(选填字母序号)。
A.该化合物的化学式为CuBr2
B.铜的配位数为8
C.与每个Br紧邻的Br有12个
D.由图中P点和Q点的原子坐标参数,确定R点的原子坐标参数为(1/4,1/4,1/4)
(6)若图中P点和R点的原子核间距为a cm,NA为阿伏伽德罗常数的值,则该晶胞密度为______g/cm3。(列出计算式即可)
高二化学综合题中等难度题查看答案及解析
过渡元素在现代社会得到广泛应用。请回答下列问题:
(1)铬能够生成美丽多色的化合物。自然界中铬以铬铁矿Fe(CrO2)2形式存在,将铬铁矿和碳酸钠混合后在空气中煅烧,将其转化为易溶于水的物质。请完成其化学方程式:4Fe(CrO2)2+8Na2CO3+7O2===________+2Fe2O3+8CO2。
(2)高锰酸钾因其强氧化性和溶液颜色变化明显而被用于物质的鉴定。请写出SO2与酸性高锰酸钾溶液反应的化学方程式:__________________________________。(高锰酸根离子的还原产物为Mn2+)
(3)向硫酸亚铁中滴加双氧水后变色,请写出其离子方程式:___________________。
(4)镍主要用于合金(可用来制造货币等)及用作催化剂(如氢化反应的催化剂),常见化合价为+2、+3。已知镍的氢氧化物均不溶于水。请写出碱性条件下Ni2+与溴水反应的离子方程式:_______________________________________________________________________。
高二化学综合题中等难度题查看答案及解析
醌类化合物广泛存在于植物中,有抑菌、杀菌作用,可由酚类物质制备:

下列说法不正确的是
A. 反应Ⅰ、Ⅱ均为氧化反应
B. 对苯醌、萘醌均属于芳香化合物
C. 苯酚与萘酚含有相同官能团,但不互为同系物
D.  属于酚类,
属于酚类, 属于醌类
属于醌类
高二化学单选题简单题查看答案及解析
香豆素是广泛存在于植物中的一类芳香化合物,大多具有光敏性,有的还具有抗菌和消炎作用。它的核心结构是芳香内酯A,其分子式为C9H6O2,该芳香内酯A经下列步骤转变为水杨酸和化合物E。
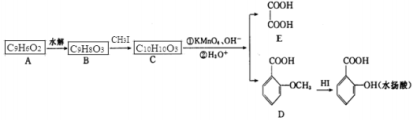
已知:
请回答下列问题:
(1)A中官能团的名称为________________;化合物C的结构简式为__________________;
(2)B生成C的反应类型为_______,化合物E的化学名称是________;
(3)写出A→B的化学方程式__________________;
(4)化合物D有多种同分异构体,其中一类同分异构体是苯的二元取代物,且水解后生成的产物之一能发生银镜反应.这类同分异构体共有_______种;写出其中核磁共振氢谱有5种峰,且其信号强度之比为1:1:2:2:2的同分异构体的结构简式_________________;
(5)已知:R-CH=CH2R-CH2-CH2Br,请设计合理方案由
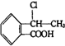 合成
合成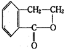 (其他无机原料自选,用反应流程图表示,并注明反应条件).示例:
(其他无机原料自选,用反应流程图表示,并注明反应条件).示例:。
高二化学推断题困难题查看答案及解析
香豆素是广泛存在于植物中的一类芳香化合物,大多具有光敏性,有的还具有抗菌和消炎作用。它的核心结构是芳香内酯A,其分子式为C9H6O2,该芳香内酯A经下列步骤转变为水杨酸和和化合物E。
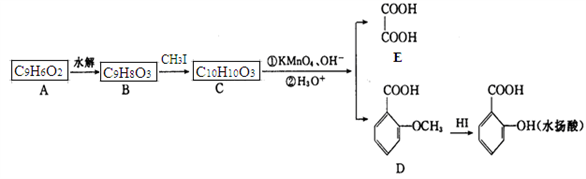
已知: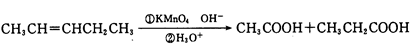
请回答下列问题:
(1)A中官能团的名称为_____________;化合物C的结构简式为______________。
(2)B生成C的反应类型为__________________,化合物E的化学名称是_________。
(3)写出A→B的化学方程式__________________________________________________。
(4)化合物D有多种同分异构体,其中一类同分异构体是苯的二元取代物,且水解后生成的产物之一能发生银镜反应。这类同分异构体共有________种;写出其中核磁共振氢谱有5种峰,且其信号强度之比为1 :1 :2 :2 :2的任一种同分异构体的结构简式___________。
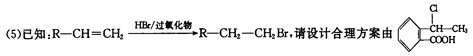 合成
合成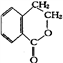
(其他无机原料自选,用反应流程图表示,并注明反应条件)。_________
示例:原料……产物
高二化学简答题困难题查看答案及解析
氮、磷属于同一主族元素,是组成生命体的重要元素,其单质及化合物用途广泛。回答下列问题:
(1)基态P原子的核外电子排布式为___________________
(2)自然固氮现象发生的一系列化学变化:,解释了民谚“雷雨发庄稼”的原理。
①分子结构中σ键和π键数目之比为__________
②中N原子采取__________杂化方式,写出它的一种等电子体的化学式:__________。
③已知酸性:,下列相关见解合理的是__________。
A.含氧酸中氧原子总数越多,酸性越强
B.同种元素化合价越高,对应含氧酸的酸性越强
C.中氮元素的正电性更高,在水溶液中更易电离出
,酸性强于
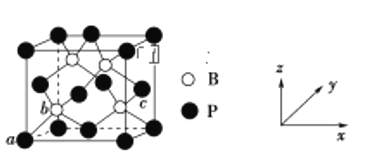
(3)磷化硼(BP)是一种超硬耐磨涂层材料,其晶胞结构如图所示,图中a点和b点的原子坐标参数分别为(0,0,0)、,则c点的原子坐标参数为__________。已知该晶体密度为
,则B—P键的键长为__________pm(阿伏加德罗常数用
表示,列出计算式即可)。
 。
。
高二化学推断题困难题查看答案及解析
香豆素是广泛存在于植物中的一类芳香化合物,大多具有光敏性,有的还具有抗菌和消炎作用。它的核心结构是芳香内酯A,其分子式为C9H6O2,该芳香内酯A经下列步骤转变为水杨酸和和化合物E。
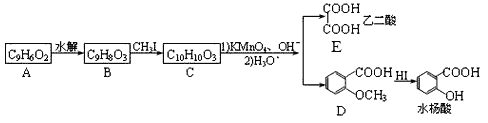
已知:CH3CH = CHCH2CH3CH3COOH + CH3CH2COOH
请回答下列问题:
(1)C中官能团的名称为________;化合物A的结构简式为________。
(2)C生成D和E的反应类型为________,化合物E的化学名称是________。
(3)写出B→C的化学反应方程式_________ 。
(4)化合物D有多种同分异构体,其中一类同分异构体是苯的二元取代物,且水解后生成的产物之一能发生银镜反应。这类同分异构体共有________种;写出其中核磁共振氢谱有4种峰,且其信号强度之比为1:2:2:3的一种同分异构体的结构简式________ 。
(5)已知: R- CH=CH2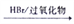 R-CH2CH2Br,请设计合理方案由
R-CH2CH2Br,请设计合理方案由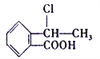 合成
合成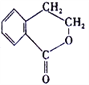 (其他无机原料自选,用反应流程图表示,并注明反应条件)。_______。示例:原料
(其他无机原料自选,用反应流程图表示,并注明反应条件)。_______。示例:原料……产物
高二化学综合题中等难度题查看答案及解析
有机化合物萜类化合物广泛存在于动植物体内,关于下列萜类化合物的说法正确的是
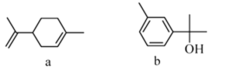
A.a和b均属于苯的同系物
B.a和b分子中所有碳原子均处于同一平面上
C.a和b均能使酸性KMnO4溶液褪色
D.1mol a物质与足量氢气加成,消耗的氢气为5mol
高二化学单选题中等难度题查看答案及解析
碳及其化合物广泛存在于自然界。随着科技的进步,利用化学反应原理将含碳物质进行合理转化,已成为资源利用、环境保护等社会关注问题的焦点。如CO2是人类工业生产排放的主要的温室气体,利用CO2制造更高价值化学品是目前的研究热点。
(1)①利用CH4和CO2这两种温室气体可以生产水煤气。已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H =890.3 kJ·mol-1
CO(g)+H2O (g)=CO2(g)+H2 (g) △H =+2.8 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H =566.0 kJ·mol-1
反应CO2(g)+CH4(g) 2CO(g)+2H2(g) 的△H =____kJ·mol-1
②250℃时,以镍合金为催化剂,向4 L恒容容器中通入6 mol CO2、6 mol CH4,发生如下反应:CO2 (g)+CH4(g) 2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
| 物质 | CH4 | CO2 | CO | H2 |
| 体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
此温度下该反应的平衡常数K=_______。
(2)利用CO2催化加氢可以合成乙醇,反应原理为:2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) ∆H<0,设m为起始时的投料比,即m= n(H2)/ n(CO2)。
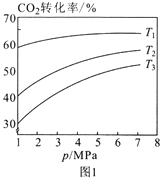
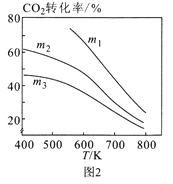
①图1中投料比相同,温度从高到低的顺序为____。
②图2中m1、m2、m3从大到小的顺序为____。
(3)高温电解技术能高效实现下列反应:CO2+H2O CO+H2+O2,其可将释放的CO2转化为具有工业利用价值的产品。工作原理示意图如下:
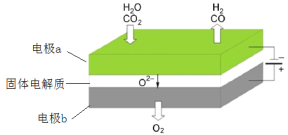
电极a的电极反应式____。
(4)工业生产烟气中的CO2捕获技术之一是氨水溶液吸收技术,将烟气冷却至15.5℃~26.5℃后用氨水吸收过量的CO2。已知:NH3·H2O的Kb=1.7×10-5,H2CO3的Ka1=4.3×10-7、Ka2=5.6×10-11。吸收后所得溶液的pH____7(填“>”、“=”或“<”)。
高二化学综合题简单题查看答案及解析