-
将30 mL 0.5 mol·L-1 NaOH溶液加水稀释到500 mL,关于稀释后的溶液叙述不正确的是( )
A. 浓度为0.03 mol·L-1 B. 从中取出10 mL溶液,其浓度为0.03 mol·L-1
C. 含NaOH 0.6 g D. 从中取出10 mL溶液,含NaOH 0.015 mol
高三化学单选题中等难度题查看答案及解析
-
将30 mL 0.5 mol·L―1的NaCl溶液加水稀释到500 mL,稀释后溶液中NaCl的物质的量浓度为
A.0.3 mol·L―1 B.0.03 mol·L―1 C.0.05 mol·L―1 D.0.04 mol·L―1
高三化学选择题简单题查看答案及解析
-
将20 mL 0.5 mol/L Al2(SO4)3溶液加水稀释到500 mL,稀释后溶液中SO42-浓度为
A.0.01 mol/L B.0.02 mol/L C.0.03mol/L D.0.06mol/L
高三化学选择题简单题查看答案及解析
-
(10分)(1)将100克质量分数为10%的NaOH溶液与50克质量分数为20%的NaOH溶液混合后,加水稀释至溶液体积为500ml,则稀释后NaOH的物质的量浓度为
(2)有BaCl2和NaCl的混合溶液a L,将它均分成两份。一份滴加稀硫酸,使Ba2+ 完全沉淀;另一份滴加AgNO3溶液,使Cl— 完全沉淀。反应中消耗x mol H2SO4、y mol AgNO3。据此得知原混合溶液中的c(Na+)为 mol·L-1
(3)某化合物质X,受热分解3X=A+2B+3C,产物均为气体,测得生成物混合气体对相同条件下氢气的相对密度为22 ,则X的相对原子质量为
(4)标准状况下,将15 LO2通入10LH2和CO的混合气中,充分燃烧干燥后,恢复至标准状况
①若剩余的气体体积为15 L,则原混合气中V(CO)=
②若剩余的气体体积为a L,则原混合气中V(CO) : V(H2)=
高三化学填空题中等难度题查看答案及解析
-
常温下向浓度均为0.10mol/L、体积均为1mL的NaOH溶液和Na2CO3溶液中分别加水,均稀释至VmL,两种溶液的pH与lgV的变化关系如图所示。下列叙述中错误的是
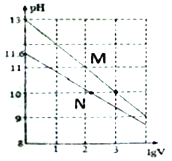
A. Ka1(CO32-)(Ka1为第一级水解平衡常数)的数量级为10-4
B. 曲线N表示Na2CO3溶液的pH随lgV 的变化关系
C. Na2CO3溶液中存在:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
D. 若将Na2CO3溶液加热蒸干,由于CO32-水解,最终析出的是NaOH固体
高三化学单选题中等难度题查看答案及解析
-
25℃时,在10mL浓度均为0.1mol/L的NaOH和CH3COONa混合溶液中滴加0.1mol/L的盐酸,所得滴定曲线如图所示。下列说法正确的是
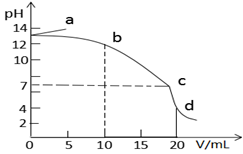
A. a点溶液加水稀释,
 逐渐增大
逐渐增大B. b→c段发生反应的离子方程式是:CH3COO- + H+ = CH3COOH
C. c点时水的电离程度最大
D. d点溶液中c(Na+)=c(Cl-)>c(CH3COOH)>c(CH3COO-)>c(H+)
高三化学选择题困难题查看答案及解析
-
25℃时,在10mL浓度均为0.1mol/L的NaOH和CH3COONa混合溶液中滴加0.1mol/L的盐酸,所得滴定曲线如图所示。下列说法正确的是

A. a点溶液加水稀释,
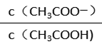 逐渐增大
逐渐增大B. b→c段发生反应的离子方程式是:CH3COO- + H+ = CH3COOH
C. c点时水的电离程度最大
D. d点溶液中c(Na+)=c(Cl-)>c(CH3COOH)>c(CH3COO-)>c(H+)
高三化学选择题困难题查看答案及解析
-
下列有关实验原理或实验操作正确的是
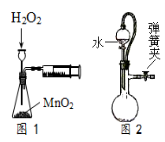
A.将氯化铁固体溶于稀盐酸配制FeCl3溶液
B.称取4.0gNaOH,放入100mL容量瓶中,加水稀释,配制1.0mol·L-1的NaOH溶液
C.利用图1装置定量测定H2O2的分解速率
D.如图2所示,关闭弹簧夹检查装置的气密性
高三化学选择题中等难度题查看答案及解析
-
常温下,用0.1000mol/L的NaOH溶液滴定20ml同浓度的一元弱酸HA,滴定过程溶液pH随X的变化曲线如图所示(忽略中和热效应),下列说法不正确的是
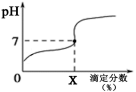
A.HA溶液加水稀释后,溶液中
的值减小
B.HA的电离常数
(x为滴定分数)
C.当滴定分数为100时,溶液中水的电离程度最大
D.滴定分数大于100时,溶液中离子浓度关系一定是c(Na+)>c(A-)>c(OH-)>c(H+)
高三化学选择题困难题查看答案及解析
-
常温下,用0.1000mol/L的NaOH溶液滴定20ml同浓度的一元弱酸HA,滴定过程溶液pH随X的变化曲线如图所示(忽略中和热效应),下列说法不正确的是

A.HA溶液加水稀释后,溶液中
的值减小
B.HA的电离常数
(x为滴定分数)
C.当滴定分数为100时,溶液中水的电离程度最大
D.滴定分数大于100时,溶液中离子浓度关系一定是c(Na+)>c(A-)>c(OH-)>c(H+)
高三化学选择题中等难度题查看答案及解析