利用海水提取溴和镁的过程如下,下列说法不正确的是
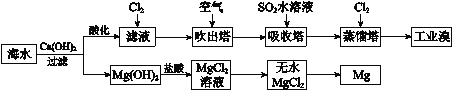
A. 工业溴中含少量Cl2,可用NaOH溶液除去
B. 工业上常利用电解熔融MgCl2冶炼金属镁
C. 富集溴元素过程中,空气吹出法利用了溴易挥发的性质
D. 若提取1 mol Br2,至少需要标准状况下44.8 L的Cl2
高三化学单选题中等难度题
利用海水提取溴和镁的过程如下,下列说法不正确的是

A. 工业溴中含少量Cl2,可用NaOH溶液除去
B. 工业上常利用电解熔融MgCl2冶炼金属镁
C. 富集溴元素过程中,空气吹出法利用了溴易挥发的性质
D. 若提取1 mol Br2,至少需要标准状况下44.8 L的Cl2
高三化学单选题中等难度题
利用海水提取溴和镁的过程如下,下列说法不正确的是
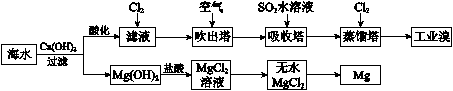
A.工业溴中含少量Cl2,可用NaOH溶液除去
B.工业上常利用电解熔融MgCl2冶炼金属镁
C.富集溴元素过程中,空气吹出法利用了溴易挥发的性质
D.若提取1 mol Br2,至少需要标准状况下44.8 L的Cl2
高三化学选择题中等难度题查看答案及解析
利用海水提取溴和镁的过程如下,下列说法不正确的是
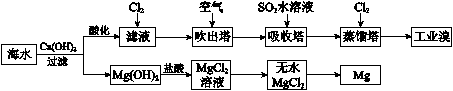
A.工业溴中含少量Cl2,可用NaOH溶液除去
B.工业上常利用电解熔融MgCl2冶炼金属镁
C.富集溴元素过程中,空气吹出法利用了溴易挥发的性质
D.若提取1 mol Br2,至少需要标准状况下44.8 L的Cl2
高三化学选择题中等难度题查看答案及解析
利用海水提取溴和镁的过程如下,下列说法不正确的是

A. 工业溴中含少量Cl2,可用NaOH溶液除去
B. 工业上常利用电解熔融MgCl2冶炼金属镁
C. 富集溴元素过程中,空气吹出法利用了溴易挥发的性质
D. 若提取1 mol Br2,至少需要标准状况下44.8 L的Cl2
高三化学单选题中等难度题查看答案及解析
海水开发利用的部分过程如图所示。下列说法错误的是
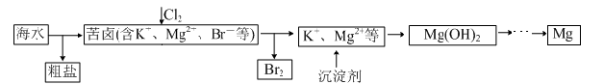
A.粗盐可采用除杂和重结晶等过程提纯
B.向苦卤中通入Cl2 是为了提取溴
C.实际生产中常选用Ca(OH)2 作为沉淀剂
D.工业生产中电解熔融氧化镁的方法制取镁
高三化学选择题中等难度题查看答案及解析
如图为海水综合利用的部分模拟过程。

下列有关说法正确的是
A. ① 中加入试剂顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液
B. 过程②为电解熔融精盐
C. 工业上过程③加入的试剂为浓NaOH溶液
D. 第④步反应的离子方程式可表示为:2Br-+Cl2=Br2+2Cl-
高三化学选择题中等难度题查看答案及解析
如图为海水综合利用的部分模拟过程。

下列有关说法正确的是
A.① 中加入试剂顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液
B.过程②为电解熔融精盐
C.工业上过程③加入的试剂为浓NaOH溶液
D.第④步反应的离子方程式可表示为:2Br-+Cl2=Br2+2Cl-
高三化学单选题中等难度题查看答案及解析
对海水进行开发利用的部分流程如下图所示。下列说法不正确的是
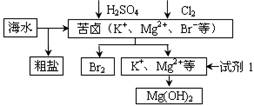
A.可用BaCl2溶液除去粗盐中的SO42-
B.从苦卤中提取Br2的反应的离子方程式为:2Br- + Cl2 == 2Cl- + Br2
C.试剂1可以选用石灰乳
D.工业上,电解熔融Mg(OH)2冶炼金属镁
高三化学选择题中等难度题查看答案及解析
下图为氯碱工业的简易装置示意图,其中两电极均为惰性电极。下列说法正确的是
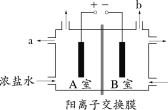
A.粗盐水中含有的少量Ca2+和Mg2+可用NaOH除去
B.适当降低阳极电解液的pH有利于Cl2逸出
C.a处得到的是浓NaOH溶液
D.若电路中通过0.2mol电子,理论上可在b处得到标准状况下1.12L气体
高三化学单选题中等难度题查看答案及解析
从淡化海水中提取溴的流程如下:
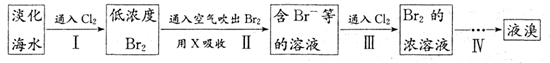
下列有关说法不正确的是
A.X试剂可用Na2SO3饱和溶液
B.步骤Ⅲ的离子反应:2Br- + Cl2 = 2Cl- +Br2
C工业上每获得1 mol Br2,需要消耗Cl2 44.8 L
D.步骤IV包含萃取、分液和蒸馏
高三化学选择题中等难度题查看答案及解析
下列解释事实的化学方程式或离子方程式,不正确的是
A.工业上可用电解法制备Mg:MgCl2(熔融) Mg + Cl2↑[
B.向Ca(ClO)2溶液中通入少量CO2:Ca2+ + 2ClO-+H2O+CO2 == 2HClO +CaCO3↓
C.用CaSO4治理盐碱地:CaSO4(s) + Na2CO3(aq) == CaCO3(s) + Na2SO4(aq)
D.用FeSO4除去酸性废水中的Cr2O72-:Cr2O72- + Fe2+ + 14H+ == 2Cr3+ + Fe3+ + 7H2O
高三化学选择题中等难度题查看答案及解析