-
两位同学设计实验确定某一元酸HA是弱电解质并分析其中的变化,实验方案如下:
甲:取纯度、质量、大小相同的锌粒于两只相同气球中,向2支试管中分别加入浓度均为0.1mol/L的HA溶液和稀盐酸各10mL,将气球套在试管上,并同时将锌粒加入试管。
乙:方案一:用pH计测定浓度为0.1mol/L HA溶液的pH;
方案二:取pH=3的HA溶液5mL稀释至500mL,再用pH计测其pH。
(1)甲同学设计的方案中,说明HA是弱电解质的实验现象是_________(填字母)。
a. 两个试管上方的气球同时鼓起,且一样大
b. 装有HA溶液的试管上方的气球鼓起慢
c. 装有盐酸的试管上方的气球鼓起慢
(2)乙同学设计的方案可证明HA是弱电解质:方案一中,测得0.1mol/L的HA溶液的pH________1(填“>”“<”或“=”);方案二中,所得结果是_________。
(3)若从水解原理角度设计一个合理而比较容易进行的方案(药品可任取),证明HA是弱电解质,你的设计方案是_________。
(4)乙同学根据HA在溶液中的电离平衡移动的原理,进一步做下列分析。
①使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1mol/L的HA溶液中,选择加入___________试剂。
②使HA的电离程度减小,c(H+)和c(A-)都增大,可在0.1mol/L的HA溶液中,选择加入________试剂。
高二化学综合题中等难度题查看答案及解析
-
两位同学设计实验确定某一元酸HA是弱电解质并分析其中的变化,实验方案如下:
甲:取纯度、质量、大小相同的锌粒于两只相同气球中,向2支试管中分别加入浓度均为0.1mol/L的HA溶液和稀盐酸各10mL,将气球套在试管上,并同时将锌粒加入试管。
乙:用pH计测定浓度为0.1mol/LHA溶液的pH;
(1)甲同学设计的方案中,说明HA是弱电解质的实验现象是_________(填字母)。
a. 两个试管上方的气球同时鼓起,且一样大
b. 装有HA溶液的试管上方的气球鼓起慢
c. 装有盐酸的试管上方的气球鼓起慢
(2)乙同学设计的方案可证明HA是弱电解质:测得0.1mol/L的HA溶液的pH________1(填“>”“<”或“=”)。
(3)若从水解原理角度设计一个合理而比较容易进行的方案(药品可任取),证明HA是弱电解质,你的设计方案是_________。
(4)乙同学根据HA在溶液中的电离平衡移动的原理,进一步做下列分析。
①使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1mol/L的HA溶液中,选择加入___________试剂。
②使HA的电离程度减小,c(H+)和c(A-)都增大,可在0.1mol/L的HA溶液中,选择加入________试剂。
A.NaA固体 B.1mol/LNaOH溶液
C. 0.1mol/LH2SO4 溶液 D.2mol/LHA
高二化学实验题中等难度题查看答案及解析
-
甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动。实验方案如下:
甲:取纯度相同,质量、大小相等的锌粒于两只试管中,同时加入0.1 mol·L-1的 HA、HCl溶液各10 mL,按图装好,观察现象;
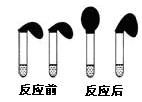
乙:① 用pH计测定物质的量浓度均为0.1 mol·L-1 HA和HCl溶液的pH;
② 再取0.1 mol·L-1的HA和HCl溶液各2滴(1滴约为1/25 mL)分别稀释至100 mL,再用pH计测其pH变化
(1)乙方案中说明HA是弱电解质的理由是:测得0.1 mol·L-1的HA溶液的pH1(填“>”、“<”或“=”) ;甲方案中,说明HA是弱电解质的实验现象是:________
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后, 试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第______步,能证明改变条件弱电解质平衡发生移动。甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:①使HA的电离程度和c(H+)都减小, c(A-)增大,可在0.1 mol·L-1的HA溶液中,选择加入_________试剂(选填“A”“B”“C”“D”,下同);②使HA的电离程度减小,c(H+)和c(A-)都增大,可在0.1 mol·L-1的HA溶液中,选择加入_____试剂。
A. NaA固体(可完全溶于水)
B.1 mol·L-1 NaOH溶液
C. 1 mol·L-1 H2SO4 D.2 mol·L-1 HA
(3)pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积V的关系如图所示,则下列说法不正确的有 ________
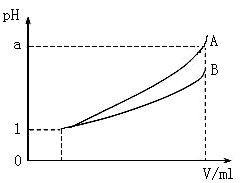
A.两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸
E.稀释后A溶液中水的电离程度比B溶液中水的电离程度小
高二化学填空题简单题查看答案及解析
-
甲、乙两位同学设计实验确定某酸HA是弱电解质,实验方案如下:
甲:取纯度相同,质量、大小相等的锌粒于两支试管中,同时加入 0.1 mol·L-1 的HA溶液、稀盐酸各10 mL,按图装好,观察现象。

乙:方案一:用pH计测定浓度为 0.1 mol·L-1HA溶液的pH;
方案二:取pH=3的HA溶液5 mL稀释至500 mL,再用pH计测其pH。
回答下列问题:
(1)甲同学设计的方案中,说明HA是弱电解质的实验现象是___________ (填序号)。
A. 加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
B. 加入HA溶液后,试管上方的气球鼓起慢
C. 加入稀盐酸后,试管上方的气球鼓起慢
(2)乙同学设计的方案一中说明HA是弱电解质的理由是:测得 0.1 mol·L-1 的HA溶液的pH ______1(填“>”、“<”或“=”);
(3)乙同学设计的方案二能证明改变条件,弱电解质电离平衡发生移动。乙同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:
①使HA的电离程度和c(H+)都减小,c(A-)增大,可在 0.1mol·L-1 的HA溶液中,选择加入____________试剂;
②使HA的电离程度减小,c(H+)和c(A-)都增大,可在 0.1mol·L-1 的HA溶液中,选择加入_____________试剂。
(4)若从水解原理角度设计一个合理而比较容易进行的方案(药品可任取) ,证明HA是弱电解质,你的设计方案是________________________________。
高二化学实验题中等难度题查看答案及解析
-
甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动.实验方案如下:
甲:取纯度相同,质量、大小相等的锌粒于两只试管中,同时加入0.1mol•L-1的 HA、HCl溶液各10mL,按图1装好,观察现象;
乙:①用pH计测定物质的量浓度均为0.1mol•L-1HA和HCl溶液的pH;
②再取0.1mol•L-1的HA和HCl溶液各2滴(1滴约为mL)分别稀释至100mL,再用pH计测其pH变化
(1)乙方案中说明HA是弱电解质的理由是:测得0.1mol•L-1的HA溶液的pH______1(填“>”、“<”或“=”);甲方案中,说明HA是弱电解质的实验现象是:______
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后,试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第______步,能证明改变条件弱电解质平衡发生移动.甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:
①使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1mol•L-1的HA溶液中,选择加入______试剂(选填“A”“B”“C”“D”,下同);
②使HA的电离程度减小,c(H+)和c(A-)都增大,可在0.1mol•L-1的HA溶液中,选择加入______试剂.
A.NaA固体(可完全溶于水)
B.1mol•L-1NaOH溶液
C.1mol•L-1H2SO4
D.2mol•L-1HA
(3)pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图2所示,则下列说法不正确的有______
A.两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸
E.稀释后A溶液中水的电离程度比B溶液中水的电离程度小.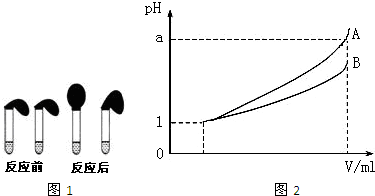
高二化学解答题中等难度题查看答案及解析
-
甲、乙两位同学设计实验确定某酸HA是弱电解质,实验方案如下:
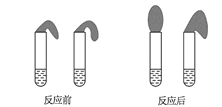
甲:取纯度相同,质量、大小相等的锌粒于两支试管中,同时加入浓度均为0.1 mol·L-1 的HA溶液、稀盐酸各10 mL,按图装好,观察现象。
乙:方案一:用pH计测定浓度为 0.1 mol·L-1HA溶液的pH;
方案二:取pH=3的HA溶液5 mL稀释至500 mL,再用pH计测其pH。
回答下列问题:
(1)甲同学设计的方案中,说明HA是弱电解质的实验现象是___________ (填序号)。
A. 加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
B. 加入HA溶液后,试管上方的气球鼓起慢
C. 加入稀盐酸后,试管上方的气球鼓起慢
(2)乙同学设计的方案一中说明HA是弱电解质的理由是:__________________
(3)乙同学设计的方案二中说明HA是弱电解质的pH的范围为__________________
(4)丙同学为了进一步证明外界条件对弱电解质电离平衡移动的情况,设计如下实验:
①使HA的电离程度和c(H+)都减小,c(A-)增大,可在 0.1mol·L-1 的HA溶液中,选择加入____________试剂;
②使HA的电离程度减小,c(H+)和c(A-)都增大,可在 0.1mol·L-1 的HA溶液中,选择加入_____________试剂。
(5)若从盐类水解原理角度设计一个合理而比较容易进行的方案(药品可任取) ,证明HA是弱电解质,你的设计方案是________________________________。
高二化学实验题中等难度题查看答案及解析
-
甲、乙两位同学设计实验确定某酸HA是弱电解质,实验方案如下:
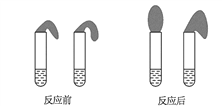
甲:取纯度相同,质量、大小相等的锌粒于两支试管中,同时加入浓度均为0.1 mol·L-1 的HA溶液、稀盐酸各10 mL,按图装好,观察现象。
乙:方案一:用pH计测定浓度为 0.1 mol·L-1HA溶液的pH;
方案二:取pH=3的HA溶液5 mL稀释至500 mL,再用pH计测其pH。
回答下列问题:
(1)甲同学设计的方案中,说明HA是弱电解质的实验现象是___________ (填序号)。
A. 加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
B. 加入HA溶液后,试管上方的气球鼓起慢
C. 加入稀盐酸后,试管上方的气球鼓起慢
(2)乙同学设计的方案一中说明HA是弱电解质的理由是:__________________
(3)乙同学设计的方案二中说明HA是弱电解质的pH的范围为__________________
(4)丙同学为了进一步证明外界条件对弱电解质电离平衡移动的情况,设计如下实验:
①使HA的电离程度和c(H+)都减小,c(A-)增大,可在 0.1mol·L-1 的HA溶液中,选择加入____________试剂;
②使HA的电离程度减小,c(H+)和c(A-)都增大,可在 0.1mol·L-1 的HA溶液中,选择加入_____________试剂。
(5)若从盐类水解原理角度设计一个合理而比较容易进行的方案(药品可任取) ,证明HA是弱电解质,你的设计方案是________________________________。
高二化学实验题中等难度题查看答案及解析
-
(12分)甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动。实验方案如下: 甲:①准确配制0.1 mol·L-1的HA、HCl溶液各100 mL;
②取纯度相同,质量、大小相等的锌粒于两只试管中,同时加入0.1 mol·L-1的 HA 、HCl溶液各10 mL,按图装好,观察现象
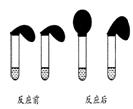
乙:①用pH计测定物质的量浓度均为0.1 mol·L-1 HA和HCl溶液的pH;
②再取0.1 mol·L-1的HA和HCl溶液各2滴(1滴约为1/20 mL)分别稀释至100 mL,再用pH计测其pH变化
(1) 甲、乙两方案中都要用到__________ mL的容量瓶。乙方案中说明HA是弱电解质的理由是,测得0.1 mol·L-1的HA溶液的pH1(填“>”、“<”或“=”) ;甲方案中,说明HA是弱电解质的实验现象是:________
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后, 试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第______步,能证明改变条件弱电解质平衡发生移动。甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:①使HA的电离程度和c(H+)都减小, c(A-)增大,可在0.1 mol/L的HA溶液中,选择加入_________试剂;②使HA的电离程度减小,c(H+)和c(A-)都增大,可在0.1 mol/L的HA溶液中,选择加入________试剂。
A. NaA固体(可完全溶于水) B.1 mol/LNaOH溶液
C. 1 mol/L H2SO4 D.2 mol/LHA
(3)pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积V的关系如图所示。
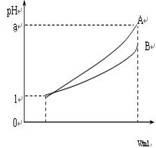
则下列说法不正确的有( )。
A.两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸
高二化学实验题简单题查看答案及解析
-
某纯碱样品中含有少量氯化钠,现欲测定其碳酸钠的质量分数,设计如下实验方案:
(方案1)称取一定质量的纯碱样品(已知锥形瓶和硫酸溶液的质量190.720 g),利用左图装置测定纯碱样品的纯度,每隔相同时间读得电子天平的数据如表:
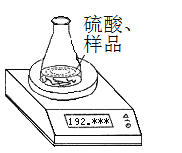
读数次数
质量(g)
锥形瓶+硫酸+试样
第1次
192.955
第2次
192.764
第3次
192.328
第4次
192.075
第5次
192.075
(1)计算纯碱样品的纯度时,必需的数据是_____________________________(填具体数据)。不必作第6次读数的原因是________________________________________________。
(2)计算纯碱样品的纯度为_________________________(保留小数后两位)。
(方案2)测定上述样品(1.15 g)中,Na2CO3质量分数的另一种方案,其操作流程如下:
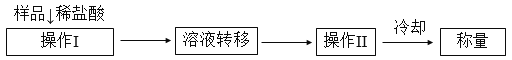
(1)溶液转移至__________(填写仪器名称),操作II的名称是______________。
(2)需直接测定的物理量是____________________。
(3)测定过程中需要的仪器有电子天平.蒸发皿、酒精灯、还需要__________、__________(固定、夹持仪器除外)。
(4)在转移溶液时,如溶液转移不完全,则Na2CO3质量分数的测定结果__________(填“偏小”、“偏大”或“不变”)
(方案3)实验装置如图:
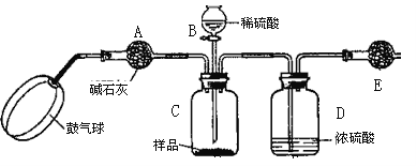
实验步骤:
①如图连接装置并加入所需药品。
②称量并记录E的质量m1(称量时注意封闭E的两端)。
③按动鼓气球,持续约1分钟。
④连接上E。
⑤打开分液漏斗B的活塞,将稀硫酸快速加入C中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录E的质量m2(称量时注意封闭E的两端及D右端的出口)。
⑧重复步骤⑥和⑦的操作,直到球形干燥管的质量基本不变,记为m3。
⑨计算。
请填空和回答问题:
(1)C中发生反应的离子方程式为:______________________________________。B仪器的名称为__________。如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果将__________(填“偏高”、“偏低”或“不变”)。
(2)浓硫酸的作用是_________________,若没有D,则实验结果__________(填“偏高”、“偏低”或“无影响”)。
(3)步骤③和⑥的作用是____________________,____________________。鼓气球的速度是快速好,还是缓慢鼓入?为什么?__________________________________________。
(4)E装置的固体试剂为__________(填编号)
A.碱石灰 B.无水氯化钙 C.浓硫酸 D.生石灰
(5)步骤⑧的目的是________________________________________________。
(6)试样中纯碱样品的质量分数计算式为_____________________________________。
(7)本实验设计中若有需要改进的地方,请指出该进之处并说明原因。
_______________________________________________________________________。
(8)实验还可以用其它定量实验方法测定试样中纯碱的质量分数,请简述一种不同的定量实验方法。___________________________________________________________ 。
高二化学实验题中等难度题查看答案及解析
-
(5分)甲、乙两同学拟用实验确定某酸HA是弱电解质。他们设计的方案(理论方案)分别是:
甲:①称取一定质量的HA配制0.1 mol/L的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=3的两种酸溶液各100 mL;
②分别取这两种溶液各1 mL,加水稀释为100 mL;
③用两支试管分别取相同体积的两种稀释液,同时加入纯度相同、颗粒大小均等的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是 。
(2)甲方案中,能说明HA是弱电质的理由是测得溶液的pH___1(选填“>”、“<”、“=”)。
(3)关于pH试纸的使用方法,下列叙述正确的是 。
a.pH试纸在使用之前应用蒸馏水润湿
b.将pH试纸直接插入待测溶液,取出后再与标准比色卡对比
c.pH试纸测出的数值应该保留一位小数
d.能使pH试纸显红色的溶液显酸性
(4)乙方案中,说明HA是弱电解质的现象是 。
高二化学实验题困难题查看答案及解析