-
25 ℃时, 用浓度为0.100 0 mol·L-1的NaOH溶液滴定20.00 mL浓度均为0.100 0 mol·L-1的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是( )
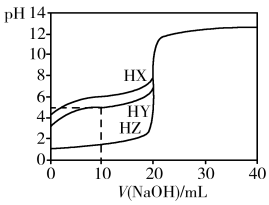
A.根据滴定曲线,可得Ka(HY)≈10-5
B.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>
c(OH-)>c(H+)
D.HY与HZ混合,达到平衡时:c(H+)= +c(Z-)+c(OH-)
+c(Z-)+c(OH-)
-
25 ℃时,用浓度为0.100 0 mol·L-1的NaOH溶液滴定20.00 mL浓度均为0.100 0 mol·L-1的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是
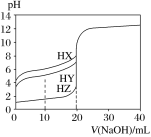
A. 在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
B. 根据滴定曲线可得Ka(HX)的数量级是10-7
C. 将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+)
D. HY与HZ混合,达到平衡时c(H+)=Ka(HY).c(HY)/c(Y-)+c(Z-)+c(OH-)
-
25℃时,用0.100mol/L的NaOH溶液滴定20.00ml、0.100mol/L的HNO2溶液,lg 与所加NaOH溶液体积的关系如图所示,下列说法错误的是
与所加NaOH溶液体积的关系如图所示,下列说法错误的是

A.25℃时,用0.100mol/L的HNO2溶液的pH值为2.75
B.B点对应的溶液中,2c(H+)+c(HNO2)=c(NO2-)+2c(OH-)
C.C点对应溶液的PH=7,加入NaOH溶液的体积为20.00ml
D.滴定过程中从A到D点溶液中水的电离程度先增大后减小
-
25℃时,用0.100 mol·L-1的NaOH溶液滴定20.00 mL 0.100 mol·L-1的HNO2溶液, 与所加NaOH溶液体积的关系如图所示,下列说法错误的是( )
与所加NaOH溶液体积的关系如图所示,下列说法错误的是( )
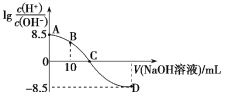
A. 25 ℃时,0.100 mol·L-1的HNO2溶液的pH=2.75
B. B点对应的溶液中,2c(H+)+c(HNO2)=c(NO2-)+2c(OH-)
C. C点对应的溶液的pH=7,加入NaOH溶液的体积为20.00 mL
D. 滴定过程中从A到D点溶液中水的电离程度先增大后减小
-
25℃时,用0.100 mol·L-1的NaOH溶液滴定20.00 mL 0.100 mol·L-1的HNO2溶液, 与所加NaOH溶液体积的关系如图所示,下列说法错误的是( )
与所加NaOH溶液体积的关系如图所示,下列说法错误的是( )
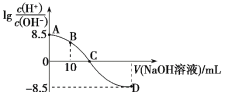
A.25 ℃时,0.100 mol·L-1的HNO2溶液的pH=2.75
B.B点对应的溶液中,2c(H+)+c(HNO2)=c(NO2-)+2c(OH-)
C.C点对应的溶液的pH=7,加入NaOH溶液的体积为20.00 mL
D.滴定过程中从A到D点溶液中水的电离程度先增大后减小
-
25℃时,用0.100 mol/L NaOH溶液分别滴定20.00mL 0.100 mol/L 的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是
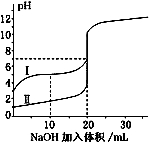
A.II表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗V(NaOH)小于20mL
C.V(NaOH) =20.00mL时,两份溶液中c(Cl-)=c(CH3COO-)
D.V(NaOH) =10.00mL时,醋酸溶液中:c(Na+)>c(CH3COO-)>c(H+ )>c(OH-)
-
常温下,用0.100mol•L-1NaOH溶液分别滴定20.00mL浓度均0.100mol•L-1CH3COOH溶液和HCN溶液,所得滴定曲线如图。下列说法不正确的是( )
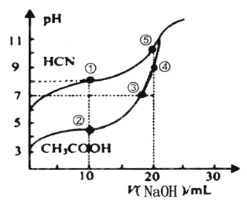
A.点①和点②所示溶液中:c(CH3COO-)>c(CN-)
B.点③时:c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
C.点③和点④所示溶液中水的电离程度:③<④
D.点④溶液中阴离子总数小于点⑤
-
室温条件下,用0.100 mol·L-1的NaOH溶液分别滴定HA和HB两种酸溶液,两种酸溶液的体积均为20.00 mL,浓度均为0.100 mol·L-1,滴定曲线如图所示。下列叙述正确的是( )
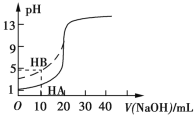
A. HA可以是醋酸,HB可以是HCl
B. 浓度相等时,B-的水解程度大于HB的电离程度
C. V(NaOH)=20.00 mL时,c(Na+)=c(A-)>c(B-)
D. pH=7时,滴定HB溶液消耗的V(NaOH)>20.00 mL
-
化学上常用AG表示溶液中的lg 。25℃时,用0.100 mol•L-1的NaOH溶液滴定20.00 mL 0.100 mol•L-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是
。25℃时,用0.100 mol•L-1的NaOH溶液滴定20.00 mL 0.100 mol•L-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是
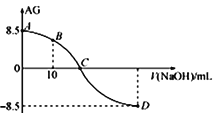
A. 滴定过程中,应选用甲基橙做指示剂
B. B点溶液中存在 c(H+)-c(OH-)=c(NO2-)-c(HNO2)
C. C点时,加入NaOH溶液的体积为20 mL
D. 25℃时,HNO2的电离常数Ka=1.0×10-4.5
-
室温下,用0.100mol•L﹣1的NaOH溶液分别滴定体积和浓度均为20.00mL 0.100mol•L﹣1的盐酸和醋酸滴定曲线如图所示。下列说法错误的是( )
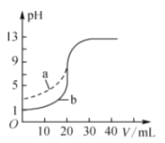
A.a表示的是醋酸的滴定曲线
B.滴定b过程中,指示剂可以是酚酞
C.pH=7时,滴定盐酸消耗的V(NaOH)=20.00mL
D.V(NaOH)=10.00mL时,醋酸中c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣)

+c(Z-)+c(OH-)








