-
A、B、C、D是元素周期表中前四周期的元素,其中A元素p电子总数比s电子总数少1; B元素p电子总数与s电子总数相等,且原子半径比A小;C元素原子3p能级上只有一对成对电子;D元素原子N层上只有1个电子,且次外层的电子充满在2个能级中。请回答以下问题:
(1)写出下列元素的名称:A______ D________。
(2)元素A、B可以形成A2B型共价化合物,写出一种与A2B等电子体的化合物________(用化学式表示)
⑶A和B第一电离能的大小关系为:A____B。(选填“>”、“<”或“ = ”)
⑷B和C元素对应的气态氢化物,沸点较髙的是______(填化学式),原因是______________。
高二化学推断题中等难度题查看答案及解析
-
A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
元素
相关信息
A
原子核外有6种不同运动状态的电子
C
基态原子中s电子总数与p电子总数相等
D
原子半径在同周期元素中最大
E
基态原子最外层电子排布式为3s23p1
F
基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反
G
基态原子核外有7个能级且能量最高的能级上有6个电子
H
是我国使用最早的合金中的最主要元素
请用化学用语填空:
(1) A元素在元素周期表中的位置________;A、B、C三种元素的第一电离能由大到小的排序为_____(用元素符号填写);
(2) B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为____,B元素所形成的单质分子中σ键与π键数目之比为____。
(3) G元素的低价阳离子的离子结构示意图是________,F元素原子的外围电子排布图是________,H元素的基态原子核外电子排布式是________。
(4) D元素的单质及其常见化合物的焰色反应主要利用了原子光谱中的______(A.原子吸收光谱B.原子发射光谱)
(5) 上述元素属于p区的是_______(用元素符号填写);
高二化学推断题中等难度题查看答案及解析
-
A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
元素
相关信息
A
原子核外有6种不同运动状态的电子
C
基态原子中s电子总数与p电子总数相等
D
原子半径在同周期元素中最大
E
基态原子最外层电子排布式为3s23p1
F
基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反
G
基态原子核外有7个能级且能量最高的能级上有6个电子
H
是我国使用最早的合金中的最主要元素
请用化学用语填空:
(1)A元素位于元素周期表第_______周期_______族;C元素和F元素的电负性比较,较小的是________。
(2)D的单质在空气中燃烧时火焰的颜色是__________________,请用原子结构的知识解释发光的原因:__________________________。
(3)H元素位于元素周期表的_________区。基态E原子的L层电子排布图为__________。
(4)B元素与宇宙中含量最丰富的元素形成的最简单化合物的VSEPR模型为________,B元素与同周期相邻两元素的电离能大小关系为______________ , 请解释原因__________________________________。
(5)G元素的低价阳离子的离子结构示意图是________,F元素原子的价电子的电子排布图是________。
(6)在基态G中,电子占据的最高能层符号为________,该能层具有的原子轨道数为____________。
(7)G的高价阳离子的溶液与H单质反应的离子方程式为___________________________;
(8)与E元素成对角线关系的某元素的最高价氧化物的水化物具有两性,写出该两性物质与D元素的最高价氧化物的水化物反应的离子方程式:________________________。
高二化学填空题中等难度题查看答案及解析
-
A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
元素
相关信息
A
原子核外有6种不同运动状态的电子
C
基态原子中s电子总数与p电子总数相等
D
原子半径在同周期元素中最大
E
基态原子价层电子排布式为3s23p1
F
基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反
G
基态原子核外有7个能级且能量最高的能级上有6个电子
H
是我国使用最早的合金中的最主要元素
请用化学用语填空:
(1)A元素在元素周期表中的位置______,B元素和C元素的第一电离能比较,较大的是___________,C元素和F元素的电负性比较,较小的是_____________。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为____________,B元素所形成的单质分子中
键与π数目之比为_________。
(3)G元素的低价阳离子的结构示意图是_________________,F元素原子的价电子排布图是__________,H元素的基态原子核外电子排布式是________________________________________。
(4)G的高价阳离子的溶液与H单质反应的离子方程式为_____________________________;与E元素成对角关系的某元素的最高价氧化物对应的水化物具有两性,该两性物质与D元素的最高价氧化物对应的水化物反应的化学方程式为________________________________。
高二化学填空题困难题查看答案及解析
-
X、Y、Z、M、Q、R是元素周期表前四周期元素,且原子序数依次增大,其相关信息如下表:
元素
相关信息
X
原子核外有6种不同运动状态的电子
Y
基态原子中s电子总数与p电子总数相等
Z
原子半径在同周期元素中最大
M
逐级电离能(kJ·mol-1)依次为 578、1817、2745、11575、14830、18376
Q
基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反
R
基态原子核外有7个能级且能量最高的能级上有6个电子
请用化学用语填空:
(1)X元素位于元素周期表第____周期____族; R是________区的元素。
(2)请写出Q元素基态原子的外围电子排布图____。
(3)X、Y、Z、M四种元素的原子半径由小到大的顺序是________。(用元素符号表示)
(4)R元素可形成R2+和R3+,其中较稳定的是R3+,原因是________。
(5)含Z元素的焰火显黄色,主要与________有关。
(6)M元素原子的逐级电离能越来越大的原因是________。
(7)与M元素成“对角线规则”关系的某短周期元素T的最髙价氧化物的水化物具有两性,写出该两性物质与Z元素的最高价氧化物的水化物反应的化学方程式:________;己知T元素和Q元素的电负性分别为1.5和3.0,则它们形成的化合物是________。(填“离子化合物”或“共价化合物”)
高二化学推断题简单题查看答案及解析
-
X、Y、Z、M、Q、R是元素周期表前四周期元素,且原子序数依次增大,其相关信息如下表:
元素
相关信息
X
原子核外有6种不同运动状态的电子
Y
基态原子中s电子总数与p电子总数相等
Z
原子半径在同周期元素中最大
M
逐级电离能(kJ/mol)依次为 578、1 817、2 745、11 575、14 830、18 376
Q
基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反
R
基态原子核外有7个能级且能量最高的能级上有6个电子
请用化学用语填空:
(1)请写出Q元素基态原子的外围电子排布图:_______。
(2)X、Y、Z、M四种元素的原子半径由大到小的顺序是__________(用元素符号表示)。
(3)R元素可形成R2+和R3+,其中较稳定的是R3+,原因是__________。
(4)写出Z元素的原子核外电子排布式_________。
(5)Q元素原子的未成对电子个数是________ 个。
高二化学综合题中等难度题查看答案及解析
-
X、Y、Z、M、Q、R是元素周期表前四周期元素,且原子序数依次增大,其相关信息如下表:
元素
相关信息
X
原子核外有6种不同运动状态的电子
Y
基态原子中s电子总数与p电子总数相等
Z
原子半径在同周期元素中最大
M
逐级电离能(kJ·mol-1)依次为 578、1817、2745、11575、14830、18376
Q
基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反
R
基态原子核外有7个能级且能量最高的能级上有6个电子
请用化学用语填空:
(1)X元素位于元素周期表第____周期____族; R是________区的元素。
(2)请写出Q元素基态原子的外围电子排布图____。
(3)X、Y、Z、M四种元素的原子半径由小到大的顺序是________。(用元素符号表示)
(4)R元素可形成R2+和R3+,其中较稳定的是R3+,原因是________。
(5)含Z元素的焰火显黄色,主要与________有关。
(6)M元素原子的逐级电离能越来越大的原因是________。
(7)与M元素成“对角线规则”关系的某短周期元素T的最髙价氧化物的水化物具有两性,写出该两性物质与Z元素的最高价氧化物的水化物反应的化学方程式:________;己知T元素和Q元素的电负性分别为1.5和3.0,则它们形成的化合物是________。(填“离子化合物”或“共价化合物”)
高二化学推断题简单题查看答案及解析
-
A、B、C、D, E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
元素
相关信息
A
原子核外有6种不同运动状态的电子
C
基态原子中s电子总数与p电子总数相等
D
原子半径在同周期元素中最大
E
基态原子最外层电子排布式为3s23p1
F
基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反
G
基态原子核外有7个能级且能量最高的能级上有6个电子
H
是我国使用最早的合金中的最主要元素
请用化学用语填空:
(1)A元素位于元素周期表第_______周期_______族;B元素和C元素的第一电离能比较,较大的是________,C元素和F元素的电负性比较,较小的是________。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子模型为________,B元素所形成的单质分子
键与π键数目之比为________。
(3)G元素的低价阳离子的离子结构示意图是________,F元素原子的价电子的轨道表示式是________,H元素的基态原子核外电子排布式的________。
(4)G的高价阳离子的溶液与H单质反应的离子方程式为_________________;与E元素成对角线关系的某元素的最高价氧化物的水化物具有两性,写出该两性物质与D元素的最高价氧化物的水化物反应的离子方程式:_________________。
高二化学推断题中等难度题查看答案及解析
-
(12分)已知A、B、C、D、E、F均为周期表中前36号元素,且原子序数依次增大。A、B、C为同一周期的主族元素,B原子p能级电子总数与s能级电子总数相等。A、F原子未成对电子是同周期中最多的,且F基态原子中电子占据三种不同形状的原子轨道。D和E原子的第一至第四电离能如下表所示:
电离能/ kJ·mol-1
I1
I2
I3
I4
D
738
1451
7733
10540
E
578
1817
2745
11578
⑴A、B、C三种元素的电负性最大的是▲ (填写元素符号),D、E两元素中D的第一电离能较大的原因是▲ 。
⑵F基态原子的核外电子排布式是▲ ;在一定条件下,F原子的核外电子从基态跃迁到激发态产生的光谱属于▲ 光谱(填“吸收”或“发射”)。
⑶根据等电子原理,写出AB+的电子式:▲ 。
⑷已知:F3+可形成配位数为6的配合物。组成为FCl3·6H2O的配合物有3种,分别呈紫色、蓝绿色、绿色,为确定这3种配合物的成键情况,分别取等质量的紫色、蓝绿色、绿色3种物质的样品配成溶液,分别向其中滴入过量的AgNO3溶液,均产生白色沉淀且质量比为3∶2∶1。则绿色配合物的化学式为▲ 。
A.[CrCl (H2O)5]Cl2·H2O B.[CrCl2(H2O)4]Cl·2H2O
C.[Cr(H2O)6]Cl3 D.[CrCl3(H2O)3] ·3H2O
高二化学填空题简单题查看答案及解析
-
(12分)周期表前四周期的元素A、B、C、D、E,原子序数依次增大。A的核外电子总数与其周期数相同,B的价电子层中的未成对电子有3个,B与C同周期,且C的s能级电子总数与p能级电子总数相等,D与C同族;E的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)E+离子的基态核外电子排布
(2)B、C、D中第一电离能由大到小的顺序为 (填元素符号)
(3)A和B、C两元素形成的两种共价化合物发生反应,生成BA4+离子,该离子的中心原子的杂化方式为 ;与BA4+离子互为等电子体的一种分子为 (填化学式)。
(4)E的硫酸盐溶液中滴加过量的氨水可以生成配合物[E(NH3)4]SO4,1 mol配合物中含有的σ键的数目为 。
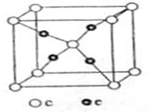
(5)E和C(空心小球为C,实心小球为E)形成的一种离子化合物的晶体结构如图所示,则离子化合物的化学式为
高二化学填空题困难题查看答案及解析