-
(15分)某化学探究小组拟用废铜屑制取Cu(NO3)2:,并探究其化学性质。
I.如图,用浓HNO3,和过量的废铜屑充分反应制硝酸铜溶液。
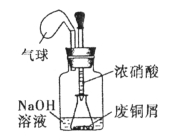
(1)写出铜与浓硝酸反应的离子方程式 。
(2)①装置中NaOH溶液的作用是 。
②欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤是蒸发浓缩、 、过滤。
③你认为此装置是否合理,并说明原因 。
如果不合理,同时在原装置上改进;如果合理,只需说明原因。
Ⅱ.为了探究 的热稳定性,探究小组按下图装置进行实验。(图中铁架台、铁夹和加热仪器均略去)
的热稳定性,探究小组按下图装置进行实验。(图中铁架台、铁夹和加热仪器均略去)
【实验装置】
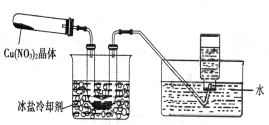
【实验操作及现象】往试管中放人研细的无水Cu(NO3)2:晶体并加热,观察到试管中有红棕色气体生成,最终残留黑色粉末;用U型管除去红棕色气体,在集气瓶中收集到无色气体。
【解释与结论】
(3)①红棕色气体是 。
②根据现象判断 在加热条件下可以分解,其化学反应方程式为 。
在加热条件下可以分解,其化学反应方程式为 。
Ⅲ.利用Cu(NO3)2制备浅绿色的碱式碳酸铜[CuCO3·Cu(OH)2]。
向大试管中加入一定量的碳酸钠溶液和硝酸铜溶液,水浴加热,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡、静置、过滤、洗涤、干燥,得到样品。
【实验数据】反应温度对样品的影响
| 实验序号 | 1 | 2 | 3 | 4 |
| 温度/℃ | 35 | 50 | 70 | 95 |
| 样品颜色 | 深蓝色 | 深蓝色 | 浅绿色 | 暗蓝色 |
| 样品中碱式碳酸铜 的质量分数/% | 90.9 | 92.7 | x | 92.0 |
(4)滤液中可能含有 ,写出检验
,写出检验 的方法 。
的方法 。
(5)95℃时,样品颜色发暗的原因:____ 。
(6)70C时,实验得到2.38 g样品,取此样品加热至分解完全(杂质不分解),得到1.76 g固体,此样品中碱式碳酸铜的质量分数是 。
-
某化学探究小组拟用废铜屑制取Cu(NO3)2并探究其化学性质。
I、如右图所示,用浓HNO3和过量的废铜屑充分反应制硝酸铜溶液。
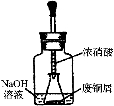
(1)写出铜与浓硝酸反应的离子方程式 。
(2)①装置中NaOH溶液的作用是 。
②欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤依次是:蒸发浓缩、 、过滤、 、烘干。
③你认为此装置是否合理,并说明原因 。
Ⅱ、为了探究Cu(NO3)2热稳定性,探究小组按下图装置进行实验。(图中铁架台、铁夹和加热仪器均略去)
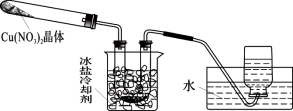
(3)往试管中放入研细的无水Cu(NO3)2晶体并加热,观察到试管中有红棕色气体生成,最终残留黑色粉末;在集气瓶中收集到无色气体。由此判断Cu(NO3)2受热分解的化学方程式为 。
Ⅲ、利用Cu(NO3)2制备浅绿色的碱式碳酸铜[CuCO3·Cu(OH)2]。
向大试管中加入一定量的碳酸钠溶液和硝酸铜溶液,水浴加热,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡、静置、过滤、洗涤、干燥,得到样品。下表是化学探究小组的实验记录,据此回答相关问题:
| 实验序号 | 1 | 2 | 3 | 4 |
| 温度/℃ | 35 | 50 | 70 | 95 |
| 样品颜色 | 深蓝色 | 深蓝色 | 浅绿色 | 暗蓝色 |
(4)95℃时,制得的样品颜色发暗的可能原因是: 。
(5)70℃时,实验得到3.82 g样品,取此样品加热至分解完全(杂质不反应),得到3.20 g固体,此样品中碱式碳酸铜的质量分数是 。
-
(15分)实验室以废铜屑为原料制取碱式碳酸铜【Cu2(OH)2CO3】的步骤如下:
步骤一:废铜屑制硝酸铜
如图,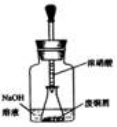
用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70℃左右,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
步骤三:碱式碳酸铜的组成测定
碱式碳酸铜可表示为:xCuCO3 ·yCu (OH)2 ·zH2O,可采用氢气还原法来确定,其反应原理为:
xCuCO3 ·yCu (OH)2 ·zH2O + H2→ Cu + CO2 + H2O(未配平)
完成下列填空:
(1)步骤一中,反应开始时,瓶内的现象是 ,
用该装置制取硝酸铜,好处是 。
(2)步骤二中,水浴加热所需仪器有 、 (加热、夹持仪器、石棉网除外);洗涤的目的是 。
(3) 步骤三中,①以字x、y、z母为系数,配平氢气还原法的化学方程式:
xCuCO3 ·yCu (OH)2 ·zH2O+ H2→ Cu+ CO2+ H2O
②称取24.0g某碱式碳酸铜样品,充分反应后得到12.8 g残留物,生成4.4g二氧化碳和7.2g水。该样品中结晶水质量为 g,化学式为 。
-
碱式碳酸铜 [Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
步骤一:废铜屑制硝酸铜
如图,用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
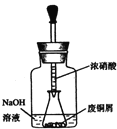
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠和硝酸铜溶液,水浴加热至70℃左右,用0.4mol/L的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
完成下列填空:
(1)写出浓硝酸与铜反应的离子方程式___________________________________。
(2)上图装置中NaOH溶液的作用是__________________________________________。
(3)步骤二中,水浴加热所需仪器有_________、________(加热、夹持仪器、石棉网除外);洗涤的目的是______________________________________________。步骤二的滤液中可能含有CO32-,写出检验CO32-的方法_______________________________________。
(4)影响产品产量的主要因素有________________________________________。
(5)若实验得到2.42g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80g固体,此样品中碱式碳酸铜的质量分数是_________________(保留两位小数)。
-
碱式碳酸铜 Cu2(OH)2CO3是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
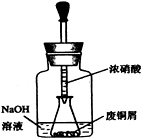
步骤一:废铜屑制硝酸铜:如图,用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液.
步骤二:碱式碳酸铜的制备:向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70℃左右,用0.4mol/L的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品.完成下列填空:
①如图装置中NaOH溶液的作用是______.反应结束后,广口瓶内的溶液中,除了含有NaOH外,还有______(填写化学式).
②步骤二中,水浴加热所需仪器有______、______(加热、夹持仪器、石棉网除外);洗涤的目的是______.
③步骤二的滤液中可能含有CO32-,写出检验CO32-的方法.
④若实验得到2.42g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80g固体,此样品中碱式碳酸铜的质量分数是______.
-
碱式碳酸铜【Cu2(OH)2CO3】是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
步骤一:废铜屑制硝酸铜
如图,用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
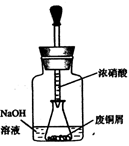
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70℃左右,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
完成下列填空:
(1)写出浓硝酸与铜反应的离子方程式:________。
(2)上图装置中NaOH溶液的作用是_ 。反应结束后,广口瓶内的溶液中,除了含有NaOH外,还有____________(填写化学式)。
(3)步骤二中,水浴加热所需仪器有___________、_(加热、夹持仪器、石棉网除外);
(4)步骤二的滤液中可能含有CO32-,写出检验CO32-的方法:
________
(5)影响产品产量的主要因素有____________。
(6)若实验得到2.42 g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80 g固体,此样品中碱式碳酸铜的质量分数是____。
-
工业上用洗净的废铜屑作原料制取硝酸铜。为节约原料和防止环境污染,宜采取的方法是( )
A. Cu+HNO3(浓)―→Cu(NO3)2
B. Cu+HNO3(稀)―→Cu(NO3)2

-
下列表示对应化学反应的离子方程式正确的是
A.将过量SO2通入少量氨水中:SO2+2NH3·H2O==2NH4++SO32-
B.实验室用Cu和稀HNO3反应制取少量NO气体:Cu+4H++NO3- ==Cu2++NO↑+2H2O
C.NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O
D.KIO3与KI在酸性溶液中反应:5I-+IO3-+3H2O==3I2+6OH-
-
【选修2-化学与技术】(15分)
“烂版液”是制印刷锌板时,用稀硝酸腐蚀锌板后得到的“废液”(含有少量的Cl-、Fe3+),某化学兴趣小组拟用“烂版液”制取Zn(NO3)2·6H2O的过程如下:
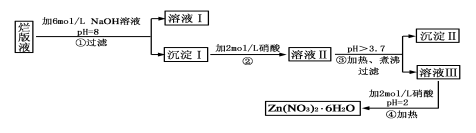
已知:Zn(NO3)2·6H2O是一种无色晶体,水溶液呈酸性,Zn(NO3)2能与碱反应,得到的产物具有两性。
(1)“烂版液”中溶质的主要成分是________(填化学式),若稀硝酸腐蚀锌板产生的气体为N2O,写出稀硝酸腐蚀锌板反应的主要化学方程式______________________。
(2)在操作①中保持pH=8的目的是_________________________________。
(3)沉淀Ⅰ的主要成分是___________________________________________。
(4)操作③中加热、煮沸的目的是___________。此步骤操作的理论依据是_______________。
(5)操作④保持pH=2的目的是_______。此步骤操作中所用的主要仪器是_____ ______。
-
为了探究Cu(NO3)2的氧化性和热稳定性,某化学兴趣小组设计了如下实验。
回答下列问题:
Ⅰ.Cu(NO3)2的氧化性
将光亮的铁丝伸入Cu(NO3)2溶液中,充分反应后将铁丝取出。为检验铁的氧化产物,进行如下实验。(可选用试剂:KSCN溶液、K3[Fe(CN)6]溶液、氯水)
(1)请完成下表:
| 操作 | 现象 | 结论 |
| 取少量溶液于试管中,加入KSCN溶液,振荡 | ① | 不存在Fe3+ |
| 另取少量溶液于试管中,加入 ② ,振荡 | 蓝色沉淀 | 存在Fe2+ |
【实验结论】Cu(NO3)2能将Fe氧化为Fe2+。
Ⅱ.Cu(NO3)2的热稳定性
用下图所示的实验装置A加热Cu(NO3)2固体,产生红棕色气体,试管中残留物为黑色固体,b中收集到无色气体。

(2)仪器a的名称是 。装置B的作用是 。
(3)【提出设想】b中收集到的无色气体可能是:
i.氧气 ⅱ.一氧化氮 ⅲ.空气
【实验验证】该小组为验证上述设想,用玻璃片在水下盖住集气瓶口,并取出正放在桌面上,移开玻璃片后瓶口未发现颜色变化,将带火星的木条伸入集气瓶,未见复燃。
【实验结论】b中的气体是 。根据上述实验结果,该小组得出了Cu(NO3)2固体加热分解的产物。请你帮助写出Cu(NO3)2加热分解的化学方程式 ;
C中反应的离子方程式 。

的热稳定性,探究小组按下图装置进行实验。(图中铁架台、铁夹和加热仪器均略去)

在加热条件下可以分解,其化学反应方程式为 。
,写出检验
的方法 。







