-
肼是一种常见的还原剂,不同条件下分解产物不同,60~300℃时,在Cu等金属表面肼分解的机理如下图所示,已知200℃时:Ⅰ.3N2H4(g)= N2(g)+4NH3(g) ΔH1=-32.9kJ·mol-1;
Ⅱ.N2H4(g)+H2(g)= 2NH3(g) ΔH2=-41.8kJ·mol-1。
下列说法不正确的是

A. 肼属于共价化合物
B. 图示过程①、②都是吸热反应
C. 反应Ⅰ中氧化剂与还原剂的物质的量之比为2∶1
D. 200℃时,肼分解的热化学方程式为N2H4(g)= N2(g)+2H2(g) ΔH=+50.7kJ·mol-1
-
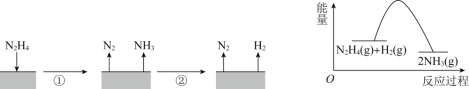
肼(N2H4)在不同条件下分解产物不同,200℃时在Cu表面分解的机理如图1。已知200℃时:反应 I : 3N2H4(g)=N2(g)+4NH3(g) ∆Hl=-32.9kJ·mol-1 , 反应II: N2H4(g)+H2(g)=2NH3(g)∆H2=-41.8 kJ·mol-1,下列说法不正确的是
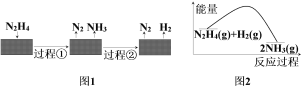
A. 图l所示过程①、②都是放热反应
B. 反应Ⅱ的能量过程示意图如图2所示
C. 断开3 molN2H4(g)中的化学键吸收的能量小于形成1 molN2(g)和4 molNH3(g)中的化学键释放的能量
D. 200℃时,肼分解生成氨气和氢气的热化学方程式为:N2H4(g) =N2(g)+2H2 (g) ∆H=+50.7kJ·mol-1
-
肼(N2H4)在不同条件下分解产物不同,200 ℃时在Cu表面分解的机理如图甲所示。已知200 ℃时:
反应Ⅰ:3N2H4(g)===N2(g)+4NH3(g) ΔH1=-32.9 kJ·mol-1
反应Ⅱ:N2H4(g)+H2(g)===2NH3(g) ΔH2=-41.8 kJ·mol-1
下列说法中不正确的是 ( )
A.图所示过程①、②都是放热反应
B.反应Ⅱ的能量过程示意图如图所示
C.断裂3 mol N2H4(g)中的化学键吸收的能量小于形成1 mol N2(g)和4 mol NH3(g)中的化学键释放的能量
D.200 ℃时,肼分解生成氮气和氢气的热化学方程式为N2H4(g)===N2(g)+2H2(g) ΔH=+50.7 kJ·mol-1
-
肼(N2H4)在不同条件下分解产物不同,200 ℃时在Cu表面分解的机理如图甲所示。已知200 ℃时:
反应Ⅰ:3N2H4(g)===N2(g)+4NH3(g) ΔH1=-32.9 kJ·mol-1
反应Ⅱ:N2H4(g)+H2(g)===2NH3(g) ΔH2=-41.8 kJ·mol-1
下列说法中不正确的是 ( )
A.图所示过程①、②都是放热反应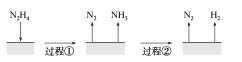
B.反应Ⅱ的能量过程示意图如图所示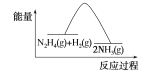
C.断裂3 mol N2H4(g)中的化学键吸收的能量小于形成1 mol N2(g)和4 mol NH3(g)中的化学键释放的能量
D.200 ℃时,肼分解生成氮气和氢气的热化学方程式为N2H4(g)===N2(g)+2H2(g) ΔH=+50.7 kJ·mol-1
-
肼(N2H4)在不同条件下分解产物不同,200℃时在Cu表面分解的机理如图1。已知200℃时:
反应 I : 3N2H4(g)=N2(g)+4NH3(g) △Hl=-32.9kJ/mol
反应II: N2H4(g)+H2(g)=2NH3(g) △H2=-41.8 kJ/mol
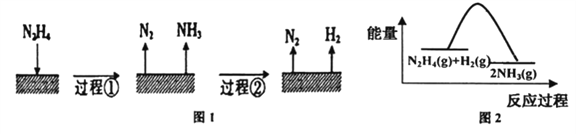
下列说法不正确的是
A. 图l所示过程①、②都是放热反应
B. 反应Ⅱ的能量过程示意图如图2所示
C. 断开3 molN2H4(g)中的化学键吸收的能量大于形成1 molN2(g)和4 molNH3(g)中的化学键释放的能量
D. 200℃时,肼分解生成氨气和氢气的热化学方程式为N2H4(g) =N2(g)+2H2 (g) △H=+50.7 kJ/mol
-
肼(N2H4)在不同条件下分解产物不同,200℃时在Cu表面分解的机理如图。已知200℃时:反应Ⅰ:3N2H4(g)=N2(g)+4NH3(g) ΔH1=-32.9 kJ·mol-1反应Ⅱ:N2H4(g)+H2(g)2NH3(g)ΔH2=-41.8 kJ·mol-1

下列说法不正确的是()
A. 图所示过程①是放热反应
B. 反应Ⅱ的能量过程示意图如图所示
C. 断开3 mol N2H4(g)的化学键吸收的能量大于形成1 molN2(g)和4 mol NH3(g)的化学键释放的能量
D. 200℃时,肼分解生成氮气和氢气的热化学方程式为N2H4(g)=N2(g)+2H2(g)ΔH=+50.7 kJ·mol-1
-
肼 在不同条件下分解产物不同,
在不同条件下分解产物不同, 时在Cu表面分解的机理如图。已知
时在Cu表面分解的机理如图。已知 时:
时:
反应Ⅰ:
 ;
;
反应Ⅱ:

总反应为
 .
.
下列说法不正确的是.
A.图示反应 是放热反应
是放热反应
B.
C. 的总能量大于
的总能量大于 和
和 的总能量
的总能量
D.
-
已知A为常见金属,常温下X、E、F为气体,C为液体.B是一种盐,受热易分解,冷却时分解产物又能化合生成B,B在工农业生产中有着广泛的用途.有关物质之间的转化关系如图(其中有些反应的条件及部分生成物被略去):
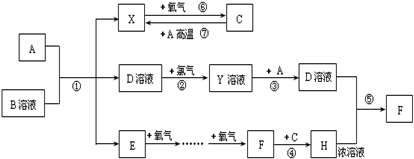
请回答下列问题:
(1)写出物质B的电子式______;
(2)比较①~⑦七个反应,请归纳它们的共同特点是______;
(3)写出反应⑦的化学方程式______ Fe3O4+4H2↑
-
已知A、B、C、D、E均为中学化学中常见物质,在一定条件下相互转化关系如下图所示(反应条件和部分产物已省略)。已知:

①A常温下为黄绿色的气体单质。
②B为一种常见变价金属单质,在冷的浓硫酸中会被钝化。
③C的水溶液是一种无氧酸,且C的组成中含有与A相同的元素。
请回答下列问题:
(1)A的化学式为 ,构成非金属单质A的元素的最高价氧化物的分子式为 ,C的名称为 。
(2)A与水反应的化学方程式为 。
(3)A与E反应生成D的离子方程式为 。
(4)在E的水溶液中加入足量氢氧化钠溶液,观察到的现象为 。
-
已知硝酸与金属反应时,在不同条件下有不同的还原产物,甚至在同一反应中可同时得到多种还原产物。现有HNO3、NH4NO3、N2O、H2O、Zn、Zn(NO3)2六种物质,
(1) 请利用其中五种物质组成一个完整的化学反应,写出该化学反应方程式:
________;
(2)上述所写反应中,硝酸表现出的化学性质是,被还原的元素是________。
(3)若六种物质组成一个完整的化学反应,则反应中的还原产物是________(填化学式),若该反应中NH4NO3与N2O物质的量之比为1︰1,那么该反应中氧化剂与还原剂的物质的量之比为________。
(4)若六种物质组成一个完整的化学反应,且没有对该反应中的某些物质的比例作限定,则方程式可能的配平系数有许多组。原因是________ 。









