-
工业上用洗净的废铜屑作原料制备硝酸铜。为节约原料和防止污染,宜采取的方法是
A. Cu+HNO3(浓)→Cu(NO3)2 B. Cu+HNO3(稀)→Cu(NO3)2
C. Cu→CuO→Cu(NO3)2 D. Cu→CuSO4→Cu(NO3)2
高三化学单选题中等难度题查看答案及解析
-
工业上用洗净的废铜屑作原料来制备硝酸铜。为了节约原料和防止污染环境,宜采取的方法是( )
A.Cu+HNO3(浓)
Cu(NO3)2
B.Cu
CuO
Cu(NO3)2
C.Cu+HNO3(稀)
Cu(NO3)2
D.Cu
CuSO4
Cu(NO3)2
高三化学选择题中等难度题查看答案及解析
-
工业上用洗净的废铜屑作原料制取硝酸铜。为节约原料和防止环境污染,宜采取的方法是( )
A. Cu+HNO3(浓)―→Cu(NO3)2
B. Cu+HNO3(稀)―→Cu(NO3)2
高三化学选择题简单题查看答案及解析
-
工业上用洗净的废铜作原料来制备硝酸铜.为了节约原料和防止污染环境,宜采取的方法是( )
A.Cu
CuSO4
Cu(NO3)2
B.Cu
CuO
Cu(NO3)2
C.Cu
Cu(NO3)2
D.Cu
Cu(NO3)2
高三化学单选题中等难度题查看答案及解析
-
工业上用洗净的废铜屑作原料来制备硝酸铜,为节约原料和防止环境污染,宜采用的方法是
A.
稀
B.
浓
C.Cu
CuSO4
Cu(NO3)2 D.Cu
CuO
Cu(NO3)2
高三化学单选题中等难度题查看答案及解析
-
从节约原料和防止环境污染因素考虑,用铜制取硝酸铜,方法最佳的是( )
A.CuCu(NO3)2
B.CuCu(NO3)2
C.CuCuCl2
Cu(NO3)2
D.CuCuO
Cu(NO3)2
高三化学选择题中等难度题查看答案及解析
-
使用单质铜制硝酸铜,耗用原料最经济,而且对环境几乎没有污染的是( )
A. Cu+HNO3(稀) B. Cu
CuO
Cu(NO3)2
C. Cu+HNO3(浓) D. Cu
CuCl2
Cu(NO3)2
高三化学选择题简单题查看答案及解析
-
制备相同质量的硝酸铜,从经济效益和环保角度考虑,最适宜采用的方法是
A.Cu+HNO3(浓)→Cu(NO3)2
B.Cu+HNO3(稀)→Cu(NO3)2
C.Cu+AgNO3→Cu(NO3)2
D.
高三化学单选题中等难度题查看答案及解析
-
(15分)某化学探究小组拟用废铜屑制取Cu(NO3)2:,并探究其化学性质。
I.如图,用浓HNO3,和过量的废铜屑充分反应制硝酸铜溶液。
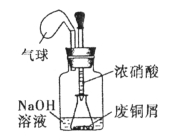
(1)写出铜与浓硝酸反应的离子方程式 。
(2)①装置中NaOH溶液的作用是 。
②欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤是蒸发浓缩、 、过滤。
③你认为此装置是否合理,并说明原因 。
如果不合理,同时在原装置上改进;如果合理,只需说明原因。
Ⅱ.为了探究
的热稳定性,探究小组按下图装置进行实验。(图中铁架台、铁夹和加热仪器均略去)
【实验装置】
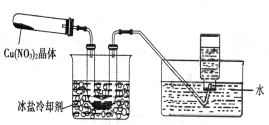
【实验操作及现象】往试管中放人研细的无水Cu(NO3)2:晶体并加热,观察到试管中有红棕色气体生成,最终残留黑色粉末;用U型管除去红棕色气体,在集气瓶中收集到无色气体。
【解释与结论】
(3)①红棕色气体是 。
②根据现象判断
在加热条件下可以分解,其化学反应方程式为 。
Ⅲ.利用Cu(NO3)2制备浅绿色的碱式碳酸铜[CuCO3·Cu(OH)2]。
向大试管中加入一定量的碳酸钠溶液和硝酸铜溶液,水浴加热,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡、静置、过滤、洗涤、干燥,得到样品。
【实验数据】反应温度对样品的影响
实验序号
1
2
3
4
温度/℃
35
50
70
95
样品颜色
深蓝色
深蓝色
浅绿色
暗蓝色
样品中碱式碳酸铜
的质量分数/%
90.9
92.7
x
92.0
(4)滤液中可能含有
,写出检验
的方法 。
(5)95℃时,样品颜色发暗的原因:____ 。
(6)70C时,实验得到2.38 g样品,取此样品加热至分解完全(杂质不分解),得到1.76 g固体,此样品中碱式碳酸铜的质量分数是 。
高三化学实验题极难题查看答案及解析
-
某化学探究小组拟用废铜屑制取Cu(NO3)2并探究其化学性质。
I、如右图所示,用浓HNO3和过量的废铜屑充分反应制硝酸铜溶液。
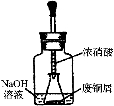
(1)写出铜与浓硝酸反应的离子方程式 。
(2)①装置中NaOH溶液的作用是 。
②欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤依次是:蒸发浓缩、 、过滤、 、烘干。
③你认为此装置是否合理,并说明原因 。
Ⅱ、为了探究Cu(NO3)2热稳定性,探究小组按下图装置进行实验。(图中铁架台、铁夹和加热仪器均略去)
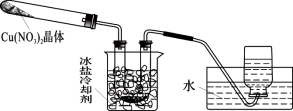
(3)往试管中放入研细的无水Cu(NO3)2晶体并加热,观察到试管中有红棕色气体生成,最终残留黑色粉末;在集气瓶中收集到无色气体。由此判断Cu(NO3)2受热分解的化学方程式为 。
Ⅲ、利用Cu(NO3)2制备浅绿色的碱式碳酸铜[CuCO3·Cu(OH)2]。
向大试管中加入一定量的碳酸钠溶液和硝酸铜溶液,水浴加热,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡、静置、过滤、洗涤、干燥,得到样品。下表是化学探究小组的实验记录,据此回答相关问题:
实验序号
1
2
3
4
温度/℃
35
50
70
95
样品颜色
深蓝色
深蓝色
浅绿色
暗蓝色
(4)95℃时,制得的样品颜色发暗的可能原因是: 。
(5)70℃时,实验得到3.82 g样品,取此样品加热至分解完全(杂质不反应),得到3.20 g固体,此样品中碱式碳酸铜的质量分数是 。
高三化学实验题困难题查看答案及解析