(1)写出该反应的离子方程式______ Mn2++Cl2↑+2H2O
高三化学解答题中等难度题
高三化学解答题中等难度题
高三化学解答题中等难度题查看答案及解析
(1)实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。请回答下列问题:
①写出该反应的离子反应方程式________________,
②反应中被氧化的HCl的物质的量为________mol。
③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________ molL-1。
(2)把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入1 molL-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
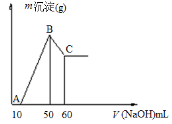
①合金中镁的质量g。
②盐酸的物质的量浓度molL-1
高三化学填空题中等难度题查看答案及解析
高三化学解答题中等难度题查看答案及解析
(6分)实验室常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。
(1)写出该反应的离子方程式___________________________________________。
(2)在反应中MnO2发生________(填“氧化”或“还原”)反应,Cl2是________(同上)产物。
(3)当0.1 mol MnO2参加反应时,转移电子数为________,被氧化的HCl为________ mol。
高三化学填空题简单题查看答案及解析
氯气在生产生活中应用广泛。实验室可用MnO2与浓盐酸反应制取,反应原理如下:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
(1)若制得标准状况下11.2 L Cl2,则被氧化的HCl为___________mol。
(2)多余的氯气可用NaOH溶液吸收,反应的离子方程式为__________。
(3)海底蕴藏着丰富的锰结核矿,其主要成分是MnO2。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的MnO2,其制备过程如下图所示:
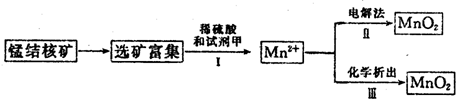
①步骤Ⅰ中, 试剂甲必须具有的性质是____________(填序号)。
A.氧化性B.还原性C.酸性
②步骤Ⅲ中,以NaClO3为氧化剂,当生成0.050 mol MnO2时,消耗0.10 mol·L-1的NaClO3溶液200 mL,该反应的离子方程式为___________________________。
(4)用100mL12.0 mol·L-1的浓盐酸与足量MnO2混合后,加热,反应产生的氯气物质的量远远少于0.30 mol,请你分析可能的原因为___________________________。
高三化学填空题困难题查看答案及解析
已知实验室在加热条件下制取Cl2的化学方程式为MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O。现将8.7 g MnO2投入到200 g质量分数为36.5%(过量)的浓盐酸中加热,充分反应后,求:
(1)标准状况下生成Cl2的体积为 。
(2)反应的HCl的分子数为 。
(3)向反应后的溶液中加入足量的AgNO3溶液,可生成白色沉淀的质量为 。
高三化学填空题中等难度题查看答案及解析
某小组在实验室使用软锰矿(主要成分为MnO2)和浓盐酸通过加热制备制备氯气,化学方程式为:MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O。并对氯气的性质进行探究。
(1)氯气制备:
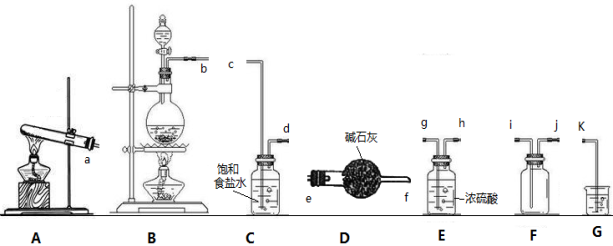
①欲收集一瓶干燥的氯气,请按接口序号完成“制取→收集”的连接顺序为:
→ c → d → → → i → j → k
②制备氯气也可用高锰酸钾固体和浓盐酸在常温下制得,其化学方程式为:
□KMnO4 + □HCl(浓) → □MnCl2 + □Cl2↑ + □KCl + □
请配平上述化学方程式。
③请写出仪器G中可能反应的离子方程式为
(2)性质检验:将氯气溶于水后,进行实验检测。所用试剂有:0.01mol/LAgNO3溶液、紫色石蕊试液。
| 操作步骤 | 实验现象 | 解释原因 |
| ① | 滴加 ,现象有: | 原因有: |
| ② | 滴加 ,现象有: | 原因有: |
高三化学实验题困难题查看答案及解析
高三化学解答题中等难度题查看答案及解析
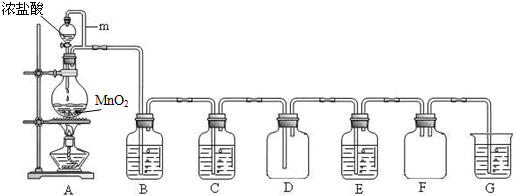
Ⅰ、实验室常用MnO2与浓盐酸反应制备Cl2(MnO2+4HCl(浓)→MnCl2+Cl2↑+2H2O反应装置如图所示)。
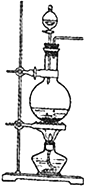
(1)装置图中的主要玻璃仪器有酒精灯、________、__________等。产生的氯气通入水中制得氯水备用。氯水含有的离子除H+、Cl-外还有___________等离子,氯水中因含有__________而具有漂白性。
Ⅱ、某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:

请根据上面流程,回答以下问题:
(2)样品溶解时加盐酸的作用是___________________________________。加入氯水所发生反应的离子方程式___________________________________。
(3)证明Fe3+离子已经沉淀完全的操作是___________________________________。将沉淀物加热灼烧过程中,为使实验结果准确,必须的操作为___________________。
(4)若原样品质量a 为40.00g,加热后红棕色固体质量b为2.200g,则样品中铁元素的质量分数是_________;若称量准确,最终测量的结果偏大,则造成误差的原因可能是_____________(写出一种原因即可)。
高三化学实验题困难题查看答案及解析
高三化学解答题中等难度题查看答案及解析