-
弱电解质在水溶液中存在多种平衡,它们在工农业生产中都有广泛的应用。已知如表数据,请回答下列问题:
化学式
温度(℃)
平衡常数
HClO
25
K=3.0×10-8
H2CO3
25
Ka1=4.5×10-7
Ka2=4.7×10-11
H2O
25
Kw=10-14
(1)向NaClO溶液中通入少量CO2,所发生的离子方程式为________;
(2)等pH的NaClO、NaHCO3与Na2CO3溶液,则物质的量浓度最大的是________;
(3)向0.1mol/L的HClO溶液中滴加NaOH溶液至3c(HClO)=c(ClO-),此时混合溶液的pH=____;
(4)已知:NaA+CO2(少量)+H2O=HA+NaHCO3,NaB+CO2(少量)+H2O=HB+Na2CO3,则HA酸性___HB的酸性(填“强于”“弱于”“无法确定”)。
高三化学填空题中等难度题查看答案及解析
-
碳及其化合物在科技、社会生产、生活中有着广泛的应用.请按要求回答下列问题:
(1)已知:
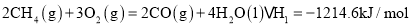
请写出
燃烧热的热化学方程式: ______ .
(2)在不同温度下反应
的平衡常数K如下表:
温度
600
750
900
1100
1250
平衡常数K
1
①该反应的
______
填“
”、“
”或“
”
.
②900℃时发生上述反应,
的转化率随时间变化如图所示,若到达平衡后加压,则
的转化率将
填“增大”、“减小”或“不变”,下同
______,正反应速率将 ______. 其他条件相同时,请在图中画出
时
的转化率随时间变化的示意图______.
③在
时发生上述反应,以下表中的物质的量投入恒容反应器,其中向正方向移动的组是
填编号
______ ,平衡后与C中各物质的百分含量相等的组有 ______
填编号
A
B
C
D
E
3
1
0
1
1
2
1
0
1
2
1
2
3
3
5
2
3
1
(3)以二甲醚
、空气、KOH溶液为原料可设计为燃料电池放电时,负极电极反应式: _______ .
①假设该燃料电池中盛有
KOH溶液,放电时参与反应的氧气在.
②标准状况下的体积为
,放电过程中没有气体逸出,则放电完毕后,所得溶液中各离子浓度由大到小的关系为 ______ .
高三化学综合题中等难度题查看答案及解析
-
硼元素、钙元素、铜元素在化学中站有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用.
(1)已知CaC2与水反应生成乙炔。请回答下列问题:
①将乙炔通入[Cu(NH3)2]Cl溶液中生成Cu2C2红棕色沉淀,Cu+基态核外电子排布式为 ______。
② CaC2中C22-与O22+互为等电子体,1mol O22+中含有的
键数目为 ______。
③乙炔与氢氰酸反应可得丙烯睛(H2C=CH-C≡N),丙烯腈分子中碳原子轨道杂化类型是 ______,构成丙烯腈元素中第一电离能最大的是 ______。
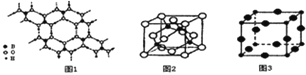
(2)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子间通过氢健相连(如上图1)则1molH3BO3的晶体中有 ______ mol氢键。硼酸溶于水生成弱电解质一水合硼酸B(OH)3•H2O,它电离生成少量[B(OH)4]-和H+,则[B(OH)4]-的空间构型为 ______。
(3)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如上图2所示(黑点代表铜原子,空心圆代表M原子)。
该晶体化学式为 ______。
已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于 ______ (填“离子”、“共价”)化合物。
(4)Cu3N的晶胞结构如上图3,N3-的配位数为 ______ ,Cu+半径为apm,N3-半径为bpm,Cu3N的密度为 ______g•cm-3(阿伏加德罗常数用NA表示)。
高三化学综合题中等难度题查看答案及解析
-
硼元素、钙元素、铜元素在化学中有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用。
已知
与水反应生成乙炔。请回答下列问题:
将乙炔通入
溶液中生成
红棕色沉淀,
基态核外电子排布式为 ______ ,其在酸性溶液中不稳定,可发生歧化反应生成
和Cu,但CuO在高温下会分解成
,试从结构角度解释高温下CuO何会生成
:______。
中
与
互为等电子体,
中含有的
键数目为 ______ 。
乙炔与氢氰酸反应可得丙烯腈
丙烯腈分子中碳原子轨道杂化类型是 ______ ,构成丙烯腈元素中第一电离能最大的是 ______ 。
硼酸
是一种片层状结构的白色晶体,层内的
分子间通过氢键相连
如图
则
的晶体中有 ______ mol氢键。硼酸溶于水生成弱电解质一水合硼酸
,它电离生成少量
和
,则
含有的化学键类型为 ______ 。

高三化学填空题中等难度题查看答案及解析
-
磷单质及其化合物在工农业生产中有着广泛的应用。
(1)温度为T℃时,向2.0L恒容密闭容器中充入
,发生反应
,经过一段时间后达测平衡,反应过程中测定的部分数据如图。反应在前50s的平均速率
___________。反应达到平衡后,升高温度,则v逆
________
填“增大”“减小”或“不变”
,再次达到平衡后,
的平衡浓度为
,则反应
_______
填“
”“
”或“
”
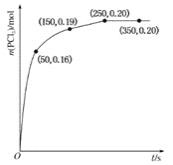
(2)温度为T℃时,若平衡时体系的总压强为p,该反应的平衡常数
________。
用平衡分压代替平衡浓度计算,分压
总压
物质的量分数
(3)温度为T℃时,上述反应若在恒压容器中进行,则达到平衡后,
的物质的量_________
填“大于”“小于”或“等于”
。
(4)已知
水解可生成亚磷酸
。常温下,
的
溶液的
,亚磷酸与足量的NaOH溶液反应生成
。则
的
溶液中各离子浓度由大到小的顺序是________。
(5)亚磷酸具有强还原性,可被氧化为
。
与NaOH溶液反应,反应混合物中含磷各微粒的分布分数
平衡时某微粒的浓度占微粒浓度之和的分数
与pH的关系如图所示。
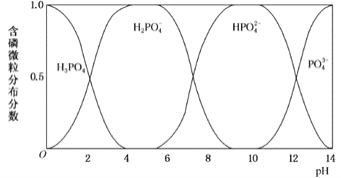
①为获得尽可能纯的
,pH应控制在___________。
②已知:25℃时,
,
,
,则
时,溶液中
___________。
高三化学综合题困难题查看答案及解析
-
硼、镁及其化合物在工农业生产中应用广泛.已知:硼镁矿主要成分为
,硼砂的化学式为
利用硼镁矿制取金属镁及粗硼的工艺流程如下.

回答下列有关问题.
(1)硼砂中B的化合价为 ______,溶于热水后,常用
调pH到
制取
,反应的离子方程式为 ______,X为
晶体加热脱水的产物,其与Mg反应制取粗硼的化学方程式为 ______,该反应中的氧化剂是 ______ (填化学式)。
(2)硼酸是一种一元弱酸,它与水作用时结合水电离的
而释放出水电离的H+,这一变化的化学方程式为 ______,皮肤上不小心碰到氢氧化钠溶液,一般先用大量水冲洗,然后再涂上硼酸溶液,则硼酸与氢氧化钠反应的离子方程式为 ______。
(3)
需要在HCl氛围中加热制
,其目的是 ______ .
(4)制得的粗硼在一定条件下生成
,
加热分解可以得到纯净的单质硼.现将
粗硼制成的
完全分解,生成的
用
为弱酸
溶液滴定至终点,消耗
溶液
盛装
溶液的仪器应为 ______
填“酸式”或“碱式”
滴定管.该粗硼样品的纯度为 ______ (提示:
)
高三化学工业流程中等难度题查看答案及解析
-
铁及其化合物在生产、生活中有广泛应用,请回答下列问题:
(一)高炉炼铁过程中发生的主要反应为:
Fe2O3(s)+CO(g)
Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数 如下:
温度/℃ 1000 1115 1300
平衡常数 4.0 3.7 3.5
(1)该反应的平衡常数表达式K= ;△H 0(填“>”、“<”或“=”).
(2)欲提高上述反应中CO的平衡转化率,可采取的措施是 .
A.提高反应温度 B.移出部分CO2
C.加入合适的催化剂 D.减小容器的容积
(3)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时υ正 υ逆(填“>”、“<”或“=”).经过10min,在1000℃达到平衡,则该时间范围内反应的平均反应速率υ(CO2)= .
(二)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.
(4)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,其中反应的氧化剂是 ;生成0.5mol K2FeO4转移电子的物质的量是 mol.
(5)从环境保护的角度看,制备K2FeO4较好的方法为电解法,其装置如图所示.电解过程中阳极的电极反应式为 .
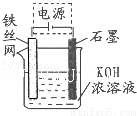
高三化学填空题困难题查看答案及解析
-
铁及其化合物在生产、生活中有广泛应用.请回答下列问题:
(一)高炉炼铁过程中发生的主要反应为:
Fe2O3(s)+CO(g)
Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数 如下:
温度/℃ 1000 1115 1300
平衡常数 4.0 3.7 3.5
(1)该反应的平衡常数表达式K=___;△H___0(填“>”、“<”或“=”).
(2)欲提高上述反应中CO的平衡转化率,可采取的措施是_____.
A.提高反应温度 B.移出部分CO2
C.加入合适的催化剂 D.减小容器的容积
(3)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时υ正___υ逆(填“>”、“<”或“=”).经过10min,在1000℃达到平衡,则该时间范围内反应的平均反应速率υ(CO2)=_____.
(二)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.
(4)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,其中反应的氧化剂是_____;生成1mol K2FeO4转移电子的物质的量是_____mol.
高三化学填空题简单题查看答案及解析
-
硼、镁及其化合物在工农业生产中应用广泛。已知:硼镁矿主要成分为Mg2B2O5·H2O, 硼砂的化学式为Na2B4O7·10H2O。利用硼镁矿制取金属镁及粗硼的工艺流程如下:
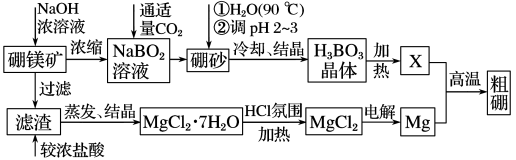
回答下列有关问题:
(1)硼砂中B的化合价为__________,溶于热水后,常用H2SO4调pH到2~3制取H3BO3,反应的离子方程式为__________________。
(2)氧化物X为H3BO3晶体加热脱水的
产物,其与Mg反应制取粗硼的化学方程式为______________,该反应中的氧化剂是(填化学式)_______________。
(3)硼酸是一种一元弱酸,它与水作用时结合水电离的OH-而释放出水电离的H+,这一变化的化学方程式为____________________。皮肤上不小心碰到氢氧化钠溶液,一般先用大量水冲洗,然后再涂上硼酸溶液,则硼酸与氢氧化钠反应的离子方程式为 。
(4)MgCl2·7H2O需要在HCl氛围中加热制MgCl2,其目的是 。
高三化学实验题中等难度题查看答案及解析
-
硼、镁及其化合物在工农业生产中应用广泛。
已知:硼镁矿主要成分为Mg2B2O5•H2O,硼砂的化学式为Na2B4O7•10H2O。利用硼镁矿制取金属镁及粗硼的工艺流程为:
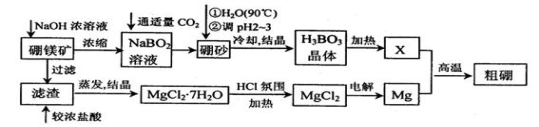
回答下列有关问题:
(1)硼砂溶于热水后,常用H2SO4调pH2~3制取H3BO3,反应的离子方程式为 。X为H3BO3晶体加热脱水的产物,其与Mg制取粗硼的化学方程式为 。
(2)MgCl2·7H2O需要在HCl氛围中加热,其目的是 。若用惰性电极电解MgCl2溶液,其阴极反应式为 。
(3)镁-H2O2酸性燃料电池的反应机理为Mg+H2O2+2H+==Mg2++2H2O,则正极反应式为 。若起始电解质溶液pH=1,则pH=2时溶液中Mg2+离子浓度为 。已知Ksp[Mg(OH)2]=5.6
10-12,当溶液pH=6时 (填“有”或“没有”)Mg(OH)2沉淀析出。
(4)制得的粗硼在一定条件下生成BI3,BI3加热分解可以得到纯净的单质硼。现将 0.020g粗硼制成的BI3完全分解,生成的I2用0.30mol·L-1 Na2S2O3(H2S2O3为弱酸)溶液滴定至终点,消耗Na2S2O3溶液18.00mL。盛装Na2S2O3溶液的仪器应为 滴定管(填“酸式”或“碱式”)。该粗硼样品的纯度为 。(提示:I2+2S2O32-=2I-+S4O62-)
高三化学填空题极难题查看答案及解析