-
磷单质及其化合物在工农业生产中有着广泛的应用。
(1)温度为T℃时,向2.0L恒容密闭容器中充入 ,发生反应
,发生反应 ,经过一段时间后达测平衡,反应过程中测定的部分数据如图。反应在前50s的平均速率
,经过一段时间后达测平衡,反应过程中测定的部分数据如图。反应在前50s的平均速率 ___________。反应达到平衡后,升高温度,则v逆
___________。反应达到平衡后,升高温度,则v逆 ________
________ 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” ,再次达到平衡后,
,再次达到平衡后, 的平衡浓度为
的平衡浓度为 ,则反应
,则反应 _______
_______ 填“
填“ ”“
”“ ”或“
”或“ ”
”
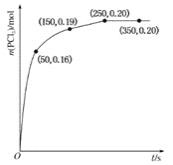
(2)温度为T℃时,若平衡时体系的总压强为p,该反应的平衡常数 ________。
________。 用平衡分压代替平衡浓度计算,分压
用平衡分压代替平衡浓度计算,分压 总压
总压 物质的量分数
物质的量分数
(3)温度为T℃时,上述反应若在恒压容器中进行,则达到平衡后, 的物质的量_________
的物质的量_________ 填“大于”“小于”或“等于”
填“大于”“小于”或“等于” 。
。
(4)已知 水解可生成亚磷酸
水解可生成亚磷酸 。常温下,
。常温下, 的
的 溶液的
溶液的 ,亚磷酸与足量的NaOH溶液反应生成
,亚磷酸与足量的NaOH溶液反应生成 。则
。则 的
的 溶液中各离子浓度由大到小的顺序是________。
溶液中各离子浓度由大到小的顺序是________。
(5)亚磷酸具有强还原性,可被氧化为 。
。 与NaOH溶液反应,反应混合物中含磷各微粒的分布分数
与NaOH溶液反应,反应混合物中含磷各微粒的分布分数 平衡时某微粒的浓度占微粒浓度之和的分数
平衡时某微粒的浓度占微粒浓度之和的分数 与pH的关系如图所示。
与pH的关系如图所示。
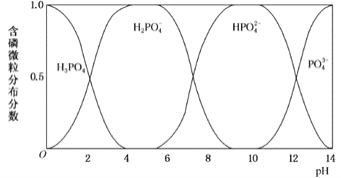
①为获得尽可能纯的 ,pH应控制在___________。
,pH应控制在___________。
②已知:25℃时, ,
, ,
, ,则
,则 时,溶液中
时,溶液中 ___________。
___________。
-
磷单质及其化合物有着广泛应用。
(1)在1.0 L密闭容器中放入0.10mol PCl5(g),一定温度进行如下反应:PCl5(g) PCl3(g)+Cl2(g) ΔH1
PCl3(g)+Cl2(g) ΔH1
反应时间(t)与容器内气体总压强(p/100kPa)的数据见下表:
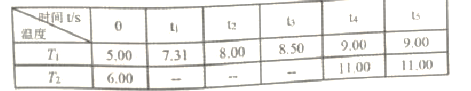
回答下列问题:
①PCl3的电子式为_______。
②T1温度下,反应平衡常数K=______。
③T1___T2(填“>”、“<”或“=”,下同),PCl5的平衡转化率α1(T1) __α2(T2)。
(2)PCl5、PCl3可转化为H3PO4、H3PO3。已知下列热化学方程式:
PCl5(g)+4H2O(l) = H3PO4(aq)+5HCl(aq) ΔH2
PCl3(g)+3H2O(l) = H3PO3(aq)+3HCl(aq) ΔH3
H3PO3(aq)+Cl2(g)+H2O(l) = H3PO4(aq)+2HCl(aq) ΔH4
则ΔH4= ______。(用ΔH1、ΔH2、ΔH3表示)
(3)次磷酸钴[Co(H2PO2)2]广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如下图。
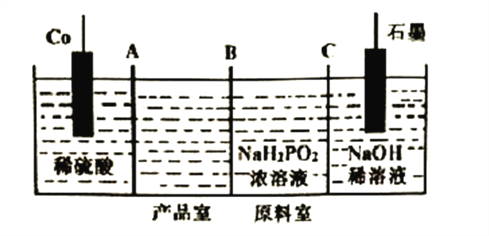
①Co的电极反应式为______________,A、B、C为离子交换膜,其中B为__________离子交换膜(填“阳”或“阴”)。
②次磷酸(H3PO2)为一元弱酸,次磷酸钠溶液中离子浓度由大到小的顺序是__________。
-
(Ⅰ)氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用。
(1)一定温度下,在1L容积恒定的密闭容器中充入2mol N2和8mol H2并发生反应。10min达平衡,测得氨气的浓度为0.4mol/L,此时氮气的转化率为________。
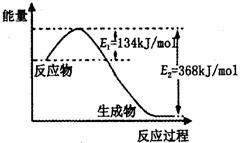
(2)下图是1mol NO2(g)和1mol CO(g)反应生成1mol CO2(g)和1mol NO(g)过程中能量变化示意图,请写出该反应的热化学方程式________。
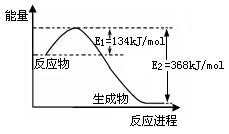
(3)NH3(g)燃烧的方程式4NH3(g)+7O2(g)==4NO2(g)+6H2O(l),
已知:2H2(g)+O2(g)==2H2O(l) △H= -483.6 kJ/mol
N2(g)+2O2(g)==2NO2 (g) △H=+67.8 kJ/mol
N2(g)+3H2(g)==2NH3 (g) △H=-92.0 kJ/mol
请计算NH3 (g)的燃烧热 。
| 温度 | 平衡浓度/ (mol L-1) |
| c(NH3) | c(CO2) |
| T1 | 0.1 | |
| T2 | | 0.1 |
(4)将一定量的氨基甲酸铵固体置于某容积恒定的真空容器中,发生反应:
H2NCOONH4(s) 2NH3(g)+CO2(g) 在不同温度下,该反应平衡状态部分数据见右表。下列说法正确的是
2NH3(g)+CO2(g) 在不同温度下,该反应平衡状态部分数据见右表。下列说法正确的是
A.若T2>T1,则该反应的ΔH<0
B.向容器中充入N2,H2NCOONH4质量增加
C.NH3体积分数不变时,说明该反应达到平衡
D.T1、T2时,H2NCOONH4转化的Δn(T2)=2Δn(T1)
(Ⅱ)海水资源的利用具有广阔前景。海水中主要离子的含量如下:
| 成分 | 含量/(mg L-1) | 成分 | 含量/(mg L-1) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Br- | 64 |
| Mg2+ | 1272 | | |
 电渗析法淡化海水示意图如下图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过。
电渗析法淡化海水示意图如下图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过。
(1)阳极主要电极反应式是________。
(2)在阴极附近产生少量白色沉淀,其成分有________和CaCO3,生成CaCO3的离子方程
式是________。

(3)淡水的出口为________(填“a”、“b”或“c”)。
-
氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用.
(1)一定温度下,在1L容积恒定的密闭容器中充入2mol N2和8mol H2并发生反应.10min达平衡,测得氨气的浓度为0.4mol/L,此时氮气的转化率为______.若想提高氨气的产率,根据化学平衡移动原理,提出合理的建议(写出一条即可)______.
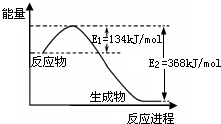
(2)如图是1mol NO2(g)和1mol CO(g)反应生成1mol CO2(g)和1mol NO(g)过程中能量变化示意图,请写出该反应的热化学方程式______.
(3)在容积恒定的密闭容器中,进行如下反应:
N2(g)+3H2(g)⇌2NH3(g)△H<0,其平衡常数K与温度T的关系如下表:
①该反应的平衡常数表达式:K=______;
②试判断K1______K2(填写“>”“=”或“<”);
③NH3(g)燃烧的方程式为4NH3(g)+7O2(g)═4NO2(g)+6H2O(l),已知:
2H2(g)+O2(g)═2H2O(l)△H=-483.6kJ/mol
N2(g)+2O2(g)═2NO2(g)△H=+67.8kJ/mol
N2(g)+3H2(g)═2NH3(g)△H=-92.0kJ/mol
请计算NH3(g)的燃烧热______.
-
氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用。
(1)一定温度下,在1L容积恒定的密闭容器中充入2 mol N2和8molH2并发生反应。10min达平衡,测得氨气的浓度为0.4 mol·L-1,此时氮气的转化率为________。若想提高氨气的产率,根据化学平衡移动原理,提出合理的建议______________(写出一条即可)。
(2)如图是1mol NO2(g)和1mol CO(g)反应生成lmol CO2(g)和1 mol NO(g)过程中能量变化示意图,请写出该反应的热化学方程式_____________________。
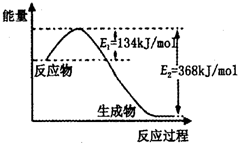
(3)在容积恒定的密闭容器中,进行如下反应:N2(g)+3H2(g) 2NH3(g)△H<0,其平衡常数K与温度T的关系如下表:
2NH3(g)△H<0,其平衡常数K与温度T的关系如下表:
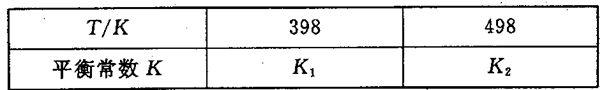
①该反应的平衡常数表达式:K=_____________;
②试判断K1__________K2(填写“>”“=”或“<”);
③NH3(g)燃烧的方程式为:4NH3(g)+7O2(g)=4NO2(g)+6H2O(l),已知:
①2H2(g)+O2(g) 2H2O(l) △H=-483.6 kJ/mol
2H2O(l) △H=-483.6 kJ/mol
②N2(g)+2O2(g) 2NO2(g) △H=+67.8 kJ/mol
2NO2(g) △H=+67.8 kJ/mol
③N2(g)+3H2(g) 2NH3(g) △H=-92.0 kJ/mol
2NH3(g) △H=-92.0 kJ/mol
请计算NH3(g)的燃烧热________kJ/mol。
-
氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用。
(1)一定温度下,在1L容积恒定的密闭容器中充入2 mol N2和8molH2并发生反应。10min达平衡,测得氨气的浓度为0.4 mol·L-1,此时氮气的转化率为________。若想提高氨气的产率,根据化学平衡移动原理,提出合理的建议______________(写出一条即可)。
(2)如图是1mol NO2(g)和1mol CO(g)反应生成lmol CO2(g)和1 mol NO(g)过程中能量变化示意图,请写出该反应的热化学方程式_____________________。
(3)在容积恒定的密闭容器中,进行如下反应:N2(g)+3H2(g) 2NH3(g) △H<0,其平衡常数K与温度T的关系如下表:
2NH3(g) △H<0,其平衡常数K与温度T的关系如下表:
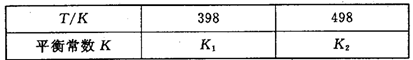
①该反应的平衡常数表达式:K=_____________;
②试判断K1__________K2(填写“>”“=”或“<”=;
③NH3(g)燃烧的方程式为:4NH3(g)+7O2(g)=4NO2(g)+6H2O(l),已知:
H2(g)+O2(g) 2H2O(l) △H=-483.6 kJ/mol
2H2O(l) △H=-483.6 kJ/mol
N2(g)+2O2(g) 2NO2(g) △H=+67.8 kJ/mol
2NO2(g) △H=+67.8 kJ/mol
N2(g)+3H2(g) 2NH3(g) △H=-92.0 kJ/mol
2NH3(g) △H=-92.0 kJ/mol
请计算NH3(g)的燃烧热________kJ/mol。
-
碳、氮、氧、铝都为重要的短周期元素,其单质及化合物在工农业生产生活中有着重要作用。请回答下列问题:
(1)在密闭容器内(反应过程保持体积不变),使1 mol N2和3 mol H2混合发生下列反应:N2(g)+3H2(g) 2NH3(g) ΔH=−92.4 kJ·mol−1。当反应达到平衡时,N2和H2的浓度之比是__________;当升高平衡体系的温度,则混合气体的平均式量________(填“增大”“减小”或“不变”);当达到平衡时,再向容器内充入1 mol N2,H2的转化率__________(填“提高”“降低”或“不变”);当达到平衡时,将c(N2)、c(H2)、c(NH3)同时增大1倍,平衡__________移动(填“正向”“逆向”或“不”)。
2NH3(g) ΔH=−92.4 kJ·mol−1。当反应达到平衡时,N2和H2的浓度之比是__________;当升高平衡体系的温度,则混合气体的平均式量________(填“增大”“减小”或“不变”);当达到平衡时,再向容器内充入1 mol N2,H2的转化率__________(填“提高”“降低”或“不变”);当达到平衡时,将c(N2)、c(H2)、c(NH3)同时增大1倍,平衡__________移动(填“正向”“逆向”或“不”)。
(2)由题干所述元素中的三种组成的某种强酸弱碱盐的化学式为__________,其溶于水能________水的电离(填“促进”或“抑制”),且使溶液的pH________(填“升高”“降低”或“不变”),原因是____________________________(用离子方程式表示)。
(3)空气是硝酸工业生产的重要原料,氨催化氧化是硝酸工业的基础,氨气在铁触媒作用下只发生主反应①和副反应②:
4NH3(g)+5O2 4NO(g)+6H2O(g) ΔH=−905 kJ·mol−1 ①
4NO(g)+6H2O(g) ΔH=−905 kJ·mol−1 ①
4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔH=−1268 kJ·mol−1 ②
2N2(g)+6H2O(g) ΔH=−1268 kJ·mol−1 ②
①氮气与氧气反应生成NO的热化学方程式为__________________________。
②在氧化炉中催化氧化时,有关物质的产率与温度的关系如图。下列说法中正确的是____________。

A.工业上氨催化氧化生成NO时,最佳温度应控制在780~840 ℃之间
B.工业上采用物料比 在1.7~2.0,主要是为了提高反应速率
在1.7~2.0,主要是为了提高反应速率
C.加压可提高NH3生成NO的转化率
D.由图可知,温度高于900 ℃时,生成N2的副反应增多,故NO产率降低
(4)M是重要的有机化工原料,其分子与H2O2含有相同的电子数,将1 mol M在氧气中完全燃烧,只生成1 mol CO2和2 mol H2O,则M的化学式为__________。某种燃料电池采用铂作为电极催化剂,以KOH溶液为电解质,以M为燃料,以空气为氧化剂。若该电池工作时消耗1 mol M,则电路中通过__________mol电子。
-
硫元素的化合物在生产、生活中有着广泛的应用。
(1)400℃,1.01× Pa下,容积为1.0L的密闭容器中充入0.5molSO2, (g)和0.3 molO2 (g),发生反应2SO2(g)+O2(g)
Pa下,容积为1.0L的密闭容器中充入0.5molSO2, (g)和0.3 molO2 (g),发生反应2SO2(g)+O2(g) 2SO3(g) △H=-198kJ/mol。反应中n(SO3)和n(O2)随时间变化的关系如右图所示
2SO3(g) △H=-198kJ/mol。反应中n(SO3)和n(O2)随时间变化的关系如右图所示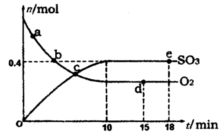 。反应的平衡常数K=_______;0到10 min内用SO2表示的平均反应速率_________。根据图中信息,判断下列叙述中正确的是_____(填序号)。
。反应的平衡常数K=_______;0到10 min内用SO2表示的平均反应速率_________。根据图中信息,判断下列叙述中正确的是_____(填序号)。
A.a点时刻的正反应速率比b点时刻的大
B.c点时刻反应达到平衡状态
C.d点和e点时刻的c(O2)相同
D.若5 00℃,1.01×105Pa下,反应达到平衡时,n( SO3) 比图中e点时刻的值大
(2)用NaOH溶液吸收工业废气中的SO2,当吸收液失去吸收能力时,25℃时测得溶液的pH=5.6,溶液中Na+,H+, HSO3-,SO32-离子的浓度由大到小的顺序是__________________。
(3)可通过电解法使(2)中的吸收液再生而循环利用(电极均为石墨电极),其工作示意图如下:
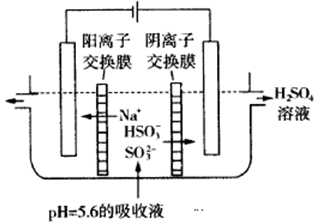
HSO3-在阳极室反应的电极反应式为________________________,阴极室的产物_________________。
-
氮及其化合物在工农业生产、生活中有着重要作用。
(1)在T℃时,将0.6molH2和0.4molN2置于容积为2 L的密闭容器中(压强为mPa)发生反应:3H2+N2 2NH3 △H<0。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强随时间变化如图所示:8 min内分钟NH3的平均生成速率为 mol·L-1·min-1。
2NH3 △H<0。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强随时间变化如图所示:8 min内分钟NH3的平均生成速率为 mol·L-1·min-1。
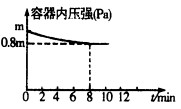
(2)仍在T℃时,将0.6molH2和0.4molN2置于一容积可变的密闭容 器中。
①下列各项能说明该反应已达到平衡状态的是 (填序号)。
a.容器内N2、H2、NH3的浓度之比为l:3:2
b.3v正(N2)=v逆(H2)
c.3v正(H2)=2v逆(NH3)
d.混合气体的密度保持不变
e.容器中气体的平均相对分子质量不随时间而变化
②该条件下达到平衡时NH3的体积分数与题(1)条件下NH3的体积分数相比 (填“变大”“变小”或“不变”)。
③达到平衡后,改变某一条件使反应速率发生了如图所示的变化,改 变的条件可能是 。
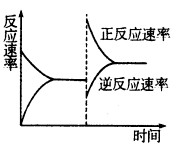
a.升高温度,同时加压
b.降低温度,同时减压
c.保持温度、压强不变,增大反应物浓度
d.保持温度、压强不变,减小生成物浓度
(3)硝酸厂的尾气含有氮氧化物,不经处理直接排放将污染空气。 氨气能将氮氧化物还原为氮气和水,其反应机理为:
2NH3(g)+5NO2(g)=7NO(g)+3H2O(g)  H=-akJ·mol-1
H=-akJ·mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(g)  H=-bkJ·mol-1
H=-bkJ·mol-1
则NH3直接将NO2还原为N2的热化学方程式为: 。
若标准状况下NO与NO2混合气体40.32L被足量氨水完全吸收,产生标准状况下氮气42.56L。该混合气体中NO与NO2的体积之比为 。
-
氮氧化物在含能材料、医药等方面有着广泛应用。请回答:
(1)一定温度下,在恒容密闭容器中 可发生下列反应:
可发生下列反应:

①该反应自发进行的条件是________。
②下表为反应在 温度下的部分实验数据:
温度下的部分实验数据:
在500s时, ________
________ 填“
填“ ”、“
”、“ ”或“
”或“ ”
” 。若在
。若在 温度下进行实验,1000s时测得反应体系中
温度下进行实验,1000s时测得反应体系中 浓度为
浓度为 ,则
,则 ________
________ 填“
填“ ”、“
”、“ ”或“
”或“ ”
” 。
。
(2)在 与
与 之间存在反应:
之间存在反应: 。将
。将 放入1L恒容密闭容器中,测得其平衡转化率
放入1L恒容密闭容器中,测得其平衡转化率 随温度变化如图所示。
随温度变化如图所示。
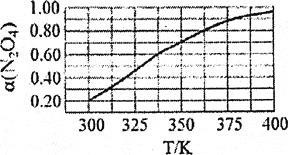
①337.5K时,反应平衡常数 ________。
________。
②已知:



则反应 的
的 ________
________ 。
。
(3)某学习小组设想利用A装置电解制备绿色硝化剂 ,装置如下
,装置如下 、d为惰性电极
、d为惰性电极 :
:
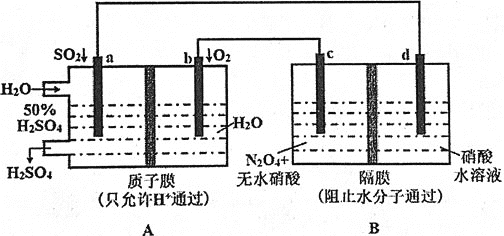
已知:无水硝酸可在液态 中发生微弱电离。写出生成
中发生微弱电离。写出生成 的电极反应式________。
的电极反应式________。
,发生反应
,经过一段时间后达测平衡,反应过程中测定的部分数据如图。反应在前50s的平均速率
___________。反应达到平衡后,升高温度,则v逆
________
填“增大”“减小”或“不变”
,再次达到平衡后,
的平衡浓度为
,则反应
_______
填“
”“
”或“
”

________。
用平衡分压代替平衡浓度计算,分压
总压
物质的量分数
的物质的量_________
填“大于”“小于”或“等于”
。
水解可生成亚磷酸
。常温下,
的
溶液的
,亚磷酸与足量的NaOH溶液反应生成
。则
的
溶液中各离子浓度由大到小的顺序是________。
。
与NaOH溶液反应,反应混合物中含磷各微粒的分布分数
平衡时某微粒的浓度占微粒浓度之和的分数
与pH的关系如图所示。

,pH应控制在___________。
,
,
,则
时,溶液中
___________。









 。反应的平衡常数K=_______;0到10 min内用SO2表示的平均反应速率_________。根据图中信息,判断下列叙述中正确的是_____(填序号)。
。反应的平衡常数K=_______;0到10 min内用SO2表示的平均反应速率_________。根据图中信息,判断下列叙述中正确的是_____(填序号)。



