-
中国首个空间实验室——“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),它是一种将水电解技术与氢氣燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,a、b、c、d均为Pt电极。 下列说法正确的是( )
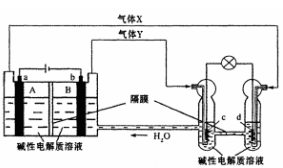
A. B区的OH-通过隔膜向a电极移动,A 区pH增大
B. 图中右管中的OH-通过隔膜向c电极移动,d电极上发生还原反应
C. c是正极,电极上的电极反应为2H++2e-=H2↑
D. 当有lmol电子转移时,b电极产生气体Y的体积为11.2L
高三化学选择题极难题查看答案及解析
-
部分弱电解质的电离平衡常数如下表:
弱电解质
HCOOH
HCN
H2CO3
NH3·H2O
电离平衡常数
(25℃)
Ka=1.8×10-4
Ka=4.9×10-10
Ka1=4.3×10-7 Ka2=5.6×10-11
Kb=1.8×10-5
下列说法不正确的是
A.结合H+的能力:CO32->CN->HCO3->HCOO-
B.0.1mol/L的HCOONH4溶液中:c(HCOO-)>c(NH4+)>c(H+)>c(OH-)
C.25 ℃时,pH=3的盐酸与pH=11的氨水混合,若溶液显中性,则二者消耗的体积是:V(盐酸)>V(氨水)
D.0.1mol/L的NaHCO3溶液中:c(Na+)+ c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
高三化学选择题极难题查看答案及解析
-
有机物X的蒸气相对氢气的密度为51,X中氧元素的质量分数为31.7%,则能在碱性溶液中
发生反应的X的同分异构体有(不考虑立体异构)( )
A. 15种 B. 14种 C. 13种 D. 12种
高三化学选择题极难题查看答案及解析
-
取一定质量的均匀固体混合物Cu、CuO和Cu2O,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少3.20 g,另一份中加入500 mL稀硝酸(其还原产物为NO),固体恰好完全溶解,且同时收集到标准状况下NO气体4.48 L,则所用硝酸的物质的量浓度为
A.2.4 mol/L B.1.4 mol/L C.1.2 mol/L D.0.7 mol/L
高三化学选择题极难题查看答案及解析
-
某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol·L-1的盐酸,测得溶液中的HCO3-、CO32-、AlO2-、Al3+离子的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是
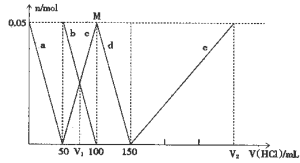
A.原混合溶液中的CO32-与AlO2-的物质的量之比为1:2
B.V1:V2=l:5
C.M点时生成的CO2为0.05mol
D.e曲线表示的离子方程式为: Al(OH)3+3H+= Al3++3H2O
高三化学选择题极难题查看答案及解析
-
某溶液中含如下离子组中的几种K+、Fe3+、Fe2+、Cl-、CO32-、NO3-、SO42-、SiO32-、I-,某同学欲探究该溶液的组成进行了如下实验:
Ⅰ.用铂丝醮取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成
Ⅲ.取Ⅱ反应后溶液分别置于两支试管中,第一支试管中加入BaCl2溶液有白色沉淀生成,再滴加KSCN溶液,上层清液变红,第二支试管加入CCl4,充分振荡静置后溶液分层,下层为无色。
下列说法正确的是
A.原溶液中肯定不含Fe2+、NO3-、SiO32-、I-
B.原溶液中肯定含有K+、Fe3+、Fe2+、NO3-、SO42-
C.步骤Ⅱ中无色气体是NO气体,无CO2气体产生
D.为确定是否含有Cl-可取原溶液加入过量硝酸银溶液,观察是否产生白色沉淀
高三化学选择题极难题查看答案及解析
-
F2和Xe在一定条件下生成氧化性极强且极易与水反应的XeF2、XeF4和XeF6三种化合物。其中XeF4与H2O可以发生如下反应:6 XeF4+12H2O=2XeO3+4Xe↑+24HF+3O2↑。下列判断正确的是
A. 上述反应中氧化剂和还原剂的物质的量之比为l:2
B. XeF4按以上方式与水反应,每生成3molO2转移12mol电子
C. XeF2加入水中,在水分子的作用下,将重新生成Xe和F2
D. XeF2、XeF4和XeF6在空气中都能长期存放
高三化学选择题极难题查看答案及解析
-
常温下,向1L0.1mol/LH2A溶液中逐渐加入等浓度NaOH溶液,所得溶液中含A元素的微粒的物质的量分数和溶液pH的关系如图所示,则下列说法中正确的是

A.H2A的电离方程式为:H2A
H++HA- ,HA-
H++A2-
B.0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol/L
C.常温下,等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0
D.pH=4.0时,图中n(HA-)约为0.0091mol
高三化学选择题极难题查看答案及解析
-
下列各溶液中,微粒的物质的量浓度关系错误的是
A.0.1 mol·L-1 NH4Cl溶液:c(NH4+)<c( Cl-)
B.0.1 mol·L-1 Na2CO3溶液:c(Na+)=2c(HCO3-)+2c(CO32¯)+2c(H2CO3)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:
c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D.常温下,将醋酸钠、盐酸两溶液混合呈中性的溶液中:c(Na+)>c( Cl-)=c(CH3COOH)
高三化学选择题极难题查看答案及解析
-
一定温度下,在三个体积均为2.0L的恒容密闭容器中发生如下反应:PCl5(g)
PCl3(g)+Cl2(g)
编号
温度(℃)
起始物质的量
(mol)
平衡物质的量
(mol)
达到平衡所需时间(s)
PCl5(g)
PCl3(g)
Cl2(g)
Ⅰ
320
0.40
0.10
0.10
t1
Ⅱ
320
0.80
t2
Ⅲ
410
0.40
0.15
0.15
t3
下列说法正确的是( )
A.平衡常数K:容器Ⅱ>容器Ⅲ
B.反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ
C.反应到达平衡时,容器I中的平均速率为v(PCl5)=0.1/t1 mol/(L•s)
D.起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl30.45 mol和Cl20.10 mol,则反应将向逆反应方向进行
高三化学选择题极难题查看答案及解析