-
室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
选项
实验操作和现象
结论
A
向苯酚钠溶液中滴加NaHSO3溶液,溶液变浑浊
苯酚酸性弱于H2SO3酸性
B
向AgNO3溶液中逐滴加入浓度均为0.05 mol·L-1的NaI、NaCl混合溶液,有黄色沉淀生成
Ksp(AgCl)>Ksp(AgI)
C
向FeCl3溶液中加入Cu粉,Cu粉溶解
Cu的还原性大于Fe
D
向盛有H2O2溶液的试管中滴几滴酸化的FeCl2溶液,溶液变成棕黄色,一段时间后,溶液中有气泡出现
铁离子催化H2O2的分解
A.A B.B C.C D.D
高三化学多选题中等难度题查看答案及解析
-
硫酸亚铁的用途广泛,可以制备下图所示物质,下列说法错误的是( )

A.
属于碱式盐,可用作净水剂
B.与足量
反应的离子方程式为:
C.可用稀硫酸和
溶液检验铁红中是否含有
D.“冷却结晶”后的操作是过滤,“煅烧”操作的主要仪器有酒精灯、蒸发皿、玻璃棒
高三化学多选题中等难度题查看答案及解析
-
室温下,Ka(CH3COOH)=1.8×10-5,Kb(NH3·H2O)=1.8×10-5。CH3COOH和CH3COONH4形成的缓冲溶液常用于高岭土的成分分析。若溶液混合引起的体积变化可忽略,室温时下列指定溶液中微粒浓度关系正确的是( )
A.0.1 mol·L-1 CH3COOH溶液:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B.0.1 mol·L-1 CH3COONH4溶液:c(NH4+)=c(CH3COO-)>c(H+)=c(OH-)
C.0.1 mol·L-1 CH3COOH溶液和0.1 mol·L-1 CH3COONH4溶液等体积混合:c(NH4+)+c(NH3·H2O)+c(OH-)=c(CH3COOH)+c(H+)
D.0.3 mol·L-1 CH3COOH溶液和0.1 mol·L-1 CH3COONH4溶液等体积混合:c(CH3COOH)+c(H+)-c(NH3·H2O)-c(OH-)=0.15 mol·L-1
高三化学多选题中等难度题查看答案及解析
-
化合物Y是一种免疫抑制剂,可由X制得。
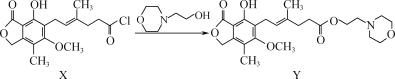
下列有关化合物X、Y的说法正确的是( )
A.X转化为Y的反应为取代反应 B.Y的化学式为C23H32O7N
C.1 mol Y最多能与4 mol NaOH反应 D.X中所有碳原子可能在同一平面
高三化学多选题中等难度题查看答案及解析
-
室温时,向100mL 0.1mol·L-1 NH4HSO4溶液中滴加0.1mol·L-1NaOH溶液,溶液pH随NaOH溶液体积的变化如图所示。下列说法正确的是( )
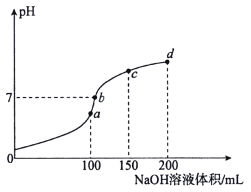
A.图中a、b、c、d四个点,水的电离程度最大的是d点
B.a点处存在c(NH4+)+c(NH3·H2O)=0.1mol·L-1
C.b点处存在c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
D.由b到c发生反应的离子方程式为NH4++OH-=NH3·H2O
高三化学多选题中等难度题查看答案及解析
-
高铁酸钠是一种新型高效水处理剂,主要制备方法如下:
湿法:Fe(OH)3+NaC1O+NaOH—Na2FeO4+NaC1+H2O(反应未配平)
干法:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列说法正确的是( )
A.高铁酸钠既有杀菌消毒的作用也有净水的作用
B.用湿法制备1molNa2FeO4需消耗1mol NaClO
C.干法中被FeSO4还原的Na2O2与做还原剂的Na2O2的物质的量之比为4:1
D.分别用湿法和干法制备等量高铁酸钠,两个反应过程中转移的电子数相同
高三化学多选题中等难度题查看答案及解析
-
W、X、Y、Z为周期序数依次增大的前四周期元素(不含稀有气体元素),W、X、Y能形成一种以X为中心的原子个数比为1:1:1的共价型化合物,它们的价电子数之和为14,Z的价电子数为8。下列有关说法正确的是
A.X、Y均能与Z形成两种及两种以上的化合物
B.电负性的大小关系为W>X>Y
C.某些含Y或Z的物质可用于饮用水的杀菌和消毒
D.W、X、Y、Z在元素周期表中分别属于四个不同的区
高三化学多选题中等难度题查看答案及解析
-
室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项
实验操作和现象
结论
A
向X溶液中滴加
溶液,振荡,有白色沉淀生成
X溶液中一定含有
B
向浓度均为0.05mol·L-1的
、
混合溶液中滴加少量
溶液,有蓝色沉淀生成
C
向2mL浓度均为0.05mol·L-1的
、
混合溶液中滴加几滴氯水,振荡,再滴加淀粉溶液,溶液显蓝色
的还原性比
的强
D
向
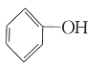 浊液中加入足量的
浊液中加入足量的溶液,浊液变为澄清
结合
能力:
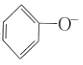
A.A B.B C.C D.D
高三化学多选题中等难度题查看答案及解析
-
设
为阿伏伽德罗常数的值,下列说法不正确的是
A.常温下,1LpH=10的
溶液中所含
的数目为
NA
B.氯碱工业中转移2mol电子时,通过阳离子交换膜的
的数目为2NA
C.过量的铜与含0.2mol
的浓硝酸反应,转移电子的数目大于0.1NA
D.室温下向1LpH=1的醋酸溶液中加水稀释,所得溶液中
的数目大于0.1NA
高三化学多选题中等难度题查看答案及解析
-
某药物中间体X,其结构如图所示。下列说法正确的是
A.X分子中含有手性碳原子
B.X可发生氧化、消去、取代等反应
C.X既能与盐酸反应,又能与NaOH溶液反应
D.1mol X与H2反应,最多消耗4mol H2
高三化学多选题中等难度题查看答案及解析