-
NO、NO2可被氨水溶液吸收(6NO+ 4NH3→5N2+6H2O;6NO2+ 8NH3→7N2+12H2O)。现有NO与NO2(不含N2O4)混合气体90mol被30%的氨水4.45×103g完全吸收,产生78mol氮气。吸收后氨水密度为0.980 g/cm3。则
A.原混合气体的平均组成为NO1.1 B.原氨水的浓度约为17.3mol/L
C.吸收后氨水的浓度约为2.4mol/L D.吸收后氨水的质量分数约为0.5
高三化学多选题困难题查看答案及解析
-
室温下,0.2mol/L的一元碱BOH与等浓度的盐酸等体积混合后,所得溶液中部分微粒的组分及浓度如图所示,下列对混合溶液的分析正确的是

A.溶液显酸性
B.升温,c(X)增大,c(Y)减小
C.c(B+) + c(Y) = c(Cl-)
D.稀释溶液,c(X)增大,c(Z)增大
高三化学多选题困难题查看答案及解析
-
常温下,将Cl2缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1 mol/L NaOH溶液,整个过程中pH的变化如图所示。下列有关叙述正确的是( )
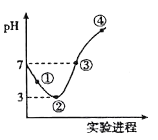
A.用pH试纸测①处c(H+)约为②处c (H+)的两倍
B.可依据②处数据计算所溶解的n(Cl2)
C.③处表示溶液中,c(Na+)= c(ClO-) + c(Cl-)
D.曲线③④段有离子反应:HClO+OH-=ClO-+H2O
高三化学多选题困难题查看答案及解析
-
下列有关离子方程式正确的是( )。
A.向稀盐酸中加入少量钠粒:2Na+2H2O=2Na+2OH+H2↑
B.NaHSO4溶液与Ba(OH)2溶液混合呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
C.用漂白粉溶液吸收尾气中SO2:Ca2++2ClO+SO2+H2O=CaSO3↓+2HClO
D.向含氯化铝的氯化镁溶液中加入氧化镁:2Al3++3MgO+3H2O=2Al(OH)3↓+3Mg2+
高三化学多选题困难题查看答案及解析
-
某恒温密闭容器中,可逆反应A(s)
B+C(g)-Q达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是
A.产物B的状态只能为固态或液态
B.平衡时,单位时间内n(A)消耗﹕n(C)消耗=1﹕1
C.保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动
D.若开始时向容器中加入1molB和1molC,达到平衡时放出热量Q
高三化学多选题困难题查看答案及解析
-
下列溶液中微粒的关系正确是
A.pH=2的HA溶液与pH=12的MOH溶液任意比混合:c(H+) + c(M+)=c(OH-) + c(A-)
B.氨水和盐酸混合后溶液呈酸性,溶液中可能存在:c(NH4+) > c(Cl-)
C.在一定温度下,相同pH的硫酸和硫酸铁溶液中水电离出来的c(H+)分别是1.0×10-amol/L和是1.0×10-bmol/L,在此温度时,水的离子积为1.0×10-(a + b)
D.常温下,0.1 mol/L酸HA pH=3,0.1 mol/L 碱BOH pH=13,则盐BA溶液的pH<7
高三化学多选题困难题查看答案及解析
-
下列离子反应方程式正确的是
A.将少量SO2气体通入NaClO溶液中:2ClO-+SO2+H2O→SO32-+2HClO
B.硫化氢气体通入硫酸亚铁溶液产生黑色硫化亚铁沉淀:H2S+Fe2+→FeS↓+ 2H+
C.向偏铝酸钠溶液中通入过量CO2:AlO2-+CO2+2H2O→Al(OH)3↓+HCO3-
D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加足量Ba(OH)2溶液 NH4++Al3++2SO42—+2Ba2++5OH-→AlO2-+2BaSO4↓+NH3·H2O+2H2O
高三化学多选题困难题查看答案及解析
-
“氯化反应”一般指将氯元素引入化合物中的反应,一般包括置换氯化、加成氯化和氧化氯化。已知在制“氯乙烯反应”中, HC≡CH (g)+HCl(g)
CH2=CHCl(g)的反应机理如图所示:

下列说法正确的是
A.碳碳叁键的键能:M1小于CH≡CH
B.由题图可知M2→M3的变化过程是热能转变成化学能的过程
C.该氯乙烯反应的总反应速率取决于M2→M3的反应速率
D.HgCl2是“氯化反应”的催化剂,不会参与反应的过程
高三化学多选题困难题查看答案及解析
-
某恒温密闭容器中,可逆反应A(s)
B+C(g)-Q达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是
A.产物B的状态只能为固态或液态
B.平衡时,单位时间内n(A)消耗﹕n(C)消耗=1﹕1
C.保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动
D.若开始时向容器中加入1molB和1molC,达到平衡时放出热量Q
高三化学多选题困难题查看答案及解析
-
改变0.1 mol·L-1己二酸(简写为H2A,电离常数分别为Ka1、Ka2)溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示。下列叙述错误的是

A.Ka1=10-4.4
B.曲线II表示的是HA-的物质的最分数δ(X)肋pH的变化关系
C.NaHA溶液中:c(H+)=c(OH-)+2c(A2-)-c(H2A)
D.等物质的量浓度的Na2A与NaHA混合溶液中:c(Na+)>c(A2-)>c(HA-)>c(H+)>c(OH-)
高三化学多选题困难题查看答案及解析