-
H2C2O4为二元弱酸。25 ℃时,向0.100 mol·L−1 Na2C2O4溶液中缓缓通入HCl气体(忽略溶液体积的变化)。下列指定溶液中微粒的物质的量浓度关系正确的是
A.0.100 mol·L−1 Na2C2O4溶液中:c(C2O42−)>c(HC2O4−)>c(OH−)>c(H+)
B.pH=7的溶液中:c(Cl-)=c(HC2O4−)+2c(H2C2O4)
C.c(Cl-)=0.100 mol·L−1溶液中:c(OH−)‒c(H+)=c(H2C2O4)‒c(C2O42−)
D.c(HC2O4−)=c(C2O42−)的酸性溶液中:c(Cl-)+c(HC2O4−)<0.100 mol·L−1+c(H2C2O4)
高三化学多选题困难题查看答案及解析
-
化合物Y具有保肝、抗炎、增强免疫等功效,可由X制得。下列有关化合物X、Y的说法正确的是
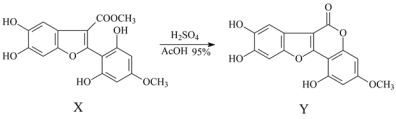
A.一定条件下X可发生氧化、取代、消去反应
B.1 mol Y最多能与4mol NaOH反应
C.X与足量H2反应后,每个产物分子中含有8个手性碳原子
D.等物质的量的X、Y分别与足量Br2反应,最多消耗Br2的物质的量相等
高三化学多选题困难题查看答案及解析
-
下图所示为镍锌可充电电池放电时电极发生物质转化的示意图,电池使用KOH 和K2Zn(OH)4为电解质溶液,下列关于该电池说法正确的是
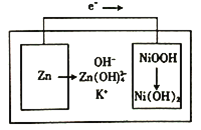
A.放电时溶液中的K+移向负极
B.充电时阴极附近的pH会升高
C.放电时正极反应为H+ +NiOOH+e-=Ni(OH)2
D.负极质量每减少6.5 g,溶液质量增加6.3 g
高三化学多选题困难题查看答案及解析
-
甲、乙为两个容积均为1 L的恒容密闭容器,向甲中充入1 mol CH4和1 mol CO2,乙中充入1 mol CH4和m mol CO2,加入催化剂,只发生反应:CH4(g)+CO2(g)
2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是( )
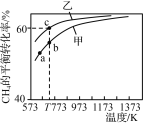
A.该反应的正反应是放热反应
B.a、b、c三点处,容器内气体总压强:p(a)<p(b)<p(c)
C.T K时,该反应的平衡常数小于12.96
D.恒温时向甲的平衡体系中再充入CO2、CH4各0.4 mol,CO、H2各1.2 mol,重新达平衡前,v(正)>v(逆)
高三化学多选题困难题查看答案及解析
-
25℃时,二元酸H3PO3的pKa1、pKa2(pK=-lgK)依次为1.30、6.60,氨水的pKb为4.75。常温时,下列指定溶液中微粒物质的量浓度关系正确的是( )
A.0.1 mol·L-1NH4H2PO3溶液中:c(H3PO3)>c(NH3·H2O)>c(H+)>c(OH-)
B.0.1 mol·L-1H3PO3溶液用NaOH溶液滴定至pH=6.60:c(H2PO3-)=c(HPO32-)
C.0.1 mol·L-1H3PO3溶液用氨水滴定至pH=7.0:c(NH4+)=c(H2PO3- )+c(HPO32-)
D.0.4 mol·L-1氨水与0.2 mol·L-1NaH2PO3等体积混合(体积变化可忽略):c(NH3·H2O)<c(H2PO3-)+2c(H3PO3)+0.1 mol·L-1
高三化学多选题困难题查看答案及解析
-
常温下,用0.1mol/LNaOH溶液分别滴定20mL浓度均为0.10mol/L的CH3COOH溶液和HCN溶液,所得滴定曲线如图所示。已知:CH3COOH的Ka=1.75×10-5,HCN的Ka=4.9×10-10。下列说法正确的是( )
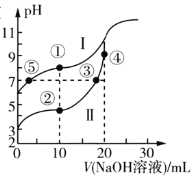
A.点①与点②对应的溶液中:c(CH3COO-)>c(CN-)
B.点②对应的溶液中:c(Na+)+c(H+)=c(CN-)+C(OH-)
C.点③和点⑤对应的溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
D.点④对应的溶液中:c(OH-)=c(H+)+c(CH3CO0H)
高三化学多选题困难题查看答案及解析
-
下列有关实验的描述正确的是( )
选项
操作
实验目的
A
沿玻璃棒将蒸馏水缓慢倒入盛有浓硫酸的烧杯中,边加边搅拌
稀释浓硫酸
B
测定相同浓度的Na2SO4和Na2SiO3溶液的pH值
比较硫和硅的非金属性强弱
C
将铁的氧化物溶于过量稀盐酸中,再滴加几滴紫红色KMnO4溶液
判断某铁的氧化物是否含有Fe2+
D
向2 mL 0.1 mol·L–1 NaOH溶液中滴加足量0.1mol·L–1 MgCl2溶液,出现白色沉淀后,再滴加3滴0.1 mol·L–1 FeCl3溶液,出现红褐色沉淀
Ksp[Mg(OH)2]>Ksp[Fe(OH)3]
A.A B.B C.C D.D
高三化学多选题困难题查看答案及解析
-
在3个体积均为1 L的恒容密闭容器中发生反应:SO2(g)+2NO(g)
2NO2(g)+S(s)。
改变容器I的反应温度,平衡时c( NO2)与温度的关系如下图所示。下列说法正确的是( )
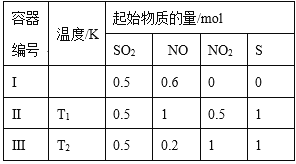
A.该反应的ΔH<0
B.T1时,该反应的平衡常数为
C.容器Ⅰ与容器Ⅱ均在T1时达到平衡,总压强之比小于1:2
D.若T2<T1,达到平衡时,容器Ⅲ中NO的体积分数小于40%
高三化学多选题困难题查看答案及解析
-
工业上一般在恒容密闭容器中采用下列反应合成甲醇:
CO(g) +2H2(g)
CH3OH(g) △H =-90.8 kJ·mol-1
300℃时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器
甲
乙
丙
反应物投入量
1 molCO、2 mol H2
1mol CH3OH
2mol CH3OH
平衡
时
数据
CH3OH的浓度(mol·L-1)
c1
c2
c3
反应的能量变化
a kJ
bkJ
ckJ
体系压强(Pa)
p1
p2
p3
反应物转化率
a1
a2
a3
下列说法正确的是
A. 2c1>c3 B. ∣a∣+∣b∣=90.8
C. 2p2<p3 D. a1+ a3<1
高三化学多选题困难题查看答案及解析
-
25 ℃时,NaCN溶液中CN-、HCN浓度所占分数(δ)随pH变化的关系如下图甲所示。向10 mL 0.01 mol·L-1 NaCN溶液中逐滴加入0.01 mol·L-1的盐酸,其pH变化曲线如下图乙所示。
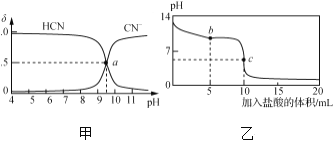
下列溶液中微粒的物质的量浓度关系一定正确的是( )
A. 图甲中pH=7的溶液:c(Cl-)=c(HCN)
B. 图甲中a点的溶液:c(CN-)<c(Cl-)
C. 图乙中b点的溶液:c(CN-)>c(Cl-)>c(HCN)>c(OH-)>c(H+)
D. 图乙中c点的溶液:c(Na+)+c(H+)=c(HCN)+c(OH-)+2c(CN-)
高三化学多选题困难题查看答案及解析