-
Ⅰ.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分【解析】
2Mg5Al3(OH)19(H2O)4
27H2O↑+10MgO+3Al2O3
(1)写出该化合物作阻燃剂的两条依据____________。
(2)用离子方程式表示除去固体产物中Al2O3的原理________。
(3)已知MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理____________。
Ⅱ.磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:
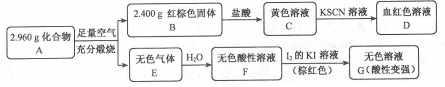
请回答:
(1)A的组成元素为_________(用元素符号表示),化学式为______。
(2)溶液C可溶解铜片,例举该反应的一个实际应用____________。
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518 g·L-1),该气体分子的电子式为____。写出该反应的离子方程式__________。
(4)写出F→G反应的化学方程式_____________。设计实验方案探究溶液G中的主要微粒(不考虑H2O、H+、K+、I-)______________。
高三化学简答题困难题查看答案及解析
-
(14分)FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。请回答下列问题:
(1)FeCl3净水的原理是 。FeCl3 溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3。
①若酸性FeCl2废液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,则该溶液的PH约为 。
②完成NaClO3 氧化FeCl2 的离子方程式:
(3)FeCl3 在溶液中分三步水解:
Fe3++H2O
Fe(OH)2++H+ K1
Fe(OH)2++H2O
Fe(OH)2++H+ K2
Fe(OH)++H2O
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:xFe3++yH2O
Fex(OH)y(3x-y)++yH+
欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释
c.加入NH4Cl d.加入NaHCO3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 。
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为 mg·L-1。
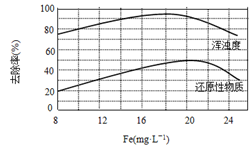
高三化学简答题极难题查看答案及解析
-
(13分)(1)在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g)
2C(g)+D(s) △H1<0反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。

①该反应的平衡常数表达式为K=___。升高温度,平衡常数将____(填“增大”“减小
”或“不变”)。
②能判断该反应是
否达到化学平衡状态的依据是________。
A.容器中压强不
变
B.混合气体的密度不变
C.υ(A):υ(B):υ(C)=2:1:2
D.c(A)=c(
C)
(2)为研究不同条件对反应2NO(g)+Cl2(g)
2C1NO(g) △H2<0的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol C12,10 min时反应达到平衡。测得NO的转化率为
。其他条件保持不变,反应在恒压条件下进行,平衡时NO的转化率为
,则
__________
,(填“大于”“小于”或“等于”)。
(3)甲醇(CH3OH)是重要的能源物质,研究甲醇具有重要意义。为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2—离子。电池工作时负极反应式为_________________。用该燃料电池作电源,以石墨为电极电解足量的硫酸铜溶液,当电路中通过0.1 mol电子时,若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入_____(填物质名称),其
质量约为_______g。
高三化学简答题极难题查看答案及解析
-
(12分)Mn(OH)2常用作油漆催干剂。向MnSO4溶液加入NaOH溶液,待沉淀完全后,过滤,洗涤,烘干即可制得Mn(OH)2。
(1)已知:常温下Mn(OH)2的Ksp=1.0×10-15。如果要使溶液中Mn2+沉淀完全,则应该保持溶液中c(OH—)≥ mol·L—1[当c(Mn2+)≤10-5mol/L时,即可认为溶液中Mn2+沉淀完全]。
(2)Mn(OH)2还可以通过MnO2与二氧化硫气体充分接触,再与石灰乳反应制得,写出该反应的总的化学方程式 。
(3)一种含Mn2+的结晶水合物组成为AxMnyBz·mH2O(A表示一种阳离子,B表示一种阴离子)。现称取39.10 g晶体配成100 mL溶液X,取20 mL溶液X,向其中加入足量的氢氧化钠溶液,加热,得到896 mL气体(标准状况);另取20 mL溶液X,向其中加入盐酸,无沉淀产生,再加入BaCl2溶液,产生白色沉淀,过滤,洗涤,烘干,得到固体9.32 g。
①A、B的离子符号分别为 、 。
②通过计算确定该结晶水合物的化学式(写出计算过程)。
高三化学简答题困难题查看答案及解析
-
丙烯酰胺(H2C=CH—CONH2)具有致癌性和遗传毒性。丙烯酰胺主要是由高碳水化合物、低蛋白质的植物性食物在加热(120 ℃以上)过程中形成,特别在烘烤、油炸时更易形成。丙烯酰胺可以进一步形成在工业上有用的聚丙烯酰胺类物质。

回答下列问题:
(1)D的结构简式为______________;F的结构简式为______________。
(2)指明下列反应类型:A→B____________________,C→D______________________。
(3)丙烯酰胺有多种同分异构体,写出分子中同时含有醛基和碳碳双键的同分异构体:______________________。
(4)写出化学方程式D→E:__________________________________________。2分子C在浓硫酸作用下可形成一个六元酯环,该反应的化学方程式为___________________________。
高三化学简答题困难题查看答案及解析
-
有机物分子中与“
”相连的碳原子上的氢活性较大,可以与甲醛或卤代烃等发生反应.
已知: ①

②
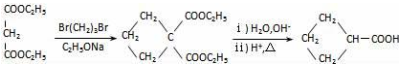
有机物 J 是重要的工业原料,其合成路线如下(部分产物和反应条件略):
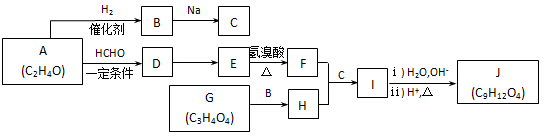
(1) A 中所含官能团的名称是_________.
(2) A→B 的反应类型是________反应. B→C 的反应方程式_____________.
(3) G 俗称缩苹果酸,与 B 以物质的量之比 1:2 反应,则 G+B→H 的化学方程式是__________.
(4) D 的分子式为 C5H10O4,若一次取样检验 D 的含氧官能团,按顺序写出所用试剂________.
(5)已知 E 中只有一种官能团,且核磁共振氢谱显示其分子中有两种不同化学环境的氢.则下列说法正确的是___________(填序号).
a.E 与 B 互为同系物 b. E 中含有的官能团是醚键
c.F 在一定条件下也可转化为 E d. F 中也有两种不同化学环境的氢
(6)J 的结构简式是________. J 的同分异构体 X 属于芳香族化合物, 1mol X 分别与足量 Na 或 NaOH 反应时的物质的量之比是 1:4 和 1:1,且苯环上只有一种一氯代物.写出符合上述所有条件的 X 的一种结构简式__________.
高三化学简答题困难题查看答案及解析
-
元素及其化合物在生活及生产中有很多重要用途.
Ⅰ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物.
(1)拟卤素如(CN)2、(SCN)2、(OCN)2 等与卤素单质结构相似、性质相近.已知(CN)2分子中所有原子都满足 8 电子稳定结构,则其分子中 σ 键与 π 键数目之比为_______.(SCN)2对应的酸有两种,理论上硫氰酸(H﹣S﹣C≡N )的沸点低于异硫氰酸(H﹣N=C=S)的沸点,其原因是_____________.
(2)卤化物 RbICl2 在加热时会分解为晶格能相对较大的卤化物 A 和卤素互化物或卤素单质,A 的化学式_____________.
Ⅱ.SiC、GaN、GaP、GaAs 等是人工合成半导体的材料, 具有高温、高频、大功率和抗辐射的应用性能而成为半导体领域研究热点.试回答下列问题:
(3)碳的基态原子 L 层电子轨道表达式为_______,砷属于_________区元素.
(4)N 与氢元素可形成一种原子个数比为 1:1 的粒子,其式量为 60,经测定该粒子中有一正四面体构型,判断该粒子中存在的化学键_________.
A.配位键 B.极性共价键 C.非极性共价键 D.氢键
(5)CaC2晶体的晶胞结构与 NaCl 晶体的相似(如图1 所示),但 CaC2 晶体中含有的哑铃形 C22﹣的存在,使晶胞沿一个方向拉长. CaC2 晶体中 1 个 Ca2+周围距离最近的 C22﹣数目为________.
Ш. A、B、C 为原子序数依次递增的前四周期的元素,A 的第一电离能介于镁和硫两元素之间,A 单质晶体的晶胞结构如图2 所示. B的价电子排布为(n+1)sn(n+1)pn+2,C位于元素周期表的 ds 区,其基态原子不存在不成对电子. B与 C所形成化合物晶体的晶胞如图3 所示.
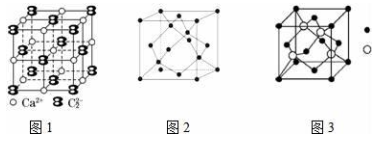
(6)A 单质晶体属于_________晶体(填晶体类型).
(7)B 与 C 所形成化合物晶体的化学式___________.
高三化学简答题中等难度题查看答案及解析
-
胆矾是一种常见的化合物,工业上它也是一种制取其它含铜化合物的原料,现有废铜(主要杂质为 Fe)来制备胆矾.有人设计了如下流程:
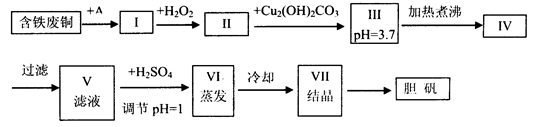
pH 值控制可参考下列数据
物质
开始沉淀时的 pH 值
完全沉淀时的 pH 值
氢氧化铁
2.7
3.7
氢氧化亚铁
7.6
9.6
氢氧化铜
5.2
6.4
请根据上述流程回答下列问题:
(1) A 可选用________(填字母).
a.稀 H2SO4 b.浓 H2SO4、加热 c.浓 FeCl3 溶液 d.浓 HNO3
(2) Ⅰ中加 H2O2 的目的____________.
(3) Ⅱ中加 Cu2(OH)2CO3 的目的是_________,其优点是___________.
(4) Ⅲ加热煮沸时发生的化学反应的离子方程式为 _____________.
(5) V 中加 H2SO4 调节 pH=1 是为了____________,某工程师认为上述流程中所加的 A 物质并不理想,需作改进,其理由是_________,若你是工程师,将对所加的 A 物质作何改进?请提出建议_________.
高三化学简答题中等难度题查看答案及解析
-
某兴趣小组的同学发现,将CuSO4溶液与K2CO3溶液混合会产生蓝绿色沉淀,它们对沉淀的组成和兴趣,决定采用实验大方法进行探究。
(1)【提出猜想】
猜想1:所得沉淀为Cu(OH)2;
猜想2:所得沉淀为______________________;(填化学式)
猜想3:所得沉淀为碱式碳酸铜[化学式可表示为mCu(OH)2·nCuCO3]。
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【实验探究】
步骤1:将所得悬浊液过滤,先用蒸馏水洗涤,再用无水乙醇洗涤,风干;
步骤2:甲同学取一定量固体,用气密性良好的如下装置(夹持仪器未画)进行定性实验;
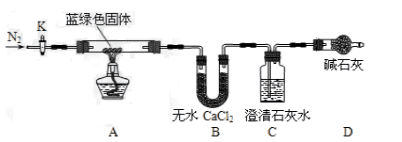
(2)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设________成立。
(3)乙同学认为只要将上图中B装置的试剂改用下列某试剂后,便可验证上述所有假设,该试剂是_______(填代号)。
A.浓硫酸 B.无水CuSO4 C.碱石灰 D.P2O5
(4)乙同学验证假设3成立的实验现象是______________。
【定量探究】
(5)乙同学进一步探究假设3中固体的组成:
①乙同学查得一些物质在常温时的数据(如下表)后,将C中的澄清石灰水改为Ba(OH)2溶液,其原因是__________(填代号)。
溶解度(S)/p
溶度积(Ksp)
摩尔质量(M)/g·mol
Ca(OH)2
Ba(OH)2
CaCO3
BaCO3
CaCO3
BaCO3
0.16
3.89
2.9×10-9
2.6×10-9
100
197
A.Ba(OH)2溶解度大于Ca(OH)2,能充分吸收CO2
B.Ba(OH)2为强碱,Ca(OH)2为弱碱
C.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
D.相同条件下,CaCO3的溶解度明显大于BaCO3
②若所取蓝绿色固体质量为27.1g,实验结束后,装置B的质量增加2.7g,C中产生沉淀的质量为19.7g。则该蓝绿色固体的化学式为__________;A中发生反应的化学方程式为_____。
高三化学简答题中等难度题查看答案及解析
-
工业碳酸钠(纯度约为 98%)中常含有 Ca2+、Mg2+、Fe3+、Clˉ和SO42ˉ等杂质.为了提纯工业碳酸钠,并获得试剂级碳酸钠,采取工艺流程如图所示:
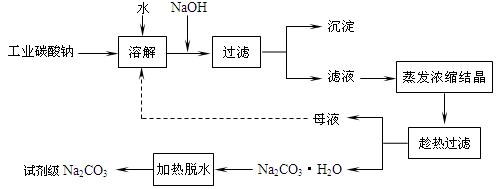
已知:Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如下图所示:
Ⅱ.有关物质的溶度积如下
物质
CaCO3
MgCO3
Ca(OH)2
Mg(OH)2
Fe(OH)3
Ksp
4.96×10﹣9
6.82×10﹣6
4.68×10﹣6
5.61×10﹣12
2.64×10﹣39
(1)加入 NaOH 溶液主要为了除去 (填离子符号),发生反应的离子方程式为__________;“沉淀”的主要成份有________(填化学式);向含有Mg2+、Fe3+的溶液中滴加 NaOH 溶液,当两种沉淀共存且溶液的 pH=8 时, c(Mg2+):c(Fe3+)=_________.
(2)热的 Na2CO3 溶液有较强的去油污能力,其原因是(用离子方程式及必要的文字加以解释)__________.
(3) “趁热过滤”时的温度应控制在____________.
(4)已知:Na2CO3•10H2O(s)=Na2CO3(s)+10H2O(g) △H=+532.36kJ•mol﹣1
Na2CO3•10H2O(s)=Na2CO3•H2O(s)+9H2O(g) △H=+473.63kJ•mol﹣1
写出 Na2CO3•H2O 脱水反应的热化学方程式__________________.
(5)有人从“绿色化学”角度设想将“母液”沿流程图中虚线所示进行循环使用.请你分析实际生产中是否可行_______,其理由是___________________.
高三化学简答题困难题查看答案及解析