-
一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3•CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中.从废料中回收氧化钴(CoO)的工艺流程如下:
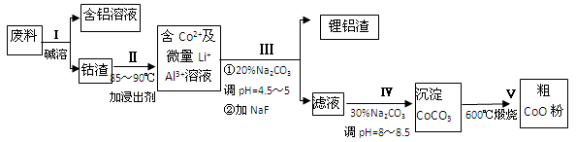
(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为 .
(2)过程II中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴.则浸出钴的离子反应方程式为 (产物中只有一种酸根).请从反应原理分析不用盐酸浸出钴的主要原因 .
(3)碳酸钠溶液在过程III和IV中所起作用有所不同,请分别用离子方程式表示在过程III、IV中起的作用: .
高三化学简答题极难题查看答案及解析
-
[化学——选修2:化学与技术]聚合硫酸铁(PFS)是水处理中重要的絮凝剂,下图是以回收废铁屑为原料制备PFS的一种工艺流程。
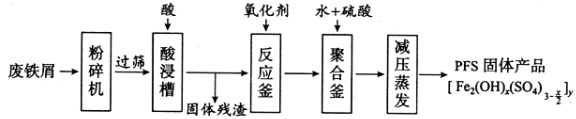
回答下列问题
(1)废铁屑主要为表面附有大量铁锈的铁,铁锈的主要成分为_________。粉碎过筛的目的是_______。
(2)酸浸时最合适的酸是_____,写出铁锈与酸反应的离子方程式_____________________。
(3)反应釜中加入氧化剂的作用是_________,下列氧化剂中最合适的是____________(填标号)。
a.KMnO4b.
c.
d.
(4)聚合釜中溶液的pH必须控制在一定的范围内。pH偏小时Fe3+水解程度弱,pH偏大时则_______。
(5)相对于常压蒸发,减压蒸发的优点是______。
(6)盐基度B是衡量絮凝剂絮凝效果的重要指标,定义式为
(n为物质的量)。为测量样品的B值,取样品mg,准确加入过量盐酸,充分反应,再加入煮沸后冷却的蒸馏水,以酚酞为指示剂,用c
的标准NaOH溶液进行中和滴定(部分操作略去,已排除铁离子干扰)。到终点时消耗NaOH溶液V mL。按照上述步骤做空白对照试验,消耗NaOH溶液
,已知该样品中Fe的质量分数w,则B的表达式为__________。
高三化学简答题困难题查看答案及解析
-
磷及其化合物与人类生产、生活密切相关。请回答下列问题:
(1)少量CO的存在会引起生产中催化剂中毒,常用SO2氧化CO,本身被还原为S。
已知:① Cc(s)+ 1/2O2 (g)=CO (g) △H1=-l26.4kJ·mol-1
②③C(s)+O2 (g) =CO2 (g) △H2=-393.5kJ·mol-1
@S(s)+O2 (g)=SO2 (g) △H3=-296.8kJ·mol-1
则SO2氧化CO的热化学反应方程式__________________。
(2) CO可用于合成甲醇,反应方程式CO(g)+2H2(g)
CH3OH(g)。
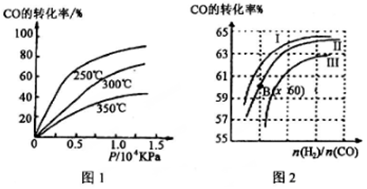
① CO转化率与温度、压强的关系如图所示,该反应△H_______0 (填“>”或“<”)
图2中曲线I、II、III对应的平衡常数分别为K1、K2、K3,则它们的大小关系为___________。测得B(x,60)点氢气的转化率为40%,则x=___________。
②一定条件下,将2molCO和2molH2置于容积为2L固定的密闭容器中发生上述反应,达到平衡时,CO与H2体积之比为2:1,则平衡常数K=___________。
(3)处理高浓度乙醛废水的原理:2CH3CHO+H2O
CH3CH2OH+CH3COOH。使用惰性电极电解,以一定浓度的CH3CHO –Na2SO4溶液为电解貭溶液模拟工业处理,其装置如图3所示:
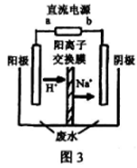
①电解过程中,两极除分别生成乙酸和乙醇外,均产生无色气体,阳极电极反应分别:4OH- -4e-=O2↑+2H2O;__________________。
②在实际处现过程中,阴极区乙醛的去除率可达60%。若在两极区分别注入lm3乙醛的含量为300mg •L-1的废水,可得到乙醇_______ kg(结果保留2位小数)。
高三化学简答题中等难度题查看答案及解析
-
红矾钠(重铬酸钠:Na2Cr2O7•2H2O)是重要的化工原料,工业上用铬铁矿(主要成分是FeO•Cr2O3)制备红矾钠的过程中会发生如下反应:4FeO(s)+Cr2O3(s)+8Na2CO3(s)+7O2(g)
8Na2CrO4(s)+
2Fe2O3(s)+8CO2(g) ΔH<0
(1)请写出上述反应的化学平衡常数表达式:K= 。
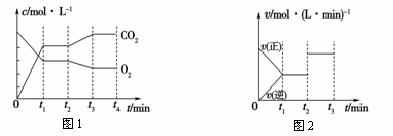
(2)图1、图2表示上述反应在t1时达到平衡,在t2时因改变某个条件而发生变化的曲线。由图1判断,反应进行至t2时,曲线发生变化的原因是____________________(用文字表达);
由图2判断,t2到t3的曲线变化的原因可能是________(填写序号)。
A.升高温度 B.加了催化剂 C.通入O2 D.缩小容器体积
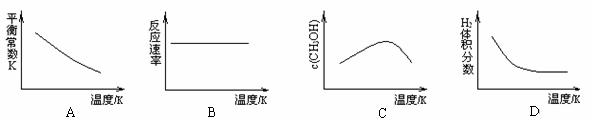
(3) 工业上可用上述反应中的副产物CO2来生产甲醇:CO2(g)+3H2(g)
CH3OH(g)+H2O(g),已知该反应能自发进行,在容积固定的密闭容器中,由CO2和H2合成甲醇,则下列图像正确的是 。
高三化学简答题困难题查看答案及解析
-
有机物Ⅰ是合成某功能高分子材料的中间体。实验室由A和F制备Ⅰ的合成路线如下:
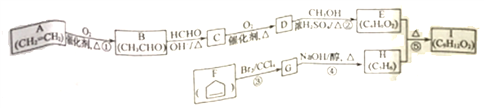
已知:①RCHO+CH3CHO
RCH=CHCHO+H2O(R代表烃基或氢原子)
②
+I
回答下列问题:
(1)C的分子式是____________,C中的官能团名称为____________。
(2)②的反应类型是____________,⑤的反应类型是_____________。
(3)I的结构简式为_______________。
(4)④的反应方程式为____________________________________________________。
(5)F的同分异构体中,属于炔烃的有____________种,其中核磁共振氢谱显示有3种不同化学环境的氢,峰面积比为6∶1∶1的结构简式为__________________。
(6)写出用乙烯和1,3一丁二烯为原料制备化合物
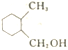 的合成路线:_________________(其他试剂任选)。
的合成路线:_________________(其他试剂任选)。高三化学简答题中等难度题查看答案及解析
-
CH4、NH3、H2O、H2S、NH4NO3和ZnS是中学化学常见的六种化合物。回答下列问题:
(1)基态S原子有__________种不同能量的电子,与Zn同属ds区且同周期的元素基态原子核外电子排布式为____________________。
(2)H2O和H2S中,沸点较高的是__________,原因是___________________________________。
(3)CH4、NH3和H2O3种氢化物中,键角由大到小的顺序为_______________,其中NH3的VESEPR模型名称为____________。
(4)NO3-离子的几何构型为__________,NO3-离子的电子体有_____________(任写一种)。
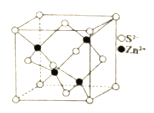
(5)ZnS晶体结构有多种,其中一种晶体的晶胞结构如图所示,晶体中与S2-等距离且最近的S2-有_____个。已知该晶体的晶胞参数为anm,其密度为 ρg·cm-3,则阿伏加德罗常数的数值为____________________________(用含字母a、ρ的表达式表示,列出计算式即可)。
高三化学简答题中等难度题查看答案及解析
-
碳及化合物在生产生活中用比较广泛。回答下列问题:
(1)已知:①H2(g)+
O2(g)=H2O(1)△H1=-285.8kJ·mol-1
②CH3OH(1)+
O2(g)=CO2(g)+2H2O(1) △H2=-725.5kJ·mol-1
则CO2(g)+3H2(g)=CH2OH(1)+H2O(1)的反应热 △H=____________。
(2)某研究小组用CO合成甲醇:CO(g)+2H2(g)
CH3OH(g)△H<0,将三组混合气体分别通入到三个2L恒容密闭容器中进行反应,得到如下三组实验数据:
实验组
温度
起始时物质的量/mol
平衡时物质的量/mol
达到平衡所需的时间/min
CO
H2
CH3OH
CO
H2
CH3OH
1
650
2.0
6.0
0
1.0
5
2
900
2.0
6.0
0
1.2
2
3
650
1.0
4.0
2.0
a
b
c
t
实验1条件下平衡常数K=__________,a、b之间可能的关系为_____________。
已知反应CO(g)+2H2(g)
CH3OH(g)中CO的转化率(a)与温度(T)、压强(p)的关系如右图所示:
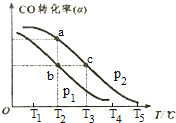
①p1______p2(填“<”“>”“=”)。先升高温度、后增大压强,能否实现b点到c点的转化?__________(填“能”或“不能”),原因是_____________________________________________。
②a、c两点的反应速率为v1________v2(填“<”“>”“=”)。
③在不改变反应物用量情况下,为提高CO的转化率可采取的措施是_____________(答出三条措施)。
高三化学简答题困难题查看答案及解析
-
明矾[KAl(SO4) 2 ·12H2O]易溶于水,不易溶于乙醇,在生产、生活中有广泛用途。利用炼铝厂的废料——铝灰(含Al、Al2O3及少量的SiO2、FeO·xFe2O3)制备明矾的工艺流程如下:
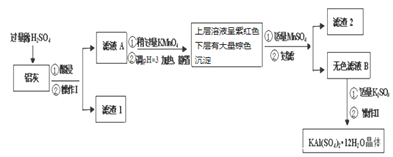
回答下列问题:
(1)酸浸时为提高铝的浸取率,可采取的措施是_________(填标号)。
a.改用同浓度的硝酸 b.用硫酸多次浸取
c.浸取时间缩短一半 d.适当升高温度
(2)滤渣1的成分是__________;滤渣2经过处理可以制得一种高效的无机高分子混凝剂,其化学式为[Fe2(OH)n(SO4)(3-0.5n)]m,则该物质中铁元素的化合价为___________。
(3)检验滤液A中含有Fe2+的实验方案及现象是________________________________________。
(4)已知常温下Ksp[Fe(OH)3]=4.0×10-38,当调节溶液的pH=3时,溶液中c(Fe3+)=____________。
(5)操作Ⅱ中包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等操作,使用酒精洗涤明矾晶体的目的是___________________________________________________________________;明矾净水的原理是_______________________________________(写离子方程式)。
(6)已知在pH=3和加热条件下,MnO4-可与Mn2+反应生成MnO2,则上述流程图中加入适量MnSO4发生反应的离子方程式为_________________________。
高三化学简答题中等难度题查看答案及解析
-
氯化铜在工农业生产中具有重要的用途。某化学兴趣小组设计如图所示装置,用CuCl2·2H2O晶体和SOCl2获取无水CuCl2并回收过量的SOCl2。已知:SOCl2的熔点为-105℃,沸点为76℃,遇水剧烈水解生成两种酸性气体。回答下列问题:
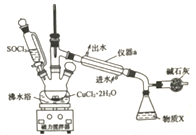
(1)在空气中直接加热CuCl2·2H2O晶体得不到纯净的无水CuCl2的原因是___________________(用化学方程式表示)。
(2)仪器a的名称是____________,锥形瓶中得到的物质x的化学式为______________。
(3)碱石灰中含有CaO和NaOH,NaOH的电子式为__________,碱石灰的作用是______________。
(4)三颈烧瓶中CuCl2·2H2O和SOCl2发生反应的化学方程式是_______________________。
(5)某同学用“间接碘量法”测定无水CuCl2样品中铜元素的百分含量,过程如下:取 0.2800 g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀。滴入几滴淀粉溶液作指示剂,用0.1000 mol·L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL(滴定反应为I2+2S2O32-=S4O42-+2I-)。
①滴定到终点时的现象是_____________________________________。
②该试样中铜元素的百分含量为__________ 。
高三化学简答题中等难度题查看答案及解析
-
砷(As)及其化合物在生产、医疗、科技等方面有许多应用
(1)中国自古“信口雌黄”、“雄黄入药”之说。雄黄As2S3和雌黄As4S4都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。一定条件下,雌黄和雄黄的转化关系如图所示。
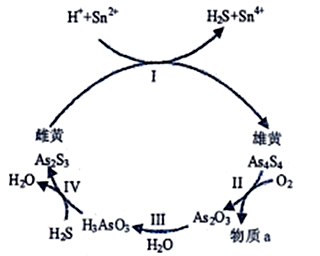
①砷元素有+2、+3+5等常见价态。,雌黄和雄黄中S元素的价态相同,其价态是______________。I中发生的离子方程式是______________________________。
②Ⅱ中,雄黄在空气中加热至300℃时会产生两种物质,若4.28g As4S4反应转移0.28mole-,则a为_______________(填化学式)砒霜(As2O3)可用双氧水将氧化成H3AsO4而除去,该反应的化学方程式为:____________________________________。
(2)AsH3是一种很强的还原剂,室温下, 0.4mol AsH3气体在空气中自燃,氧化产物为As2O3固体,放出b kJ 热量,AsH3自燃的热化学方程式是:____________________________________。
(3)将Na3AsO3(aq)+I2(aq)+H2O(l)
Na2HasO4(aq)+NaI (aq)设计成原电池如图所示,放电时电流强度(I)与时间关系如图所示.
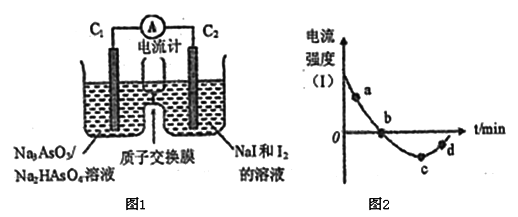
①如图中表示在该时刻上述可逆反应达到平衡状态的点是_________________(填字母)。
②已知:a点对应如图中电流由C1极经外电路流向C2极。则d点对应的负极的反应式为_____________。
③如图中,b→c改变条件可能是____________(填代号),c→d电流强度变化的原因是___________。
A.向左室中加入适量的浓Na3AsO3溶液 B.向左室中加入适量的烧碱溶液
C.向右室中加入适量的浓KI溶液 D. 向右室中加入适量的稀硫酸
高三化学简答题困难题查看答案及解析