-
(14分) 实验室用苯和浓硝酸、浓硫酸发生反应制取硝基苯的装置如图所示.回答下列问题:
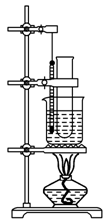
(1)反应需在50℃~60℃的温度下进行,图中给反应物加热的方法是水浴加热,其优点是_____ ___和_____ ___;
(2)在配制混合酸时应将__________加入到________中去;
(3)该反应的化学方程式是________________________________;反应类型:
(4)由于装置的缺陷,该实验可能会导致的不良后果是______ __.
(5)反应完毕后,除去混合酸,所得粗产品用如下操作精制:
①蒸馏 ②水洗 ③用干燥剂干燥 ④用10%NaOH溶液洗 ⑤水洗
正确的操作顺序是 。
A.①②③④⑤ B.②④⑤③① C.④②③①⑤ D.②④①⑤③
高一化学实验题极难题查看答案及解析
-
甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素。
(1)该反应的离子方程式为 。
设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
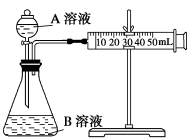
(2)甲组:通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小。实验装置如图,实验时分液漏斗中A溶液一次性放下,A、B的成分见下表:
序号
A溶液
B溶液
①
2 mL 0.1 mol/L H2C2O4溶液
4 mL 0.01 mol/L KMnO4溶液
②
2 mL 0.2 mol/L H2C2O4溶液
4 mL 0.01 mol/L KMnO4溶液
③
2 mL 0.2 mol/L H2C2O4溶液
4 mL 0.01 mol/L KMnO4溶液和少量MnSO4
该实验探究的是 对化学反应速率的影响。在反应停止之前,相同时间内针管中所得CO2的体积由大到小的顺序是 (用实验序号填空)。
(3)乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率的大小。取两支试管各加入2 mL 0.1 mol/L H2C2O4溶液,另取两支试管各加入4 mL 0.1 mol/L KMnO4溶液。将四支试管分成两组(各有一支盛有H2C2O4溶液和KMnO4溶液的试管),一组放入冷水中,另一组放入热水中,经过一段时间后,分别混合并振荡,记录溶液褪色所需时间。该实验目的是研究 对化学反应速率的影响,但该组同学始终没有看到溶液褪色,其原因是 。
高一化学实验题极难题查看答案及解析
-
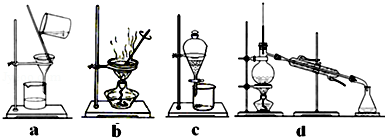
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下图:

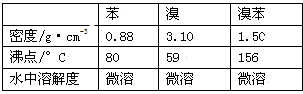
(1)在a中加入15mL无水苯和少量铁屑.在b中小心加入4.0mL液态溴.向a中滴入几滴溴,有白色烟雾产生,是因为生成了______气体.继续滴加至液溴滴完.装置d的作用是______;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是:______.
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是______;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为______,要进一步提纯,下列操作中必须的是_______(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是______(填入正确选项前的字母).
A.25mL B.50mL C.250mL D.500mL
高一化学实验题极难题查看答案及解析
-
(12分)(1)已知H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1。若向三份等体积、等物质的量浓度的NaOH溶液中分别加入醋酸、浓硫酸、稀硝酸至恰好完全反应,并将上述过程中放出的热量分别记为Q1kJ、Q2kJ、Q3kJ。则三者的由小到大关系是________(用Q1、Q2、Q3表示)。
(2)如图所示A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其目的是_____________; 若实验中不加盖泡沫塑料板,则求得的中和热数值 (填偏大、偏小、无影响)。
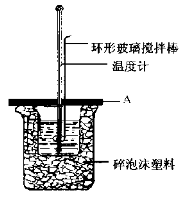
(3)实验室用50mL 0.50mol·L-1盐酸、50mL 0.55mol·L-1NaOH溶液利用上图装置,进行测定中和热的实验。假设盐酸和氢氧化钠溶液的密度都是1 g/cm3,又知中和后生成溶液的比热容c=4.18 J/(g·℃)。为了计算中和热,实验时还需测量的数据有(填序号)________。
A.反应前盐酸的温度
B.反应前盐酸的质量
C.反应前氢氧化钠溶液的温度
D.反应前氢氧化钠溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
实验序号
起始温度t1/℃
终止温度t2/℃
盐酸
氢氧化钠溶液
混合溶液
1
20.0
20.1
23.4
2
20.2
20.4
23.6
3
20.5
20.6
23.8
依据该学生的实验数据计算,该实验测得的中和热ΔH为________。(保留三位有效数字)
高一化学实验题极难题查看答案及解析
-
(2015秋•桃源县校级月考)电子工业中用过量的FeCl3溶液溶解电路板中的铜箔时,会产生大量废液.由该废液回收铜并得到净水剂(FeCl3•6H2O)的步骤如下:
I.在废液中加入过量铁粉,过滤;
II.向I的滤渣中加入过量试剂A,充分反应后,过滤,得到铜;
III.合并I和II中的滤液,不断通入氯气至完全反应;
IV. ,得到FeCl3•6H2O晶体.
(1)用FeCl3溶液腐蚀铜箔的离子方程式是 .
(2)试剂A是 .
(3)步骤III反应过程中既有Fe2+又有Fe3+,如果要验证滤液中铁元素的存在形式,可另取反应过程中的两份滤液分别进行实验,实验方法、现象与结论如下表,请将其补充完整.可供选择的试剂:
a.酸性KMnO4 b.NaOH溶液 c.KSCN溶液 d.氯水
实验方法
实验现象
结论
步骤1:在滤液中加入 (填字母)
滤液中有Fe3+
步骤2:在滤液中加入 (填字母)
滤液中有Fe2+
(4)完成步骤IV需要用到的实验装置是 (填字母).
高一化学实验题极难题查看答案及解析