-
I.二甲醚(CH3OCH3)被称为21世纪的新型燃料,工业上以CO和H2为原料生产二甲醚。已知:
①CO(g)+2H2(g) CH3OH(g) △H=-99kJ/mol
CH3OH(g) △H=-99kJ/mol
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H=-24 kJ/mol
CH3OCH3(g)+H2O(g) △H=-24 kJ/mol
③CO(g)+H2O(g) H2(g)+CO2(g) △H=-41 kJ/mol
H2(g)+CO2(g) △H=-41 kJ/mol
(1)反应4H2(g)+2CO(g) CH3OCH3(g)+H2O(g)的△H=___________。
CH3OCH3(g)+H2O(g)的△H=___________。
(2)某温度下,将4.0molH2和4.0molCO充入容积为1L的密闭容器中,发生反应3CO(g)+3H2(g) CH3OCH3(g)+CO2(g),5min时CO2的物质的量浓度为0.5mo1/L,10min后反应达到平衡状态,测得二甲醚的体积分数为25%。
CH3OCH3(g)+CO2(g),5min时CO2的物质的量浓度为0.5mo1/L,10min后反应达到平衡状态,测得二甲醚的体积分数为25%。
①5min时CO的转化率=___________;
②该温度下此反应的平衡常数K=___________;
③下列措施能提高 CH3OCH3平衡产率的有___________(填标号)。
A.分离出 CH3OCH3 B.升高温度 C.增大压强 D.改用高效催化剂
Ⅱ.液氨是一种良好的储氢物质
已知:2NH3(g) N2(g)+3H2(g) △H=+92.4 kJ/mol
N2(g)+3H2(g) △H=+92.4 kJ/mol
其他条件相同时,反应在不同金属催化剂作用下进行相同时间后,氨的转化率[a(NH3)]随反应温度的变化情况如图所示。
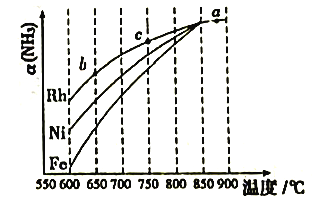
(1)用___________作催化剂时,氨气分解反应的活化能最大。
(2)a点所代表的状态___________(填“是”或“不是”)平衡状态。
(3)c点时NH3的转化率高于b点时NH3的转化率,原因是______________________。
-
(14分)二甲醚(CH3OCH。)和甲醇(CH3OH)被称为21世纪的新型燃料,具有清洁、高效等优良的性能。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:
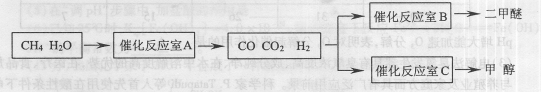
(1)催化反应室B中CO与H2合成二甲醚的化学方程式为________.
(2)催化反应室A中发生的反应为:
CH4(g)+H2O(g) CO(g)+3H2(g)……(I)、CO(g)+H2O(g)
CO(g)+3H2(g)……(I)、CO(g)+H2O(g) CO2(g)+H2(g)……(Ⅱ)催化反应室C中发生的反应为:
CO2(g)+H2(g)……(Ⅱ)催化反应室C中发生的反应为:
CO(g)+2H2(g) CH3OH(g)……(Ⅲ)、CO2(g)+3H2(g)
CH3OH(g)……(Ⅲ)、CO2(g)+3H2(g) CH3OH(g)+H2O(g)……(Ⅳ)
CH3OH(g)+H2O(g)……(Ⅳ)
①已知:原子利用率= ×100%,试求反应(Ⅳ)的原子利用率为________。
×100%,试求反应(Ⅳ)的原子利用率为________。
②反应(Ⅳ)的△S ________0(填“>”、“=”或“<”)。
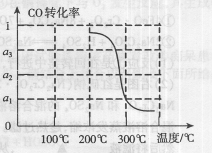
③在压强为5MPa,体积为VL的反应室c中,amol CO与20mol H2在催化剂作用下发生反应(Ⅲ)生成甲醇,CO的转化率与温度的关系如右图。则该反应的△H________0(填“>”、“=”或“<”)。300℃时该反应的平衡常数K= ________(用含字母的代数式表示)。
(3)我国某科研所提供一种碱性“直接二甲醚燃料电池”。
该燃料电池负极的电极反应式为:
CH3OCH3一12e一+16OH一=2CO2-3+11H2O。有人提出了一种利用氯碱工业产品治理含二氧化硫(体积分数为x)废气的方法如下:
①将含SO2的废气通人电解饱和食盐水所得溶液中,得NaHSO3溶液;
②将电解饱和食盐水所得气体反应后制得盐酸;
③将盐酸加入NaHSO3溶液中得SO2气体回收。
用上述碱性“直接二甲醚燃料电池”电解食盐水来处理标准状况下VL的废气,计算消耗二甲醚的质量。
-
二甲醚(CH3OCH3)被称为21世纪的新型燃料,以CO和H2为原料生产二甲醚主要发生以下三个反应:
| 化学反应方程式 | | 化学平衡常数 |
| ①CO(g)+2H2(g) CH3OH(g) CH3OH(g) | ΔH1=-99 kJ•mol-1 | K1 |
| ②2CH3OH(g) CH3OCH3(g)+H2O(g) CH3OCH3(g)+H2O(g) | ΔH2=-24 kJ•mol-1 | K2 |
| ③CO(g)+H2O(g) CO2(g)+H2(g) CO2(g)+H2(g) | ΔH3=-41 kJ•mol-1 | K3 |
(1)该工艺的总反应为3CO(g)+3H2(g) CH3OCH3(g)+CO2(g) ΔH
CH3OCH3(g)+CO2(g) ΔH
该反应ΔH=__________________,化学平衡常数K=____________________(用含K1、K2、K3的代数式表示)。
(2)某温度下,将8.0molH2和4.0molCO充入容积为2L的密闭容器中,发生反应:4H2(g)+2CO(g)  CH3OCH3(g)+H2O(g),10 分钟后反应达平衡,测得二甲醚的体积分数为25%,则CO的转化率为________。
CH3OCH3(g)+H2O(g),10 分钟后反应达平衡,测得二甲醚的体积分数为25%,则CO的转化率为________。
(3)下列措施中,能提高CH3OCH3产率的有________。
A.分离出二甲醚 B.升高温度 C.改用高效催化剂 D.增大压强
(4)该工艺中反应③的发生提高了CH3OCH3的产率,原因是_______________________________。
-
二甲醚(CH3OCH3,沸点为-24.9℃)被称为21世纪的新型能源。科学家利用太阳能分解水生成的氢气与从烟道气中分离出的CO2在催化剂作用下合成二甲醚,并开发出直接以二甲醚为燃料的燃料电池。其合成流程如下:
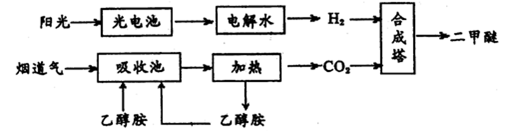
(1)已知:CH3OCH3(g)、H2(g)的标准燃烧热分别为:△H= -1455.0kJ·mol-1、△H= -285.8 kJ·mol-1。写出以CO2、H2合成CH3OCH3的热化学方程式:________;
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂。写出吸收CO2反应的化学方程式________;
(3)一定条件下用CO2和H2合成二甲醚,反应物气流量对CO2的转化率、二甲醚的选择性(是指转化生成二甲醚的碳占已转化碳的比例)影响结果如图1所示,当控制气流量为28mL· min-1时,则生成0.3mol二甲醚需要通入CO2的物质的量为________;
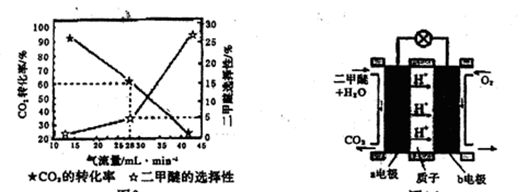
图1 图2
(4)图2为二甲醚燃料电池示意图。
①a电极的电极反应式为________;
②若以1.12 L·min-l(标准状况)的速率向该电池中通入二甲醚,用该电池电解50mL2 mol·L-1 CuSO4溶液,通电0.50 min后,计算理论上可析出金属铜的质量为。
-
二甲醚(CH3OCH3,沸点为-24.9℃)被称为21世纪的新型能源。科学家利用太阳能分解水生成的氢气与从烟道气中分离出的CO2在催化剂作用下合成二甲醚,并开发出直接以二甲醚为燃料的燃料电池。其合成流程如下:
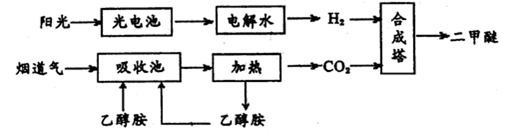
(1)已知:CH3OCH3(g)、H2(g)的标准燃烧热分别为:△H= -1455.0kJ·mol-1、△H= -285.8 kJ·mol-1。写出以CO2、H2合成CH3OCH3的热化学方程式:________;
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂。写出吸收CO2反应的化学方程式________;
(3)一定条件下用CO2和H2合成二甲醚,反应物气流量对CO2的转化率、二甲醚的选择性(是指转化生成二甲醚的碳占已转化碳的比例)影响结果如图1所示,当控制气流量为28mL· min-1时,则生成0.3mol二甲醚需要通入CO2的物质的量为________;
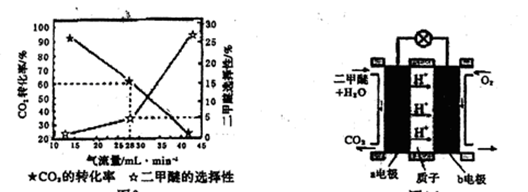
图1 图2
(4)图2为二甲醚燃料电池示意图。
①a电极的电极反应式为________;
②若以1.12 L·min-l(标准状况)的速率向该电池中通入二甲醚,用该电池电解50mL2 mol·L-1 CuSO4溶液,通电0.50 min后,计算理论上可析出金属铜的质量为。
-
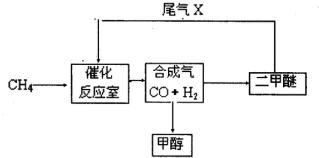
合成气(CO+H2)是一种重要的化工原料,在化工生产中具有十分广泛的用途. 可以生产被称为21世纪的新型燃料--甲醇、二甲醚(CH3OCH3)等物质.其工艺流程如下:
(1)写出用合成气生产二甲醚的化学方程式______ CH3OCH3+H2O
-
开发清洁能源是当今化工研究的一个热点问题。二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用,工业上以CO和H2为原料生产CH3OCH3。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g) CH3OH(g) △H1=-99kJ·mol-1
CH3OH(g) △H1=-99kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1
(1)催化反应室中的总反应3CO(g)+3H2(g) CH3OCH3(g)+CO2(g),计算△H=___。反应原料来自煤的气化。已知该反应的平衡常数表达式为K=
CH3OCH3(g)+CO2(g),计算△H=___。反应原料来自煤的气化。已知该反应的平衡常数表达式为K= ,每生成1molH2需要吸收131.3kJ的热量。写出该反应的热化学方程式___。
,每生成1molH2需要吸收131.3kJ的热量。写出该反应的热化学方程式___。
(2)在该条件下,若反应①的起始浓度分别为:c(CO)=0.6mol·L-1,c(H2)=1.4mol·L-1,8min后达到平衡,CO的转化率为50%,则8min内H2的平均反应速率为___。
(3)在t℃时,反应②的平衡常数为400,此温度下,在1L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol·L-1) | 0.46 | 1.0 | 1.0 |
此时刻v正___v逆(填“>”“<”或“=”),平衡时c(CH3OCH3)的物质的量浓度是___。
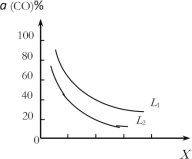
(4)在(1)小题中催化反应室的总反应3CO(g)+3H2(g) CH3OCH3(g)+CO2(g),CO的平衡转化率a(CO)与温度、压强的关系如图所示,图中X代表___(填“温度”或“压强”),且L1___L2(填“>”“<”或“=”)
CH3OCH3(g)+CO2(g),CO的平衡转化率a(CO)与温度、压强的关系如图所示,图中X代表___(填“温度”或“压强”),且L1___L2(填“>”“<”或“=”)
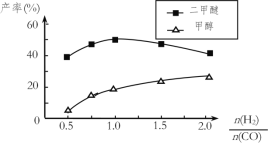
(5)在催化剂的作用下同时进行三个反应,发现随着起始投料比 的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:__。
的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:__。
-
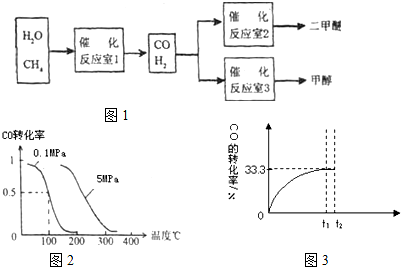
二甲醚和甲醇被称为21世纪的新型燃料,以CH4和H2O为原料制备二甲醚和甲醇的工业流程如图1:
I:(1)在一定条件下,容积为 100L密闭容器中发生反应:CH4(g)+H2O(g)⇌CO(g)+3H2(g);△H>0
将1.0mol CH4和2.0mol H2O(g)通入该密闭容器 l0min时有0.1mol CO生成,则10min内该反应的平均速率v(H2)______.
(2)在压强为0.1MPa条件下,容积为V L某密闭容器中a mol CO与 2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)⇌CH3OH(g)平衡时CO的转化率与温度、压强的关系如图2.
①该反应的△H______0 (填“<”、“>”或“=”).
②100℃时该反应的平衡常数K=______(用含a、V的代数式表示).
③在温度容积不变的情况下,向该密闭容器再增加a mol CO与 2a mol H2,达到新平衡时,CO的转化率______(填“增大”、“减小”或“不变”).平衡常数______(填“增大”、“减小”或“不变”)
④在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2反应生成CH3OH(g),达到平衡时CO的转化率为90%,此时容器内的压强为开始时的______倍.
II:某温度下,向密闭容器中充入2.0mol CO和1.0mol H2O,发生反应:
CO(g)+H2O(g)⇌CO2(g)+H2(g).CO的转化率随时间变化关系如图2,回答下列问题:
(1)如果一个可逆反应的平衡常数K值很大,下列说法正确的是______(填字母).
A.该反应的反应物混合后很不稳定
B.该反应一旦发生将在很短的时间内完成
C.该反应达平衡时至少有一种反应物的百分含量很小
D.该反应一定是放热反应 E.该反应使用催化剂意义不大
(2)t2时刻向平衡体系中再通入1.0mol H2O(g),请在原坐标图3中将改变这一条件后CO的转化率的变化结果表示出来.
-
二甲醚(CH3OCH3)被称为21世纪的新型燃料,清洁、高效,有优良的环保性能,以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.有关说法正确的是( )
A.电池中二甲醚反应后最终转化为CO2和H2O
B.正极:3O2+12e-+12H+=6H2O
C.负极:CH3OCH3+16OH--12e-=2CO32-+11H2O
D.负极:CH3OCH3-12e-+3H2O=12H++2CO2
-
甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455 kJ/mol,甲醚可作燃料电池的燃料。工业上用合成气(CO、H2)直接或间接制取甲醚。
(1)写出甲醚燃烧的热化学方程式________。
(2)已知H2(g)和C(s)的燃烧热分别是285.8 kJ·mol-1、393.5 kJ·mol-1;计算反应4C(s)+6H2(g)+O2(g)==2CH2OCH3(g)的反应热为________。(3)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极
可构成燃料电池。该电池的负极反应式为________
________;
从能量角度分析甲醚用作燃料电池与直接燃烧相比
主要的优点是________。
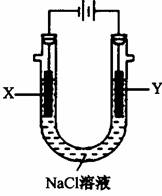
(4)用(3)中的燃料电池为电源,以石墨为电极电解
500 mL滴有酚酞的:NaCl溶液,装置如图所示:
①请写出电解过程中Y电极附近观察到的现象
________。
②当燃料电池消耗2.8 LO2(标准状况下)时,计算
此时:NaCl溶液的pH=________(假设溶液的体积不变,气体全部从溶液中逸出)。
CH3OH(g) △H=-99kJ/mol
CH3OCH3(g)+H2O(g) △H=-24 kJ/mol
H2(g)+CO2(g) △H=-41 kJ/mol
CH3OCH3(g)+H2O(g)的△H=___________。
CH3OCH3(g)+CO2(g),5min时CO2的物质的量浓度为0.5mo1/L,10min后反应达到平衡状态,测得二甲醚的体积分数为25%。
N2(g)+3H2(g) △H=+92.4 kJ/mol