-
工业食盐中含Ca2+、Mg2+等杂质,某厂电解饱和食盐水制取NaOH溶液的工艺流程如图所示,回答下列问题:
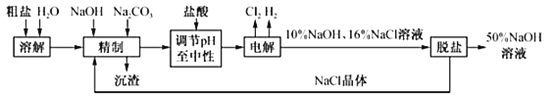
(1)“精制”过程中发生反应的离子方程式为_____
(2)若粗盐中SO42﹣含量也较高,沉淀剂可以是_____(填字母)且要在试剂Na2CO3之_____加入(填“前”或“后”)。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(3)在电解过程中,产生H2的电极与外接电源的_____极相连;溶液pH增大的区域是_____(填“阳极区”或“阴极区”)。
(4)烧碱和氯气是电解饱和食盐水时按照固定的比率k(质量比)生成的产品。理论上k=_____(填写计算表达式和结果且结果保留两位小数)。
-
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:

依据上图,完成下列填空:
(1)工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为
,
(2)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是
________(选填a、b、c,多选扣分)
A. Ba(OH)2 B. Ba(NO3)2 C. BaCl2
(3)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为
(选填a,b,c多选扣分)
a. 先加NaOH,后加Na2CO3,再加钡试剂
b. 先加NaOH,后加钡试剂,再加Na2CO3
c. 先加钡试剂,后加NaOH,再加Na2CO3
(4)电解过程的总反应方程为________。
(5)电解槽阳极产物可用于
(至少写出两种用途)。
-
氯碱工业是以电解饱和食盐水为基础的工业。饱和食盐水是以含Ca2+、Mg2+、SO42-、Fe3+等杂质离子的粗盐水精制,需要使用的药品包括:①稀盐酸 ②烧碱溶液 ③碳酸钠溶液 ④氯化钡溶液。下列有关说法不正确的是( )
A.加入烧碱溶液主要是除去Mg2+、Fe3+
B.药品加入的先后顺序可以是②③④①
C.加入稀盐酸主要是除去所加过量物质中的OH-、CO32-
D.加入碳酸钠溶液主要是除去Ca2+及所加过量物质中的Ba2+
-
工业上对海水资源综合开发利用的部分工艺流程如图1所示.
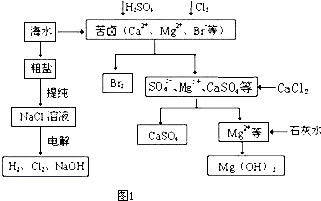
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质,粗制后可得饱和NaCl溶液,精制时通常在溶液中依次中加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性.请写出加入Na2CO3溶液后相关化学反应的离子方程式:______.
(2)本工艺流程中先后制得Br2、CaSO4、Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4的顺序制备?______(填“能”或“否”),原因是______.
(3)氯化钠是重要的氯碱工业化工的原料.电解饱和食盐水常用离子膜电解槽和隔膜电解槽.离子膜和隔膜均允许通过的分子或离子是______.
A.Cl- B.Na+ C.OH- D.Cl2
(4)饱和食盐水电解时与电源正极相连的电极上发生的反应为______,与电源负极线连的电极附近溶液pH______(变大、不变、变小).
(5)氯化钠的可用于生产纯碱,我国化学家侯德榜改革国外生产工艺,生产流程简要表示如图2:
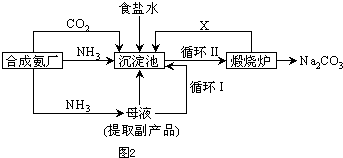
①上述生产纯碱的方法称______,副产品的一种用途为______.
写出上述流程中X物质的分子式______.使原料氯化钠的利用率从70%提高到90%以上,主要是设计了______(填上述流程中的编号)的循环.从沉淀池中取出沉淀的操作是______.
②合成氨原料气中氮气制备的方法之一为______,另一原料气氢气的制取化学方程式为______ CO+H2,CO+H2O CO2+H2
CO2+H2
-
电解法制碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42-杂质,不符合电解要求,因此必须经过精制.某校实验小组精制粗盐水的实验过程如下:
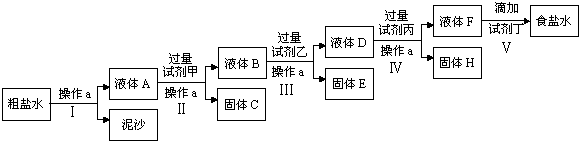
请回答以下问题:
(1)操作a的名称是________,所用玻璃仪器有________;
(2)在Ⅱ步中,加入过量试剂甲后,生成了两种大量的难溶沉淀,则试剂甲为________(填化学式)溶液;
(3)写出固体H所含物质的化学式________;
(4)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的;
溶解时:________.
过滤时:________.
蒸发时:________.
-
化工中把电解饱和食盐水的工业生产叫氯碱工业,其生产流程如下:
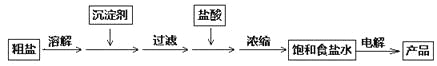
除去食盐水中的Ca2+、Mg2+、SO42—,应分别加入下列沉淀剂:①NaOH(aq)、
②Na2CO3(aq)、③BaCl2(aq),加入沉淀剂的顺序为 (填序号);加入盐酸的作用为 。
(2)下图为实验室电解饱和食盐水的实验装置。X、Y均为石墨电极,两极周围溶液均滴有几滴酚酞试液。
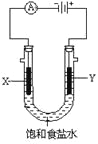
①电解一段时间后,X电极及附近溶液能观察到的现象是 ;
Y电极上的电极反应式为 ,检验该极产生的气体的方法是 。
②电解饱和食盐水的离子方程式为 ;若饱和食盐水体积为200mL,且忽略电解过程中的体积变化及气体溶解,当两极共收集到气体(共两种)44.8mL(标准状况)时,溶液的pH= 。
-
化工中把电解饱和食盐水的工业生产叫氯碱工业,其生产流程如下:
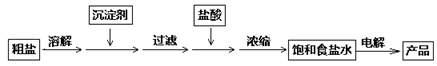
除去食盐水中的Ca2+、Mg2+、SO42—,应分别加入下列沉淀剂:①NaOH(aq)、
②Na2CO3(aq)、③BaCl2(aq),加入沉淀剂的顺序为________(填序号);加入盐酸的作用为________。
(2)下图为实验室电解饱和食盐水的实验装置。X、Y均为石墨电极,两极周围溶液均滴有几滴酚酞试液。
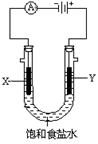
①电解一段时间后,X电极及附近溶液能观察到的现象是________;
Y电极上的电极反应式为________,检验该极产生的气体的方法是________。
②电解饱和食盐水的离子方程式为________;若饱和食盐水体积为200mL,且忽略电解过程中的体积变化及气体溶解,当两极共收集到气体(共两种)44.8mL(标准状况)时,溶液的pH=________。
-
(1)海水中有丰富的食盐资源,工业上以粗食盐水(含少量Ca2+、Mg2+杂质)、氨、石灰石等为原料,可以制备Na2CO3。流程如下:
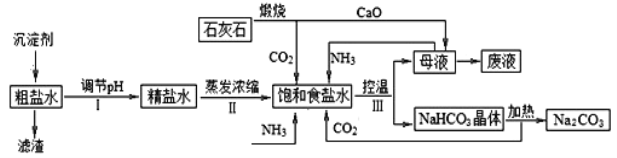
请回答:
①粗盐精制过程中加入的沉淀剂是石灰乳和纯碱,加入顺序是_____。
②上述流程中循环使用的物质是____。
③上图中制得的饱和食盐水还可用于氯碱工业,NaCl 溶液的电解产物可用于生产盐酸、漂白粉、氢氧化钠等产品。工业上电解饱和食盐水的离子方程式为_____。
④氨气可用电解法合成,其原料转化率大幅度提高, 有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如图 1 和图 2 所示。
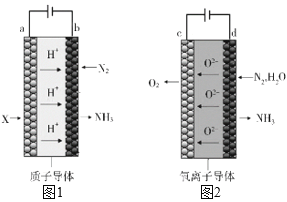
图 1 中,a 电极上通入的X 为_____。图 2 中,d 电极上的电极反应式为_________。
(2)海水中有丰富的锂资源,我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如图 3 所示:

图 3
①金属锂在电极_____(填“A”或“B”)上生成。
②阳极产生两种气体单质,电极反应式是_____。
③某种锂离子二次电池的总反应为:FePO4(s)+Li(s) LiFePO4(s) , 装置如下图所示(a 极材料为金属锂和石墨的复合材料)。下列说法不正确的是_____。
LiFePO4(s) , 装置如下图所示(a 极材料为金属锂和石墨的复合材料)。下列说法不正确的是_____。
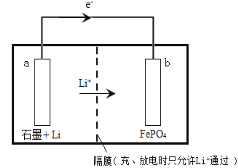
A.图中 e-及 Li+移动方向说明该电池处于放电状态
B.该电池中a 极不能接触水溶液
C.充电时 a 极连接外接电源的正极
D.充电时,b 极电极反应式为:LiFePO4-e-= Li++ FePO
-
如图为阳离子交换膜法电解饱和食盐水原理示意图。下列说法不正确的是( )
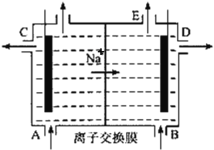
A.粗盐水中含Ca2+、Mg2+、SO42-等离子,精制时除杂试剂BaCl2溶液应在Na2CO3溶液之前加入
B.标准状况下每生成22.4LCl2,便产生2 mol NaOH
C.从E口逸出的气体是Cl2
D.从B口加入含少量NaOH的水溶液以增强导电性
-
(1)电解饱和食盐水之前食盐水需要精制,目的是除去粗盐中的Ca2+、Mg2+、SO42-等杂质离子,使用的试剂和操作有a.Na2CO3溶液,b.Ba(OH)2溶液,c.稀盐酸,d.过滤,其合理的加入顺序为________(填字母代号)。
(2)电解饱和食盐水时离子交换膜的作用是_____________________________
(3)电解饱和食盐水时,如果在容积为10 L的离子交换膜电解槽中,1 min在阳极可产生11.2 L(标准状况)Cl2,这时溶液的pH是(设体积维持不变)________。
(4)Cl2常用于自来水的杀菌消毒,现有一种新型消毒剂ClO2,若它们在杀菌过程中还原产物均为Cl-,消毒等量的自来水,所需Cl2和ClO2的物质的量之比为________。













