-
某兴趣小组欲探究SO2与Cu(OH)2 的反应。
| 实验 | 实验步骤 | 现象 |
| 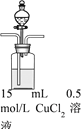
| 步骤1:打开分液漏斗,向烧瓶中加入30mL 0.5 mol/LNaOH溶液 | I. 有蓝色絮状沉淀,静置后分层。 |
| 步骤2:从左侧导管通入SO2气体 | II. 静置后分层,上层溶液为淡绿色,底部有白色沉淀 |
(1)现象I中产生蓝色沉淀的离子方程式是___________。
(2)甲为了确认现象II中白色沉淀的成分,进行如下探究。查阅资料:
| CuSO3 | CuCl | Cu2O |
| 溶解性 | 不溶于水,浅黄色沉淀 | 不溶于水,白色沉淀 | 不溶于水,砖红色沉淀 |
| 性质 | 与酸反应 | 能溶于较浓的HCl溶液 | 酸性体系中不稳定,进一步反应生成Cu和Cu2+ |
并进行如下实验:
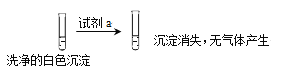
①试剂a是___________。
②现象II中生成白色沉淀的离子方程式是___________。
(3)甲认为Cu(OH)2沉淀全部转化为CuCl,乙依据实验现象对甲的观点进行反驳,依据的实验现象是_________。
(4)丙认为实验存在干扰,欲探究纯净的Cu(OH)2 悬浊液与SO2的反应。
①丙过滤I中的蓝色沉淀,洗涤,取最后一次洗涤液于试管中,_________(填操作和现象),证明已洗涤干净。再进行如下实验:
| 实验 | 实验步骤 | 现象 |
| 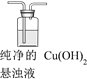
| 从左侧导管通入SO2气体 | III. 静置后分层,上层溶液为淡绿色,底部有砖红色沉淀。 |
②丙预测产物是Cu2O,取砖红色沉淀,洗涤后,_________(填操作和现象),证明产物是Cu2O。
(5)纯净的Cu(OH)2 悬浊液与SO2发生反应的化学方程式是_________。
-
(15分)
某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
| 装置 | 序号 | 试管中的药品 | 现象 |
| 持续通入 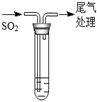
| 实验Ⅰ | 1.5 mL 1 mol·L-1 CuSO4溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| 实验Ⅱ | 1.5 mL 1 mol·L-1 CuCl2溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(1)制取新制Cu(OH)2悬浊液的离子方程式为 。
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明: 。检验Cu(OH)2洗涤干净的方法是 。
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl + 2NH3·H2O === Cu(NH3)2+ + Cl- + 2H2O 、 。
②乙同学用另一种方法证明了该白色沉淀为CuCl,实验方案如下:
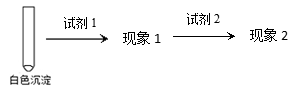
填写下表空格:
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式: 。
(4)丙同学通过实验证明:实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中, ,则说明砖红色沉淀是Cu2O。
-
某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
| 装置 | 序号 | 试管中的药品 | 现象 |
| 持续通入 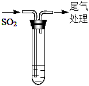
| 实验Ⅰ | 1.5 mL 1 mol·L-1 CuSO4溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| 实验Ⅱ | 1.5 mL 1 mol·L-1 CuCl2溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(1)制取新制Cu(OH)2悬浊液的离子方程式为 。
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明: 。检验Cu(OH)2洗涤干净的方法是 。
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl + 2NH3·H2O = Cu(NH3)2+ + Cl- + 2H2O 、 ____________ 。
②乙同学用另一种方法证明了该白色沉淀为CuCl,实验方案如下:
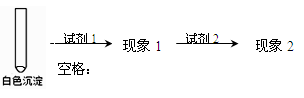
填写下表空格:
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式: 。
(4)丙同学通过实验证明实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中, _______________ ,则说明砖红色沉淀是Cu2O。
-
某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
| 装置 | 序号 | 试管中的药品 | 现象 |
| 持续通入 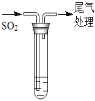
| 实验Ⅰ | 1.5 mL1 mol/L CuSO4溶液和3.5 mL 1mol/L NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| 实验Ⅱ | 1.5 mL1 mol/L CuCl2溶液和3.5 mL 1 mol/L NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(1)制取新制Cu(OH)2悬浊液的离子方程式为__________________________________。
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明:__________________,检验Cu(OH)2洗涤干净的方法是____________________________________________。
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl+2NH3·H2O
=Cu(NH3)2++Cl-+2H2O、____________________________。
②乙同学用另一种方法证明了该白色沉淀为CuCl,参考如下实验方案填写表格:
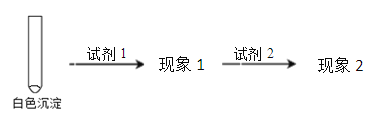
填写下表空格:
| 试剂1 | _________________ | 试剂2 | 蒸馏水 |
| 现象1 | _________________ | 现象2 | _________________ |
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式:_________________。
(4)丙同学通过实验证明:实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中,_________________________________,则说明砖红色沉淀是Cu2O。
-
(16分)某兴趣小组利用以下装置制备氮化镁并探究氮化镁的某些性质。
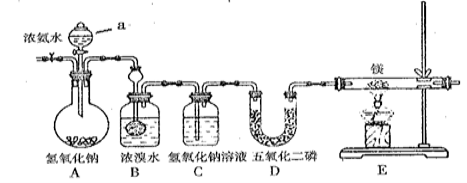
请完成横线上的相关问题:
(1)实验步骤及现象:
① 连接仪器并 。然后,向各仪器中加入适量所需药品。② 。
③ 打开分液漏斗活塞,观察到B中浓溴水颜色变浅至褪色,C中产生无色气泡。
④ 点燃酒精灯,观察到E中固体变成了黄绿色。(氮化镁是黄绿色固体,遇水剧烈反应生成两种碱)
(2)A装置中仪器a的名称为 。
(3)写出B处反应的化学方程式 。
(4)D装置中P2O5是一种非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是 。
A.NH3 B. H2 C.SO2 D.CO2
(5)E装置中发生反应的化学方程式为 。
(6)此装置中存在着明显缺陷,你的改进措施是 。
(7)某同学要探究E中固体成分。将E中的固体放入稀盐酸中,观察到固体溶解并产生气泡,写出此过程中反应的化学方程式 、 。
-
(11分)果汁在生产过程中添加亚硫酸及其盐类,以抑制有害微生物的生长及抗氧化。某化学兴趣小组查阅文献后,用下图所示装置测定某果汁样品中SO2残留量。
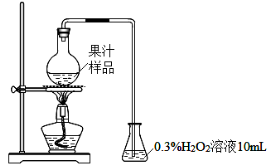
实验步骤:
(ⅰ)在烧瓶中加入50.00 mL果汁样品与3mL浓硫酸的混合液,加热10 min。
(ⅱ)移出锥形瓶,迅速滴入2~3滴酚酞试液,用0.01000 mol·L-1NaOH标准溶液滴定。
回答问题:
(1)实验室配制NaOH标准溶液时,不需要用到的仪器是 。
A.容量瓶 B.胶头滴管 C.烧瓶 D.玻璃棒
(2)将50. 00 mL果汁样品与3mL浓硫酸混合的操作是 。
(3)锥形瓶中发生反应的离子方程式是 。
(4)若步骤(ⅱ)消耗NaOH标准溶液25. 00 mL,则果汁样品中SO2残留量是 g/L。
(5)若改用0.5%的碘水10 mL作吸收液,实验中消耗NaOH标准溶液体积 。
A.V = 25 mL B.25 mL<V<50 mL C.V>50 mL
-
某研究小组利用题9图装置探究铜与浓硫酸反应的产物。
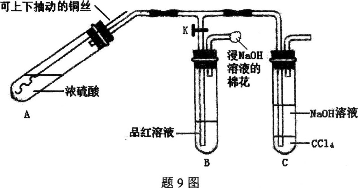
实验步骤与现象如下:
①检查装置气密性,向A中加入5 mL浓硫酸,打开K,将铜丝伸入浓硫酸中,给A处加热,观察到B中品红溶液褪色,再关闭K。
②实验观察到A中液面下铜丝变黑,产生气泡,液面上方产生大量白雾,一段时间后溶液中有白色固体出现,拉出铜丝,停止加热。回答下列问题:
(1)溶液中白色固体是 (填化学式),C中CCl4的作用是 。
(2)取出铜丝,用蒸馏水洗净后伸入到稀硫酸中,铜丝变亮、溶液变蓝。写出A中可能发生反应的化学方程式: 、 。
(3)分离出C中的上层液体,滴加过量稀盐酸和BaCl2溶液,有白色沉淀产生。
①分离的操作名称为: :
②白色沉淀为: ;
③产生白色沉淀的原因可能是 。
-
某研究小组利用题9图装置探究铜与浓硫酸反应的产物。
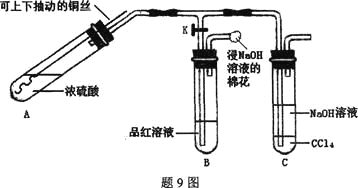
实验步骤与现象如下:
①检查装置气密性,向A中加入5 mL浓硫酸,打开K,将铜丝伸入浓硫酸中,给A处加热,观察到B中品红溶液褪色,再关闭K。
②实验观察到A中液面下铜丝变黑,产生气泡,液面上方产生大量白雾,一段时间后溶液中有白色固体出现,拉出铜丝,停止加热。回答下列问题:
(1)溶液中白色固体是 (填化学式),C中CCl4的作用是 。
(2)取出铜丝,用蒸馏水洗净后伸入到稀硫酸中,铜丝变亮、溶液变蓝。写出A中可能发生反应的化学方程式: 、 。
(3)分离出C中的上层液体,滴加过量稀盐酸和BaCl2溶液,有白色沉淀产生。
①分离的操作名称为: :
②白色沉淀为: ;
③产生白色沉淀的原因可能是 。
-
某研究小组利用如图装置探究铜与浓硫酸反应的产物。

实验步骤与现象如下:
①检查装置气密性,向A中加入5 mL浓硫酸,打开K,将铜丝伸入浓硫酸中,给A处加热,观察到B中品红溶液褪色,再关闭K。
②实验观察到A中液面下铜丝变黑,产生气泡,液面上方产生大量白雾,一段时间后溶液中有白色固体出现,拉出铜丝,停止加热。
将回答下列问题:
(1)C中CCl4的作用是_______________。
(2)下列说法中不合理的是:
A、上下移动A中铜丝可控制SO2的量
B、B中选用品红溶液验证有SO2生成
C、C中选用氢氧化钠溶液吸收多余的SO2,也可以改为澄清石灰水
D、为确认A中白色固体是CuSO4,可向A中加入水,观察颜色变化。
(3)取出铜丝,用蒸馏水洗净后伸入到稀硫酸中,铜丝变亮、溶液变蓝。写出A中可能发生反应的化学方程式:_______________________、______________________。
(4)分离出C中的上层液体,滴加过量稀盐酸和BaCl2溶液,有白色沉淀产生。
①分离的操作名称为___________________:
②白色沉淀为:_______________________;
③产生白色沉淀的原因可能是______________________________________________。
-
(16分)某化学兴趣小组为探究铜与浓硫酸的反应,用下图所示装置进行有关实验。 甲同学取ag Cu 片和12ml 18mol/L浓H2SO4放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的H2SO4和Cu剩余。

(1)Cu与浓H2SO4反应的化学方程式是_____________。装置E中试管D内盛有品红溶液,当C中气体集满后,D中有可能观察到的现象是____________,为避免实验装置D有可能造成环境污染试用最简单方法加以解决实验用品自选____ _____。
(2)装置B的作用是贮存多余的气体。B中应放置的液体是_______(填序号)。
a.饱和Na2SO3溶液 b.酸性 KMnO4溶液 c.浓溴水 d.饱和NaHSO3溶液
当D处有明显现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是_________________。
(3)反应完毕后,烧瓶中还有一定量的余酸,为什么却不能使Cu完全溶解的原因是_____________。使用足量的下列药品不能用来证明反应结束后的烧瓶中的确有余酸的是____________(填序号)。
a.Fe粉 b.BaCl2溶液 c.CuO d.Na2CO3溶液
实验中某学生向A中反应后溶液中通入一种常见气体单质,使铜片全部溶解且仅生成硫酸铜溶液,该反应的化学方程式是___________________________。














