25 ℃时,将0.10mol/L的NaOH溶液逐滴滴入20 mL 0.10 mol/LCH3COOH溶液中,pH随滴入NaOH溶液体积的变化如下图所示。
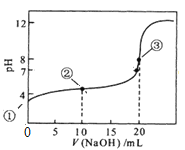
(1)点①存在的电离平衡是___________。
(2)点②两溶液发生反应的离子方程式是_______。
(3)点③溶液的pH_____7(填“>”、“<”或“=”),此时c(Na+)_____c(CH3COO-)(填“>”、“<”或“=”)。
高三化学实验题简单题
25 ℃时,将0.10mol/L的NaOH溶液逐滴滴入20 mL 0.10 mol/LCH3COOH溶液中,pH随滴入NaOH溶液体积的变化如下图所示。

(1)点①存在的电离平衡是___________。
(2)点②两溶液发生反应的离子方程式是_______。
(3)点③溶液的pH_____7(填“>”、“<”或“=”),此时c(Na+)_____c(CH3COO-)(填“>”、“<”或“=”)。
高三化学实验题简单题
25 ℃时,将0.10mol/L的NaOH溶液逐滴滴入20 mL 0.10 mol/LCH3COOH溶液中,pH随滴入NaOH溶液体积的变化如下图所示。

(1)点①存在的电离平衡是___________。
(2)点②两溶液发生反应的离子方程式是_______。
(3)点③溶液的pH_____7(填“>”、“<”或“=”),此时c(Na+)_____c(CH3COO-)(填“>”、“<”或“=”)。
高三化学实验题简单题查看答案及解析
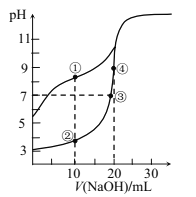
25℃时,将 0.10 mol•L-1的NaOH溶液逐滴滴入到20.00 mL 0.10 mol• L-1醋酸溶液中,溶液中的pH曲线与NaOH溶液体积的关系如图所示:
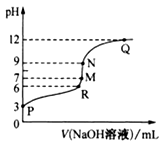
下列有关判断错误的是( )
A. 该温度下,醋酸的Ka的数量级为l0-5 B. N点对应的NaOH溶液体积可能为20.0mL
C. 溶液中,水的电离程度N点比Q点大 D. R点所示溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
高三化学选择题中等难度题查看答案及解析
25℃时,将20mL 0.10 mol/LCH3COOH溶液和20mL 0.10 mol/LHX溶液分别与20mL 0.10 mol/LNaHCO3溶液混合,测得产生气体的体积(V)随时间(t)变化如下图,下列说法中不正确的是
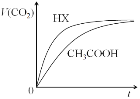
A. 反应开始前,HX溶液中c(H+)大于CH3COOH中c(H+)
B. CH3COOH溶液反应结束后,c(Na+)>c(CH3COO—)
C. 反应结束后所得两溶液中,c(CH3COO—)<c(X—)
D. 由该实验可知HX为强酸
高三化学单选题中等难度题查看答案及解析
常温下,用0.10 mol/L NaOH溶液分别滴定20.00 mL浓度均为0.10 mol/LCH3COOH溶液和 HCN 溶液所得滴定曲线如图[Ka(CH3COOH)>Ka(HCN)]。下列说法正确的是
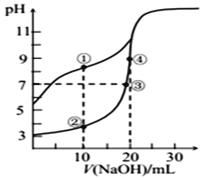
A.点①和点②所示溶液中:c(CH3COO﹣)<c(CN﹣)
B.点①和点②所示溶液中:c(CH3COO﹣)-c(CN﹣) = c(HCN)-c(CH3COOH)
C.溶液中水的电离程度:③>④
D.点③和点④所示溶液中都有:c(CH3COO﹣)+c(OH﹣) = c(CH3COOH)+c(H+)
高三化学单选题困难题查看答案及解析
T℃时,在20.00 mL 0.10 mol/LCH3COOH溶液中滴入0.10 mol/LNaOH溶液,溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
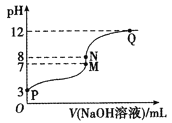
A.T℃时,CH3COOH的电离平衡常数Ka=1.0×10-3
B.M点对应的NaOH溶液的体积为20.00 mL
C.N点所示溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.N点与Q点所示溶液中水的电离程度:N>Q
高三化学单选题中等难度题查看答案及解析
常温下向20mL0.10mol/LCH3COOH溶液中滴加0.10mol/ L NaOH溶液时,混合溶液的pH与相关微粒的浓度关系如图所示。已知:pKa=-lgKa。下列说法不正确的是
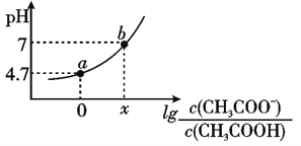
A. CH3COOH溶液中存在如下平衡:CH3COOHH++CH3COO-
B. b点,加入NaOH溶液的体积小于20mL
C. 将等物质的量的CH3COOH和CH3 COONa一起溶于蒸馏水中,得到对应a点的溶液
D. 常温下,CH3COOH的电离常数为Ka,则pKa=4.7
高三化学单选题困难题查看答案及解析
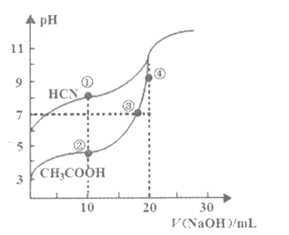
常温下,用0.10mol/LNaOH溶液分别滴定20.00mL浓度均为0.10mol/LCH3COOH溶液和HCN溶液所得滴定曲线如图[Ka(CH3COOH)>K(HCN)]。下列说法正确的是( )
A.点①和点②所示溶液中:c(CH3COO-)<c(CN-)
B.点③所示溶液中:c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
D.点③和点④所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
高三化学单选题中等难度题查看答案及解析
常温下,用0.10 mol/LNaOH溶液分别滴定20.00mL浓度均为0.10mol/LCH3COOH溶液和HCN溶液,所得滴定曲线如右图所示。下列说法错误的是
A. 点①和点②所示溶液中:c(CH3COO-)>c(CN-)
B. 点③和点④所示溶液中水的电离程度:③>④
C. 点①和点②所示溶液中:c(CH3 COO-)-c(CN-)=c(HCN)-c(CH3COOH)
D. 相同条件,浓度均为0.10mol/L CH3COOH溶液和HCN溶液的导电性:CH3COOH>HCN
高三化学单选题中等难度题查看答案及解析
25°C 时,向 20 mL 0.10 mol•L-1的一元酸 HA 中逐滴加入 0.10 mol•L-1 NaOH 溶液,溶液 pH随加入 NaOH 溶液体积的变化关系如图所示。下列说法正确的是( )
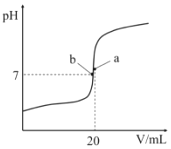
A.HA 为强酸
B.a 点溶液中,c(A-)>c(Na+)>c(H+)>c(OH-)
C.酸碱指示剂可以选择甲基橙或酚酞
D.b 点溶液中,c(Na+)=c(A-)
高三化学单选题中等难度题查看答案及解析
25°C 时,向 10 mL 0.10 mol·L-1 的 HA (Ka =1.0×10-4)中逐滴加入 0.10 mol·L-1NaOH 溶液,溶液 pH 随滴入的 V[(NaOH)aq]变化如下图所示。下列说法正确的是
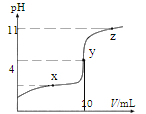
A.x 点,c(HA)> c(A-)
B.y 点,c(HA)+c(A-)=c(Na+) =0.10 mol·L-1
C.z 点,c(Na+) = c(A-) + c(OH-)
D.水的电离程度,x 点小于 y 点
高三化学单选题简单题查看答案及解析