-
氮元素可以形成许多化合物,在我们生活生产中有广泛的应用。
(1)与NF3分子互为等电子体的分子为________。
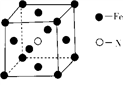
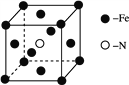
(2)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构见图甲。
写出Fe3+的基态电子排布式________。
写出该反应的化学方程式:______________。

甲 乙 丙
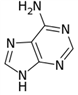
(3)维生素B4结构如图乙,则1mol维生素B4分子中含有σ键的数目为______mol。
(4)配合物丙的结构见图,丙中含有__________(填序号);
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
丙中碳原子的杂化方式有______________。
-
氮元素可以形成许多化合物,在我们生活生产中有广泛的应用。
(1) 与NF3分子互为等电子体的阴离子为________。
(2) 铁和氨气在640 ℃可发生置换反应,产物之一的晶胞结构见图。写出Fe3+的外围电子排布式:_____________,写出该反应的化学方程式:_____________。
(3) 维生素B4结构如图,则1 mol维生素B4分子中含有σ键的数目为________mol。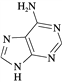
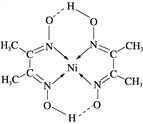
(4) 某配合物的结构如图,其中含有________(填序号);
a. 极性共价键 b. 非极性共价键 c. 配位键 d. 氢键
其中碳原子的杂化方式有________。
-
氮元素可形成卤化物,叠氮化物及配合物等许多化合物。下列说法不正确的是( )
A.NF3分子的空间构型为三角锥形
B.叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3-,则N2O与N3-互为等电子体
C.叠氮化物与Co3+等形成配合物,如:[Co(N3)(NH3)5]SO4,则其中钴的配位数为8
D.NaN3与KN3的结构类似,则NaN3的晶格能大于KN3的晶格能
-
氮元素广泛存在于自然界中,对人类生命和生活具有重要意义。含氮元素的化合物在工业生产和国防建设中都有广泛的应用。
(1)氮元素原子核外有 个未成对电子,最外层有 种能量不同的电子。PH3分子的空间构型为 ,是 分子。(填极性或非极性)
(2)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是 (填编号)
a.NH3比PH3稳定性强
b.硝酸显强氧化性,磷酸不显强氧化性
c.氮气与氢气能直接化合,磷与氢气很难直接化合
d.氮气常温是气体,磷单质是固体
亚硝酸盐是食品添加剂中急性毒性较强的物质之一,可使正常的血红蛋白变成正铁血红蛋白而失去携带氧的功能,导致组织缺氧。
(3)亚硝酸钠溶液滴加到K2Cr2O7酸性溶液中,溶液由橙色变为绿色,反应如下,补上缺项物质并配平:
Cr2O72- + NO2- + → Cr3+ + NO3-+
(4)上题反应中每消耗0.6mol NO2-,转移电子数为 。
(5)氮氧化物(NO和NO2)污染环境。若用Na2CO3溶液吸收NO2可生成CO2,9.2gNO2和Na2CO3溶液完全反应时转移电子0.1 mol,则反应的离子方程式为 。
-
硒化铜纳米晶体在光电转化中有着广泛的应用,铜和硒等元素形成的化合物在生产、生活中应用广泛。
(1)基态硒原子的核外电子排布式为______。As、Se、Br三种元素第一电离能由大到小的顺序为______。
(2)SeO2易溶解于水,熔点为340~350℃,315℃时升华,由此可判断SeO2中的化学键类型为______。
(3)Se2Cl2为深棕红色的剧毒液体,其分子结构中含有Se-Se 键,该分子中,Se原子的杂化轨道类型为______,Se2Cl2的空间构型为______ (填字母)。
a.直线形 b.锯齿形 c.环形 d.四面体形
(4)硒酸钢(CuSeO4)在电子、仪表工业中发挥着重要作用。硒酸的酸性与硫酸的比较,酸性较强的是______(填化学式)。
(5)SeO42-中Se-O的键角比SeO3的键角______(填“大“或“小“),原因是______。
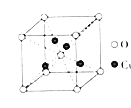
(6)铜的某种氧化物的晶胞结构如图所示,则该氧化物的化学式为______,若组成粒子氧、铜的半径分别为r(O)pm、r(Cu)pm,密度为ρg•cm-3,阿伏加德罗常数的值为NA,则该晶胞的空间利用率为______(用含π的式子表示)。
-
铁被誉为“第一金属”,铁及其化合物广泛应用于生活、生产、国防等领域。
(1)已知:元素的一个基态的气态原子得到一个电子形成-1价气态阴离子时所放出的能量称为该元素的第一电子亲和能,用E1表示。从-1价的气态阴离子再得到1个电子,成为-2价的气态阴离子所放出的能量称为第二电子亲和能E2,依此类推。FeO是离子晶体,其晶格能可通过如下的Born-Haber循环计算得到。
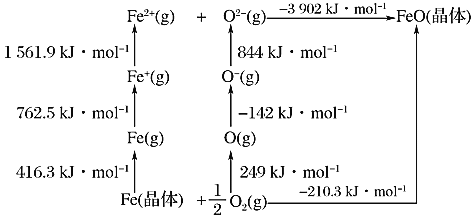
铁单质的原子化热为__________kJ/mol,FeO的晶格能为__________kJ/mol,基态O原子E1____________E2(填“大于”或“小于”),从原子结构角度解释_________。
(2)乙二胺四乙酸又叫做EDTA(图1),是化学中一种良好的配合剂,形成的配合物叫做螯合物。EDTA在配位滴定中经常用到,一般是测定金属离子的含量。已知:EDTA配离子结构(图2)。

EDTA中碳原子轨道的杂化类型为____________,EDTANa-Fe(Ⅲ)是一种螯合物,六个配位原子在空间构型为____________。EDTANa-Fe(Ⅲ)的化学键除了σ键和配位键外,还存在____________。
(3)Fe3O4晶体中,O2-的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的O 围成的正四面体空隙和如3、6、7、8、9、12的O2-围成的正八面体空隙。Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则Fe3O4晶体中,O2-数与正四面体空隙数(包括被填充的)之比为__________,有__________%的正八面体空隙填充阳离子。Fe3O4晶胞的八分之一是图示结构单元(图3),晶体密度为5.18 g/cm3,则该晶胞参数a=____________pm。(写出计算表达式)

-
I.碳元素广泛存在于自然界中,对人类生命和生活具有重要意义。含碳化合物在工业生产和国防建设中有广泛的应用。
(1)碳元素原子核外有_____个未成对电子,最外层有_____种能量不同的电子。CH4 分子的空间构型为_____,是_____分子。(填“极性”或“非极性”)
(2)碳和硅是同主族元素,下列能说明二者非金属性相对强弱的是_____(填编号)
a.CH4的稳定性比SiH4强 b.SiH4的沸点比CH4高
c.碳酸是强酸,硅酸是弱酸 d.碳原子半径比硅原子小
II.氮化硅(Si3N4)是一种重要的陶瓷材料,可用石英与焦炭在800℃氮气气氛下合成:3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)
(1)该反应的平衡常数表达式K_____。已知平衡常数:K(800℃)>K(850℃),则正反应是__________反应(填“放热”或“吸热”)
(2)任写两种能提高二氧化硅转化率的措施_____、_____。
(3)一定温度下,在2 L密闭容器内,充入一定量的反应物,5分钟时达到平衡,测得容器内气体增加了0.4mol,用CO表示该反应时间内的反应速率为_____。
-
金属镍及其化合物在合金材料以及催化剂等方面应用广泛。
(1)基态Ni原子的价电子(外围电子)排布式为 ;
(2)金属镍能与CO形成配合物Ni(CO)4,写出与CO互为等电子体的一种分子和一种离子的化学式 、 ;
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应。
如①CH2=CH2、②HC≡CH、③ 、④HCHO,其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形;
、④HCHO,其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形;
(4)Ni2+和Fe2+的半径分别为69 pm和78 pm,则熔点NiO FeO(填“<”或“>”);
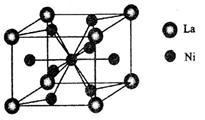
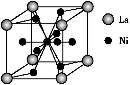
(5)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如下图所示。该合金的化学式为 ;
-
Ⅰ.金属镍及其化合物在合金材料以及催化剂等方面应用广泛。
(1)基态镍原子的价电子(外围电子)排布式为 。
(2)金属镍能与CO形成配合物Ni(CO)4,写出与CO互为等电子体的一种分子和一种离子的化学式 、 。
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应。
如①CH2 CH2、②HC≡CH、③
CH2、②HC≡CH、③ 、④HCHO,其中碳原子采取sp2杂化的分子有________ (填物质序号),HCHO分子的立体结构为 形。
、④HCHO,其中碳原子采取sp2杂化的分子有________ (填物质序号),HCHO分子的立体结构为 形。
(4)Ni2+和Fe2+的半径分别为69 pm和78 pm,则熔点NiO FeO(填“<”或“>”)。
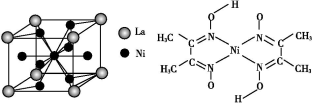
(5)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为 。
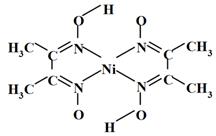
(6)丁二酮肟常用于检验Ni2+:在稀氨水中,丁二酮肟与Ni2+反应生成鲜红色沉淀,其结构如右下图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用箭头和“…”表示出配位键和氢键。
-
I、金属镍及其化合物在合金材料以及催化剂等方面应用广泛。
(1)基态Ni原子的价电子(外围电子)排布式为 ________;
(2)金属镍能与CO形成配合物Ni(CO)4,写出与CO互为等电子体的一种分子和一种离子的化学式________、________;
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应。
如①CH2=CH2、②HC≡CH、③
 、④HCHO其中碳原子采取sp2杂化的分子有
、④HCHO其中碳原子采取sp2杂化的分子有
________(填物质序号),HCHO分子的立体结构为形;
(4)Ni2+和Fe2+的半径分别为69 pm和78 pm,则熔点NiO________FeO
(填“<”或“>”);
(5)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为 ________;
(6)丁二酮肟常用于检验Ni2+:在稀氨水中,丁二酮肟与Ni2+反应生成鲜红色沉淀,其结构如右下图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用箭头和“…”表示出配位键和氢键。