-
铅(Pb)的原子序数为82,有+2、+4两种常见化合价。PbO2随温度的升高发生如下变化:PbO2→Pb2O3→Pb3O4→PbO。下列说法不正确的是
A. Pb位于周期表ⅣA族
B. Pb3O4可以写成2PbO·PbO2
C. PbO2分解生成Pb2O3同时生成O2
D. PbO2可作为铅蓄电池的正极,放电时发生氧化反应
高三化学单选题中等难度题查看答案及解析
-
已知:Pb的化合价只有+2、+4,且+4价的Pb具有强氧化性,能氧化浓HCl生成Cl2;PbO2不稳定,随温度升高按下列顺序逐步分【解析】
PbO2→Pb2O3→Pb3O4→PbO.现将a mol PbO2加热分解,收集产生的O2;向加热后所得固体中加入足量的浓盐酸,收集产生的Cl2.加热反应后所得固体中,Pb2+占Pb元素的物质的量分数为x;两步反应中收集的O2和Cl2的物质的量之和为y mol.
试回答下列问题:
(1)试写出Pb2O3与浓盐酸反应的化学方程式______.
(2)用含X与a的表达式表示产生的O2、Cl2的物质的量n(O2)=______ n(Cl2)=______
(3)写出y与a、x的函数关系式.______
(4)若两步反应中O2和Cl2的物质的量之比为5:3,则剩余固体中含有的物质为______;其物质的量之比为______.高三化学解答题中等难度题查看答案及解析
-
已知:Pb的化合价只有+2、+4,且+4价的Pb具有强氧化性,能氧化浓HCl生成C12;PbO2不稳定,随温度升高按下列顺序逐步分【解析】
PbO2→Pb2O3→Pb3O4→PbO。现将a mol PbO2加热分解,收集产生的O2;加热反应后所得固体中,Pb2+占Pb元素的物质的量分数为x;向加热后所得固体中加入足量的浓盐酸,收集产生的C12。两步反应中收集的O2和C12的物质的量之和为y mol。
试回答下列问题:
(1)Fe3O4可写成FeO·Fe2O3的形式,如果将Pb3O4也写成相对应的形式应为___________。
(2)试写Pb2O3与浓盐酸反应的化学方程式_________________________________。
(3)通过计算确定y与a、x的函数关系式___________________________。
高三化学填空题困难题查看答案及解析
-
已知Pb3O4与HNO3溶液发生反应Ⅰ:Pb3O4+4H+=PbO2+2Pb2++2H2O;PbO2与酸化的MnSO4溶液发生反应Ⅱ:5PbO2+2Mn2++4H++5SO42-=2MnO4-+5PbSO4+2H2O。下列推断正确的是( )
A. 由反应Ⅰ可知,Pb3O4中Pb(Ⅱ)和Pb(Ⅳ)含量之比为2:1
B. 由反应Ⅰ、Ⅱ可知,氧化性:HNO3>PbO2>MnO4-
C. Pb可与稀硝酸发生反应:3Pb+16HNO3=3Pb(NO3)4+4NO↑+8H2O
D. Pb3O4可与盐酸发生反应:Pb3O4+8HCl=3PbCl2+4H2O+Cl2↑
高三化学多选题简单题查看答案及解析
-
四氧化三铅(Pb3O4,也可写作2PbO·PbO2)俗名“铅丹”或“红丹”,可用作防锈剂。工业上以废旧铅酸电池的铅膏(主要成分是PbSO4和PbO2)为原料制备Pb3O4的流程如下:
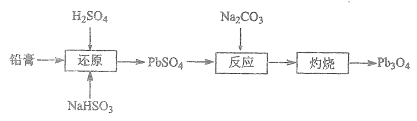
(1)“还原”时的化学方程式为__________。
(2)已知: Ksp[PbCO3]=1.5×10-13。 若使溶液中Pb2+的浓度小于1×10-5 mol/L,此时溶液中的c(CO32-)>_____mol/L。
(3)为测定某样品四氧化三铅含量,称取样品0.1200g,加入足量的6 mol/LHNO3充分溶解,过滤,得到含Pb2+的滤液和PbO2固体。将固体PbO2连同滤纸一并置于另一只锥形瓶中,加入足量的醋酸和醋酸钠混合溶液,再加入过量KI,使PbO2充分氧化I-,以淀粉溶液作指示剂,用0.01000mol/L Na2S2O3溶液滴定,终点时用去30.00mL。已知:I2+ 2 Na2S2O3 = Na2S4O6 + 2NaI。
①所加KI必须过量,原因是_____________________________。
②计算试样中Pb3O4的质量分数____________。(写出计算过程)
高三化学综合题中等难度题查看答案及解析
-
铅的单质、氧化物、盐在现代工业中有着重要用途。
Ⅰ.(1)铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化物PbO2、类似Fe3O4 的Pb3O4,Pb3O4 与HNO3 发生非氧化还原反应生成一种盐和一种铅氧化物,其反应的化学方程式为_____________。
Ⅱ.以含铅废料(主要含Pb、PbO、PbO2、PbSO4)为原料制备高纯PbO,其主要流程如下:
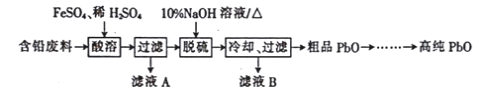
(2)“酸溶”时,在Fe2+催化下,Pb 和PbO2反应生成PbSO4生成1mol PbSO4转移电子的物质的量为____________mol 。
(3)已知:①PbO溶解在NaOH 溶液中,存在平衡:PbO(s)+NaOH(aq)
NaHPbO2(aq),其溶解度曲线如图所示:
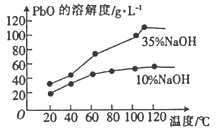
②粗品PbO 中所含杂质不溶于NaOH 溶液。
结合上述信息,完成由粗品PbO得到高纯PbO 的操作:将粗品PbO溶解在一定量__________(填“35%”或“10%”)的NaOH 溶液中,加热至110℃,充分溶解后,__________,将滤液冷却结晶,过滤、洗涤并干燥得到高纯PbO 固体。
(4)将PbO粗品溶解在HCl 和NaCl 的混合溶液中,得到含Na2PbCl2 的电解液,电解Na2PbCl4 溶液生成Pb 的装置如图所示。
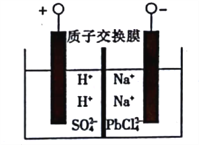
①阴极的电极反应式为_______________________。
②电解一段时间后,Na2PbCl4浓度极大减小,为了恢复其浓度且实现物质的循环利用,阴极区采取的方法是_________________________。
高三化学综合题中等难度题查看答案及解析
-
铅的单质、氧化物、盐在现代工业中有着重要用途。
Ⅰ.(1)铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化物PbO2、类似Fe3O4 的Pb3O4,Pb3O4 与HNO3 发生非氧化还原反应生成一种盐和一种铅氧化物,其反应的化学方程式为_____________。
Ⅱ.以含铅废料(主要含Pb、PbO、PbO2、PbSO4)为原料制备高纯PbO,其主要流程如下:
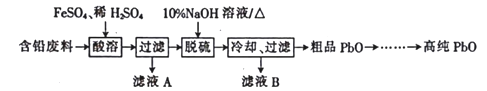
(2) “酸溶”时,在Fe2+催化下,Pb 和PbO2反应生成PbSO4生成1mol PbSO4转移电子的物质的量为____________mol 。
(3)已知:①PbO溶解在NaOH 溶液中,存在平衡:PbO(s)+NaOH(aq)
NaHPbO2(aq),其溶解度曲线如图所示:
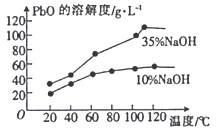
②粗品PbO 中所含杂质不溶于NaOH 溶液。
结合上述信息,完成由粗品PbO得到高纯PbO 的操作:将粗品PbO溶解在一定量__________(填“35%”或“10%”)的NaOH 溶液中,加热至110℃,充分溶解后,___________(填“趁热过滤”或“蒸发浓缩”),将滤液冷却结晶,过滤、洗涤并干燥得到高纯PbO 固体。
(4)将PbO粗品溶解在HCl 和NaCl 的混合溶液中,得到含Na2PbCl2 的电解液,电解Na2PbCl4 溶液生成Pb 的装置如图所示。
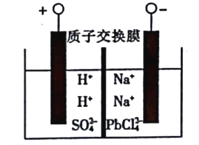
①阴极的电极反应式为_______________________。
②电解一段时间后,Na2PbCl4浓度极大减小,为了恢复其浓度且实现物质的循环利用,阴极区采取的方法是_________________________。
高三化学综合题简单题查看答案及解析
-
铅的单质、氧化物、盐在现代工业中有着重要用途。
I.(1)铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化物PbO2、类似Fe3O4的Pb3O4。Pb3O4 与HNO3发生非氧化还原反应生成一种盐和一种铅氧化物,其反应的化学方程式为_____________________________。
II.以含铅废料(主要含Pb、PbO、PbO2、PbSO4)为原料制务高纯PbO,其主要流程如下:
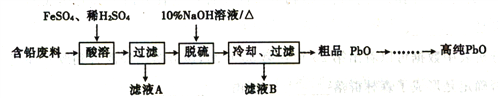
(2)“酸溶”时,在Fe2+催化下,Pb和PbO2反应生成1molPbSO4 时转移电子的物质的量为____mol。
(3)已知:PbO溶解在NaOH溶液中,存在平衡:PbO(s) +NaOH(aq)=NaHPbO2(aq),其溶解度曲线如图所示:

结合上述信息,完成由粗品PbO(所含杂质不溶于NaOH溶液)得到高纯PbO的操作:将粗品PbO溶解在一定量_________(填“35%”或“10%”)的NaOH 溶液中,加热至110℃,充分溶解后,___________(填“趁热过滤”或“蒸发浓缩”),将滤液冷却结晶,过滤、洗涤并干燥得到高纯PbO固体。
(4)工业上利用硫化氢除去滤液A 中少量的Pb2+,发生的反应为Pb2++H2S
PbS↓+2H+,该反应的平衡常数为_____________。(H2S的Ka1=1.5×10-7,Ka2=7.0×10-15,PbS的Ksp=8.4×10-28)
(5)将粗品PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示:

①阴极的电极反应式为________________________;
②当有2.07gPb生成时,通过质子交换膜的n(H+)=______________。
高三化学综合题中等难度题查看答案及解析
-
铅的单质、氧化物、盐在现代工业中有着重要用途。
Ⅰ.(1)铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化物PbO2、类似Fe3O4的Pb3O4,Pb3O4与HNO3发生非氧化还原反应生成一种盐和一种铅氧化物,其反应的化学方程式为___________________。
Ⅱ.以含铅废料(主要含Pb、PbO、PbO2、PbSO4)为原料制备高纯PbO,其主要流程如下:
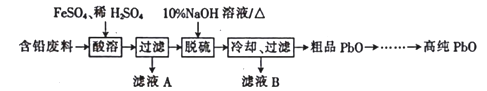
(2)“酸溶”时,在Fe2+催化下,Pb和PbO2反应生成PbSO4生成1mol PbSO4转移电子的物质的量为______mol。
(3)已知:①PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)
NaHPbO2(aq),其溶解度曲线如图所示:
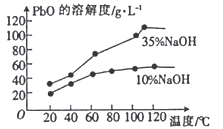
②粗品PbO中所含杂质不溶于NaOH溶液。结合上述信息,完成由粗品PbO得到高纯PbO的操作:将粗品PbO溶解在一定量__________(填“35%”或“10%”)的NaOH溶液中,加热至110℃,充分溶解后,___________(填“趁热过滤”或“蒸发浓缩”),将滤液冷却结晶,过滤、洗涤并干燥得到高纯PbO固体。
(4)将PbO粗品溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl2的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。
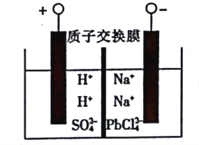
①阴极的电极反应式为_______________________。
②电解一段时间后,Na2PbCl4浓度极大减小,为了恢复其浓度且实现物质的循环利用,阴极区采取的方法是_________________________。
高三化学综合题简单题查看答案及解析
-
用足量的CO还原13.7 g某铅氧化物,把生成的CO2全部通入到过量的澄清石灰水中,得到的沉淀干燥后质量为8.0g,则此铅氧化物的化学式是( )
A.PbO B.Pb2O3 C.Pb3O4 D.PbO2
高三化学选择题简单题查看答案及解析