硒是人体必需的微量元素,右图是硒在周期表中的信息,关于硒元素的说法错误的是

A. 位于第四周期
B. 质量数为34
C. 原子最外层有6个电子
D. 相对原子质量为78.96
高三化学单选题中等难度题
硒是人体必需的微量元素,右图是硒在周期表中的信息,关于硒元素的说法错误的是

A. 位于第四周期
B. 质量数为34
C. 原子最外层有6个电子
D. 相对原子质量为78.96
高三化学单选题中等难度题
硒是人体必需的微量元素,右图是硒在周期表中的信息,关于硒元素的说法错误的是

A. 位于第四周期
B. 质量数为34
C. 原子最外层有6个电子
D. 相对原子质量为78.96
高三化学单选题中等难度题查看答案及解析
硒(Se)是人体健康必需的一种微量元素,已知Se的原子结构示意图如图: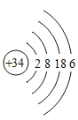 。下列说法不正确的是( )
。下列说法不正确的是( )
A. 该原子的质量数为34 B. 该元素处于第四周期第ⅥA族
C. SeO2既有氧化性又有还原性 D. 酸性:HClO4>H2SeO4
高三化学单选题简单题查看答案及解析
硒(Se)是人体健康必需的一种微量元素。已知Se的原子结构示意图为: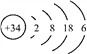 下列说法不正确的是
下列说法不正确的是
A. 该原子的质量数为34 B. 该元素处于第四周期第ⅥA族
C. SeO2既有氧化性又有还原性 D. 酸性:HBrO4 > H2SeO4
高三化学单选题简单题查看答案及解析
有机锗具有抗肿瘤活性,锗元素的部分信息如右图,则下列说法错误的是
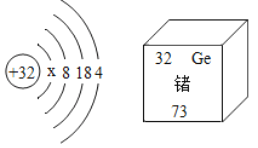
A.在元素周期表中锗元素与硫元素位于同一族 B.x=2
C.锗原子的核外电子数为32 D.锗原子的中子数为41
高三化学单选题简单题查看答案及解析
硒及其化合物在工农业生产中有重要用途,硒也是人体必需的微量元素。
(1)硒(34Se)在周期表中位于硫下方,画出其原子结构示意图_____________。
(2)氧族元素单质均能与H2反应生成H2X,用原子结构解释原因_______________。
(3)298K、1.01×l0-5Pa,O2、S、Se、Te分别与H2化合的反应热数据如图所示。写出Se与H2化合的热化学反应方程式__________________。
(4)可以从电解精炼铜的阳极泥中提取硒,通过化学工艺得到亚硒酸钠等含硒物质。常温下,Se(Ⅳ)溶液中各组分的物质的量分数随pH变化曲线如图。
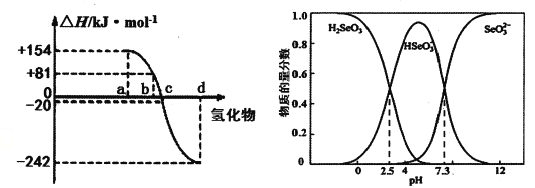
①向亚硒酸溶液滴入NaOH溶液至pH =5,该过程中主要反应的离子方程式________。
②在pH<0的酸性环境下,向Se(Ⅳ)体系中通入SO2制得单质Se的化学方程式是_______。
③下列说法正确的是____(填字母序号)。
a.NaHSeO3溶液显酸性
b.pH=8时,溶液中存在c(HAsO3-)+2c(SeO32-)+c(OH-)=c(H+)
c.在Na2SeO3溶液中,c(SeO32-》c(HSeO3-)> c(H2SeO3)
④常温下,H2SeO3的第二步电离平衡常数为K2,计算K2=________。
高三化学综合题中等难度题查看答案及解析
下列关于原子结构及元素周期表的说法错误的是
A.位于同一轨道内电子的运动状态也不相同
B.位于 d 区和 ds 区的元素都是金属元素
C.前四周期未成对电子数最多的元素位于ⅥB 族
D.基态原子最外层电子排布为ns1 的元素均在ⅠA 族或ⅠB 族
高三化学单选题中等难度题查看答案及解析
铟产业被称为“信息时代的朝阳产业”。元素周期表中铟的数据见图,下列说法完全正确的是
A.铟元素的质量数是114.8
B.铟元素的相对原子质量是115,中子数为66
C.铟元素是一种主族元素,位于第五周期第ⅢA族
D.铟原子最外层有3个能量相同的电子
高三化学单选题中等难度题查看答案及解析
已知有位于元素周期表前四周期的元素X、Y、Z、T、W、Q,其部分信息如下表:
| X | 宇宙中含量最丰富的元素 |
| Y | 植物生长所必需的三种营养元素中,电负性最大的 |
| Z | 原子最外层电子数是其电子层数的3倍 |
| Q | 其气态氢化物与其低价氧化物常温下能反应,生成该元素的单质 |
| T | 最高正价与最低负价代数和为6,其单质能与强碱溶液反应制消毒液 |
| W | 其+2价阳离子的价电子排布为3d9 |
请回答下列问题:
(1)W元素位于周期表的第___周期___族,W2+能与X、Y形成的简单分子结合生成一种深蓝色的离子,其离子符号为___。
(2)X与Z按原子个数比为1:1组合得到的一种物质甲,它能用于杀菌消毒,物质甲的电子式为___;Q与T也能按原子个数比为1:1组合,得到一种暗黄色的液体乙,其结构与甲相似,则乙中存在的化学键类型有___和___;乙遇水发生歧化反应,得到一种淡黄色的固体和两种具有刺激性气味的气体,该反应的化学反应方程式为___。
(3)元素Q的简单离子半径___元素T的简单离子半径(填“>”“<”或“=”);元素T能形成多种含氧酸:HTO、HTO2、HTO3、HTO4,其酸性由强到弱的顺序为___(用化学式表示)。
高三化学推断题中等难度题查看答案及解析
A、D、E、W是中学常见的四种元素,原子序数依次增大,A的原子最外层电子数是次外层的2倍,D的氧化物属于两性氧化物,D、E位于同周期,A、D、E的原子最外层电子数之和为14,W是人体必需的微量元素,缺乏W会导致贫血症状。
(1)A在元素周期表中的位置是____________。
(2)下列事实能用元素周期律解释的是(填字母序号)________。
a. D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b. E的气态氢化物的稳定性小于HF
c. WE3的溶液可用于刻蚀铜制的印刷电路板
(3)E的单质可以从NaBr溶液中置换出Br2单质,从原子结构的角度解释其原因是____________。
(4)①工业上用电解法制备D的单质,反应的化学方程式为____________。
②家用“管道通”的有效成分是烧碱和D的单质,使用时需加入一定量的水,此时发生反应的化学方程式为________。
(5)W的单质可用于处理酸性废水中的NO3-,使其转换为NH4+,同时生成有磁性的W的氧化物X,再进行后续处理。上述反应的离子方程式为____________。
高三化学填空题中等难度题查看答案及解析
A、D、E、W是中学常见的四种元素,原子序数依次增大,A的原子最外层电子数是次外层的2倍,D的氧化物属于两性氧化物,D、E位于同周期,A、D、E的原子最外层电子数之和为14,W是人体必需的微量元素,缺乏W会导致贫血症状。
(1)A在元素周期表中的位置是____________。
(2)下列事实能用元素周期律解释的是(填字母序号)________。
a. D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b. E的气态氢化物的稳定性小于HF
c. WE3的溶液可用于刻蚀铜制的印刷电路板
(3)E的单质可以从NaBr溶液中置换出Br2单质,从原子结构的角度解释其原因是____________。
(4)①工业上用电解法制备D的单质,反应的化学方程式为____________。
②家用“管道通”的有效成分是烧碱和D的单质,使用时需加入一定量的水,此时发生反应的化学方程式为________。
(5)W的单质可用于处理酸性废水中的NO3-,使其转换为NH4+,同时生成有磁性的W的氧化物X,再进行后续处理。上述反应的离子方程式为____________。
高三化学填空题中等难度题查看答案及解析