-
氯化亚铜是一种重要的化工原料,一种利用低品位铜矿 主要含有Cu2S、CuS、FeO、Fe2O3、SiO2等
主要含有Cu2S、CuS、FeO、Fe2O3、SiO2等 为原料制取CuCl的工艺流程如下:
为原料制取CuCl的工艺流程如下:

(1)反应Ⅰ“浸取”前需将铜矿粉碎的目的是___________________________;
(2)滤渣Ⅰ的成分除S和 外还含有___________,反应 Ⅰ中
外还含有___________,反应 Ⅰ中 的作用为_______________
的作用为_______________
(3)已知生成氢氧化物的pH如下表,则反应Ⅱ“中和”时,用氨水调pH的范围是______________。
(4)检验滤液Ⅱ中是否含有 所需要的试剂是:______________
所需要的试剂是:______________
(5)①反应Ⅲ中生成难溶 的离子方程式:______________
的离子方程式:______________
②反应Ⅳ所对应的化学方程式:______________________________
(6) CuCl的定量分析
步骤1.取样品0.7500g和30.0mL 1.0mol·L-1过量的FeCl3溶液置于250mL的锥形瓶中,不断摇动。
步骤2.待样品溶解后,平均分为3份,用0.1000mol·L-1 Ce(SO4)2标准溶液进行滴定。
三次实验测得数据如下表
已知: ;
; 。
。
①数据处理:计算得CuCl的纯度为_________
②误差下列操作会使测定结果偏高的是______________
A.锥形瓶中有少量蒸馏水
B.滴定终点读数时仰视滴定管刻度线
C.0.1000mol·L-1硫酸铈溶液久置后浓度变小
D.滴定前滴定管尖嘴无气泡,滴定后产生气泡
E.用量筒取10.0mL 1.0mol·L-1的 溶液时仰视刻度线
溶液时仰视刻度线
-
氯化亚铜是一种重要的化工原料,一种利用低品位铜矿 主要含有Cu2S、CuS、FeO、Fe2O3、SiO2等
主要含有Cu2S、CuS、FeO、Fe2O3、SiO2等 为原料制取CuCl的工艺流程如下:
为原料制取CuCl的工艺流程如下:
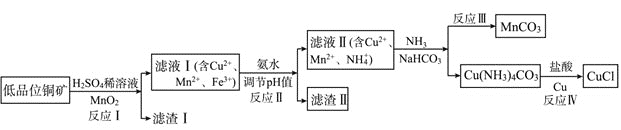
(1)反应Ⅰ“浸取”前需将铜矿粉碎的目的是___________________________;
(2)滤渣Ⅰ的成分除S和 外还含有___________,反应 Ⅰ中
外还含有___________,反应 Ⅰ中 的作用为_______________
的作用为_______________
(3)已知生成氢氧化物的pH如下表,则反应Ⅱ“中和”时,用氨水调pH的范围是______________。
(4)检验滤液Ⅱ中是否含有 所需要的试剂是:______________
所需要的试剂是:______________
(5)①反应Ⅲ中生成难溶 的离子方程式:______________
的离子方程式:______________
②反应Ⅳ所对应的化学方程式:______________________________
(6) CuCl的定量分析
步骤1.取样品0.7500g和30.0mL 1.0mol·L-1过量的FeCl3溶液置于250mL的锥形瓶中,不断摇动。
步骤2.待样品溶解后,平均分为3份,用0.1000mol·L-1 Ce(SO4)2标准溶液进行滴定。
三次实验测得数据如下表
已知: ;
; 。
。
①数据处理:计算得CuCl的纯度为_________
②误差下列操作会使测定结果偏高的是______________
A.锥形瓶中有少量蒸馏水
B.滴定终点读数时仰视滴定管刻度线
C.0.1000mol·L-1硫酸铈溶液久置后浓度变小
D.滴定前滴定管尖嘴无气泡,滴定后产生气泡
E.用量筒取10.0mL 1.0mol·L-1的 溶液时仰视刻度线
溶液时仰视刻度线
-
氯化亚铜是一种重要的化工原料,广泛应用于有机合成、石油、油脂、染料等工业。一种利用低品位铜矿(Cu2S、CuS及FeO和Fe2O3等)为原料制取CuCl的工艺流程如下:
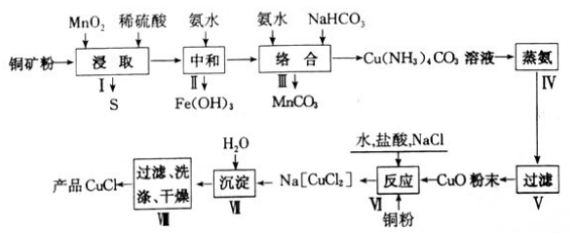
回答下列问题:
(1)步骤Ⅰ“浸取”前需将铜矿粉碎的目的是______________;“浸取”时,被氧化的元素有________(填元素符号)
(2)已知Cu2+、Mn2+、Fe3+开始生成沉淀和沉淀完全的pH如下表,则步骤Ⅱ“中和”时,pH应控制的范围为_______________。
| 物质 | Cu(OH)2 | Mn(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 4.7 | 8.3 | 1.2 |
| 完全沉淀pH | 6.7 | 9.8 | 3.2 |
(3)步骤IV加热“蒸氨”时发生反应的化学方程式为________________。
(4)步骤VI反应的离子方程式为______________,其中盐酸需过量,其原因是________________。
(5)步骤Ⅶ获得CuCl晶体需经过滤、洗涤、干燥。洗涤时,常有无水乙醇代替蒸馏水做洗涤剂的优点是______________(写一点)。
-
CuCl是生产印刷颜料酞菁蓝的重要原料,工业上可用一种低品位铜矿(主要成分CuS、Cu2S、CuO、Fe2O3、FeO 及其他非酸溶性杂质)和软锰矿(主要成分为MnO2 和其他非酸溶性杂质)来进行生产,过程如下:
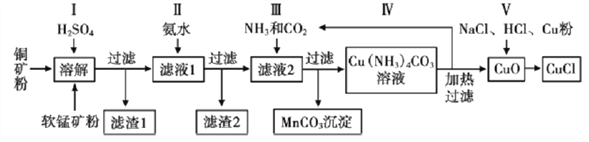
回答下列问题:
(1)步骤Ⅰ中反应较多,下列反应是其中之一:Cu2S+2MnO2+4H2SO4=2CuSO4+2MnSO4+4H2O+S, 该反应的氧化产物为____________________(填化学式)。
(2)为确定滤液1中是否含有Fe2+,首先用有机萃取剂除去溶液中MnSO4,再取下层水溶液进行检测,所用试剂为_____________________。
(3)步骤Ⅱ加入氨水控制溶液的pH 为5左右,目的是______________________。
(4)为模拟步骤Ⅲ的生产过程,某同学设计如下实验,下列有关叙述正确的是_____________。
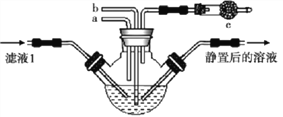
A.a 通入CO2,然后b 通入NH3;c中放碱石灰
B.b通入NH3,然后a通入CO2;c中放碱石灰
C.a通入NH3,然后b 通入CO2;c中放蘸稀硫酸的脱脂棉
D.b通入CO2,然后a 通入NH3;c中放蘸稀硫酸|的脱脂棉
(5)步骤Ⅳ的滤液中主要成分X 是步骤Ⅱ和步骤Ⅲ都有的产物,可以回收作为肥料使用, 该肥料_______( 填“可以”或“不可以”)与草木灰(有效成分K2CO3) 共用,简述原因:__________。
(6)已知CuCl 为难溶于水的白色沉淀,写出步骤Ⅴ发生反应的离子方程式:_____________。
-
CuCl是生产印刷颜料酞菁蓝的重要原料,工业上可用一种低品位铜矿(主要成分CuS、Cu2S、CuO、Fe2O3、FeO 及其他非酸溶性杂质)和软锰矿(主要成分为MnO2 和其他非酸溶性杂质)来进行生产,过程如下:
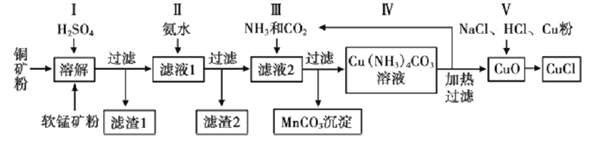
回答下列问题:
(1)步骤Ⅰ中反应较多,下列反应是其中之一:Cu2S+2MnO2+4H2SO4=2CuSO4+2MnSO4+4H2O+S, 该反应的氧化产物为____________________(填化学式)。
(2)为确定滤液1中是否含有Fe2+,首先用有机萃取剂除去溶液中MnSO4,再取下层水溶液进行检测,所用试剂为_____________________。
(3)步骤Ⅱ加入氨水控制溶液的pH 为5左右,目的是______________________。
(4)为模拟步骤Ⅲ的生产过程,某同学设计如下实验,下列有关叙述正确的是_____________。
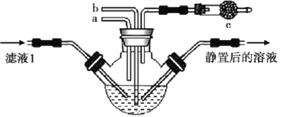
A.a 通入CO2,然后b 通入NH3;c中放碱石灰
B.b通入NH3,然后a通入CO2;c中放碱石灰
C.a通入NH3,然后b 通入CO2;c中放蘸稀硫酸的脱脂棉
D.b通入CO2,然后a 通入NH3;c中放蘸稀硫酸|的脱脂棉
(5)步骤Ⅳ的滤液中主要成分X 是步骤Ⅱ和步骤Ⅲ都有的产物,可以回收作为肥料使用, 该肥料_______( 填“可以”或“不可以”)与草木灰(有效成分K2CO3) 共用,简述原因:__________。
(6)已知CuCl 为难溶于水的白色沉淀,写出步骤Ⅴ发生反应的离子方程式:_____________。
-
氯化亚铜广泛应用于有机合成、石油、油脂、染料等工业。以某种铜矿粉(含Cu2S、CuS及FeS等)为原料制取CuCl的工艺流程如下:
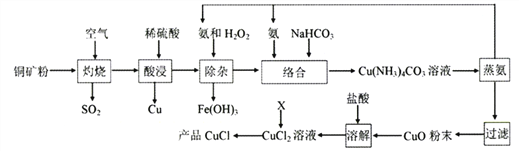
已知:①CuS、Cu2S、FeS灼烧固体产物为Cu2O、FeO;
②Ksp(CuCl)= 2×10-7,2Cu+= Cu+Cu2+的平衡常数K1= 1×106
回答下列问题:
(1)“灼烧”时,被还原的元素有____________(填元素符号)。
(2)“酸浸”所需H2SO4是用等体积的98% H2SO4和水混合而成。实验室配制该硫酸溶液所需的玻璃仪器除玻璃棒、胶头滴管外,还有_______。“酸浸”时硫酸不宜过多的原因是__________________。
(3)“除杂”的总反应方程式是_____________________。
(4)“络合”反应中的NH3与NaHCO3理论比值是____________________。
(5)加热“蒸氨”在减压条件下进行的原因是________________。
(6)X 可以充分利用流程中的产物,若X 是SO2时,通入CuCl2溶液中反应的离子方程式是________________;若X 是Cu时,反应Cu+Cu2++2Cl-= 2CuCl 的平衡常数K2=_________。
(7)以铜为阳极电解NaCl溶液也可得到CuCl,写出阳极电极反应式__________________。
-
氯化亚铜广泛应用于有机合成、石油、油脂、染料等工业。以某种铜矿粉(含Cu2S、CuS及FeS等)为原料制取CuCl的工艺流程如下:
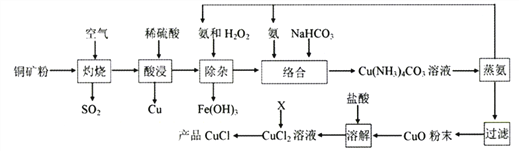
已知:①CuS、Cu2S、FeS灼烧固体产物为Cu2O、FeO;
②Ksp(CuCl)= 2×10-7,2Cu+= Cu+Cu2+的平衡常数K1= 1×106
回答下列问题:
(1)“灼烧”时,被还原的元素有____________(填元素符号)。
(2)“酸浸”所需H2SO4是用等体积的98% H2SO4和水混合而成。实验室配制该硫酸溶液所需的玻璃仪器除玻璃棒、胶头滴管外,还有_______。“酸浸”时硫酸不宜过多的原因是__________________。
(3)“除杂”的总反应方程式是_____________________。
(4)“络合”反应中的NH3与NaHCO3理论比值是____________________。
(5)加热“蒸氨”在减压条件下进行的原因是________________。
(6)X 可以充分利用流程中的产物,若X 是SO2时,通入CuCl2溶液中反应的离子方程式是________________;若X 是Cu时,反应Cu+Cu2++2Cl-= 2CuCl 的平衡常数K2=_________。
(7)以铜为阳极电解NaCl溶液也可得到CuCl,写出阳极电极反应式__________________。
-
辉铜矿石主要含有硫化亚铜(Cu2S),还含有FeO、CaO、SiO2等。以辉铜矿石为原料制备CuCl2·2H2O的工艺流程如图所示:
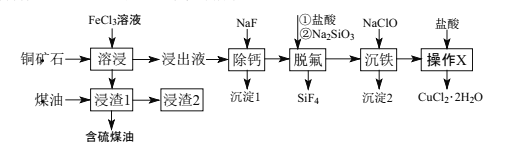
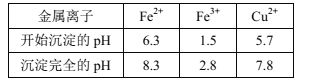
已知:Ⅰ.金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
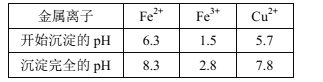
Ⅱ.NaCl易溶于水,不溶于酒精,随温度变化溶解度变化不明显;CuCl2·H2O易溶于水,酒精,浓氨水,随温度升高溶解度变化明显增大。
Ⅲ.Ksp(CaF2)=4.0×10-11
(1)为了提高“溶浸”效率,可采取的措施是___。写出“溶浸”过程中Cu2S溶解时离子方程式:___。
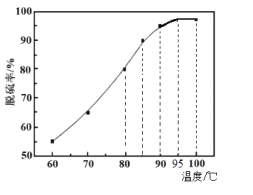
(2)“脱硫”时,随着温度的升高,脱硫率呈上升趋势(如图),原因是___。
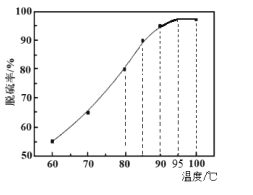
(3)写出“脱氟”时HF发生反应的化学方程式:___。
(4)“沉铁”过程中,加入NaClO的两个作用是___。
(5)“操作X”的具体操作是___。
(6)经过“操作X”后,母液经过一系列操作可得到另外一种物质,要得到这种纯净物,最好选用下列试剂洗涤___。
A.浓盐酸 B.水 C.酒精 D.浓氨水
(7)向“浸出液”中加入NaF除去溶液中Ca2+(浓度为1.0×10-3mol·L-1),当溶液中c(F-)=2.0×10-3mol·L-1时,除钙率为___。
-
辉铜矿石主要含有硫化亚铜(Cu2S),还含有FeO、CaO、SiO2等。以辉铜矿石为原料制备CuCl2·2H2O的工艺流程如图所示:
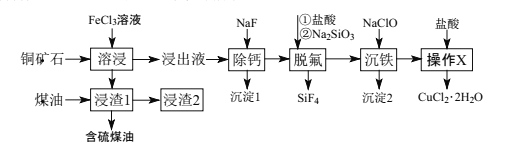
已知:Ⅰ.金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
Ⅱ.NaCl易溶于水,不溶于酒精,随温度变化溶解度变化不明显;CuCl2·H2O易溶于水,酒精,浓氨水,随温度升高溶解度变化明显增大。
Ⅲ.Ksp(CaF2)=4.0×10-11
(1)为了提高“溶浸”效率,可采取的措施是___。写出“溶浸”过程中Cu2S溶解时离子方程式:___。
(2)“脱硫”时,随着温度的升高,脱硫率呈上升趋势(如图),原因是___。
(3)写出“脱氟”时HF发生反应的化学方程式:___。
(4)“沉铁”过程中,加入NaClO的两个作用是___。
(5)“操作X”的具体操作是___。
(6)经过“操作X”后,母液经过一系列操作可得到另外一种物质,要得到这种纯净物,最好选用下列试剂洗涤___。
A.浓盐酸 B.水 C.酒精 D.浓氨水
(7)向“浸出液”中加入NaF除去溶液中Ca2+(浓度为1.0×10-3mol·L-1),当溶液中c(F-)=2.0×10-3mol·L-1时,除钙率为___。
-
氯化亚铜广泛应用于有机合成。工业上以低品位铜矿(主要含CuS、Fe2O3、SiO2)为原料,
制备氯化亚铜的生产工艺如下:
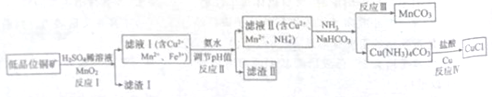
(1)CuS中Cu的化合价为_____________。
(2)滤渣Ⅰ的成分除S之外还有__________,反应Ⅰ中MnO2的作用是______________
(3)已知生成氢氧化物的pH如下表:
| 沉淀物 | Fe(OH)3 | Mn(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.7 | 8.3 | 4.2 |
| 完全沉淀的pH | 3.2 | 9.8 | 6.7 |
则反应Ⅱ中用氨水调节pH值的范围是________________。
(4)检验滤液Ⅱ中是否含有Fe3+的试剂是____________。
(5)请用化学用语回答:
①反应中Ⅲ生成难溶MnCO3的离子方程式_____________;
②反应Ⅳ素所对应的化学方程式____________________。
(6)氯化亚铜的定量分析:
步骤Ⅰ.称取0.2500g的样品和10.0mL 1.0mol/L的FeCl3溶液置于250mL锥形瓶中,不断摇动;
步骤Ⅱ.待样品溶解后,加水10.0mL和3滴指示剂;
步骤Ⅲ.用0.1000mol/L CeOSO4标准溶液滴至终点,并记录读数。重复实验两次,测得数据如下:
| 序号 | 1 | 2 | 3 |
| 起始读数 | 0.95mL | 0.70mL | 1.00mL |
| 终点读数 | 20.95mL | 24.95mL | 21.00mL |
已知:CuCl+FeCl3=CuCl2+FeCl2 Fe2++Ce4+=Fe3++Ce3+
①数据处理:计算CuCl纯度________________;
②误差分析:下列操作会使滴定结果偏高的是__________________。
A.锥形瓶中有少量蒸馏水
B.滴定终点读数时仰视滴定管刻度线,其他操作正确
C.0.1000mol/L CeOSO4溶液久置后浓度变小
D.滴定前滴定管尖嘴有气泡,滴定后气泡消失
E.所取FeCl3溶液体积偏大
主要含有Cu2S、CuS、FeO、Fe2O3、SiO2等
为原料制取CuCl的工艺流程如下:

外还含有___________,反应 Ⅰ中
的作用为_______________
所需要的试剂是:______________
的离子方程式:______________
;
。
溶液时仰视刻度线














