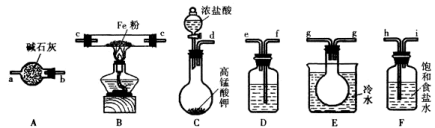-
无水三氯化铬 为紫色单斜晶体,极易潮解和升华,常用作其他铬盐的合成原料。某课题小组利用
为紫色单斜晶体,极易潮解和升华,常用作其他铬盐的合成原料。某课题小组利用 浅绿色粉末
浅绿色粉末 、木炭粉和
、木炭粉和 制备无水
制备无水 并测定其纯度,制备时用到的实验装置如下。
并测定其纯度,制备时用到的实验装置如下。
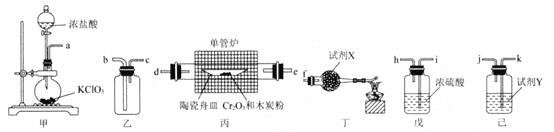
请回答下列问题:
 上述装置的连接顺序为
上述装置的连接顺序为 ________
________ 填装置接口处的小写字母
填装置接口处的小写字母 。
。
 试剂X、Y可分别选用下列试剂中的________、________
试剂X、Y可分别选用下列试剂中的________、________ 填序号
填序号 。装置丁中酒精灯的作用是________。
。装置丁中酒精灯的作用是________。
 溶液
溶液  无水
无水
 碱石灰
碱石灰  酸性
酸性 溶液
溶液  饱和食盐水
饱和食盐水
 装置乙中使用粗导管的原因为________。
装置乙中使用粗导管的原因为________。
 装置丙中发生反应的化学方程式为________。
装置丙中发生反应的化学方程式为________。
 实验结束后,装置乙中的实验现象为________。
实验结束后,装置乙中的实验现象为________。
 测定样品中三氯化铬的含量。
测定样品中三氯化铬的含量。
称取 样品溶于水配制成
样品溶于水配制成 溶液,取
溶液,取 所得溶液于锥形瓶中,加入
所得溶液于锥形瓶中,加入 的
的 溶液,充分反应后,加入指示剂,用
溶液,充分反应后,加入指示剂,用 的
的 标准溶液滴定至终点时,消耗标准溶液的体积为
标准溶液滴定至终点时,消耗标准溶液的体积为 已知:
已知: 、
、 。
。
 该样品中
该样品中 的质量分数为________
的质量分数为________ 计算结果精确到
计算结果精确到 。
。
 若滴定至终点时,发现滴定管尖嘴处有气泡,则测定结果________
若滴定至终点时,发现滴定管尖嘴处有气泡,则测定结果________ 填“偏高”“偏低”或“无影响”
填“偏高”“偏低”或“无影响” 。
。
-
无水三氯化铬(CrCl3)为紫色晶体,在工业上主要用作媒染剂和催化剂,某化学小组用Cr2O3和CCl4在高温下制备无水三氯化铬,部分实验装置如图所示。
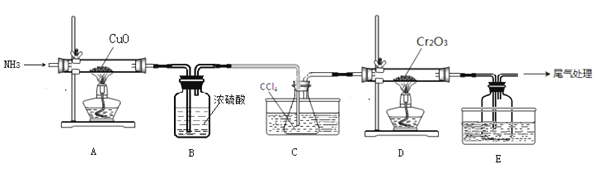
已知:①CrCl3熔点为83℃,易潮解,易升华,易溶于水但不易水解,高温下易被氧气氧化;②Cr2O3和CCl4在高温下反应的产物为CrCl3和光气(COCl2 )。请回答下列问题:
(1)装置A是氮气制备装置,氮气的作用是____________。
(2)装置B的作用为________。装置C和装置E的水槽中应分别盛有__________、____________。
(3)装置D中生成CrCl3和光气(COCl2 )的化学方程式为_________。
(4)该实验装置有设计不合理的地方,请写出改进方法:_________(写一点即可)
(5)产品中CrCl3质量分数的测定:
(i)称取0.3000 g得到的CrCl3样品溶于水并于250mL容量瓶中定容。
(ii)取25.00mL样品溶液于带塞的锥形瓶中,加热至沸腾后加入稍过量的Na2O2,稀释并加热煮沸,再加入过量的H2SO4酸化,将Cr3+氧化为Cr2O72-;再加入过量的KI固体,加塞摇匀,使铬完全以Cr3+形式存在
(iii)加入1mL指示剂,用0.0250 mol·L-1标准Na2S2O3溶液滴定至终点,平行测定三次,平均消耗标准Na2S2O3溶液21.00mL(已知2Na2S2O3+I2= Na2S4O6+2NaI)
①ii中加入稍过量的Na2O2后要加热煮沸,其主要原因是____________;加入KI发生反应的离子方程式为________________
②滴定实验可选用的指示剂为____________产品中CrCl3质量分数为_______%(结果保留两位有效数字)
-
无水三氯化铬(CrCl3)为紫色晶体,在工业上主要用作媒染剂和催化剂,某化学小组用Cr2O3和CCl4在高温下制备无水三氯化铬,部分实验装置如图所示。
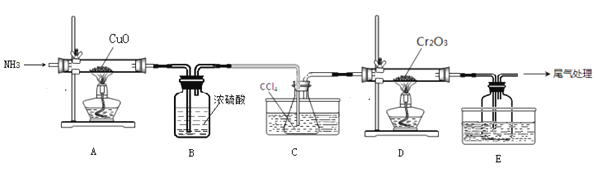
已知:①CrCl3熔点为83℃,易潮解,易升华,易溶于水但不易水解,高温下易被氧气氧化;②Cr2O3和CCl4在高温下反应的产物为CrCl3和光气(COCl2 )。请回答下列问题:
(1)装置A是氮气制备装置,氮气的作用是____________。
(2)装置B的作用为________。装置C和装置E的水槽中应分别盛有__________、____________。
(3)装置D中生成CrCl3和光气(COCl2 )的化学方程式为_________。
(4)该实验装置有设计不合理的地方,请写出改进方法:_________(写一点即可)
(5)产品中CrCl3质量分数的测定:
(i)称取0.3000 g得到的CrCl3样品溶于水并于250mL容量瓶中定容。
(ii)取25.00mL样品溶液于带塞的锥形瓶中,加热至沸腾后加入稍过量的Na2O2,稀释并加热煮沸,再加入过量的H2SO4酸化,将Cr3+氧化为Cr2O72-;再加入过量的KI固体,加塞摇匀,使铬完全以Cr3+形式存在
(iii)加入1mL指示剂,用0.0250 mol·L-1标准Na2S2O3溶液滴定至终点,平行测定三次,平均消耗标准Na2S2O3溶液21.00mL(已知2Na2S2O3+I2= Na2S4O6+2NaI)
①ii中加入稍过量的Na2O2后要加热煮沸,其主要原因是____________;加入KI发生反应的离子方程式为________________
②滴定实验可选用的指示剂为____________产品中CrCl3质量分数为_______%(结果保留两位有效数字)
-
无水三氯化铬(CrCl3)为紫色晶体,在工业上主要用作媒染剂和催化剂,某化学小组用Cr2O3和CCl4在高温下制备无水三氯化铬,部分实验装置如图所示。
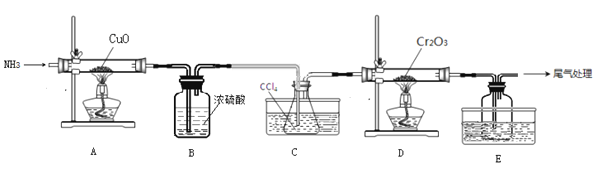
已知:①CrCl3熔点为83℃,易潮解,易升华,易溶于水但不易水解,高温下易被氧气氧化;②Cr2O3和CCl4在高温下反应的产物为CrCl3和光气(COCl2 )。请回答下列问题:
(1)装置A是氮气制备装置,氮气的作用是____________。
(2)装置B的作用为________。装置C和装置E的水槽中应分别盛有__________、____________。
(3)装置D中生成CrCl3和光气(COCl2 )的化学方程式为_________。
(4)该实验装置有设计不合理的地方,请写出改进方法:_________(写一点即可)
(5)产品中CrCl3质量分数的测定:
(i)称取0.3000 g得到的CrCl3样品溶于水并于250mL容量瓶中定容。
(ii)取25.00mL样品溶液于带塞的锥形瓶中,加热至沸腾后加入稍过量的Na2O2,稀释并加热煮沸,再加入过量的H2SO4酸化,将Cr3+氧化为Cr2O72-;再加入过量的KI固体,加塞摇匀,使铬完全以Cr3+形式存在
(iii)加入1mL指示剂,用0.0250 mol·L-1标准Na2S2O3溶液滴定至终点,平行测定三次,平均消耗标准Na2S2O3溶液21.00mL(已知2Na2S2O3+I2= Na2S4O6+2NaI)
①ii中加入稍过量的Na2O2后要加热煮沸,其主要原因是____________;加入KI发生反应的离子方程式为________________
②滴定实验可选用的指示剂为____________产品中CrCl3质量分数为_______%(结果保留两位有效数字)
-
无水氯化铝是一种重要的化工原料,某研究性学习小组查阅资料后利用图1所示装置制备无水氯化铝(反应温度为450℃-500℃)。资料显示:氯化铝为无色透明晶体或白色而微带浅黄色的结晶性粉末,在178℃ 升华,在空气中能吸收水分,发生水解。
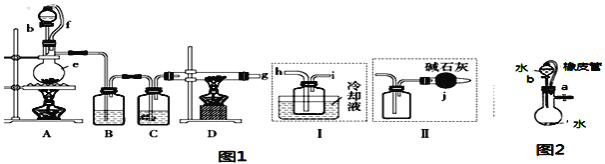
回答下列问题:
(1)某同学检验装置A部分的气密性,如图2所示,关闭图装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:A部分装置是否漏气?____________ (填“漏气”、“不漏气”或“无法确定”),判断理由:________________________。
(2)装置e的名称是_______________________。
(3)某学习小组设计了以下两种实验方案:方案甲:g接装置I;方案乙:g接装置II。但是甲乙两个方案中虚线内装置均有不足之处,请你评价后填写下表。
| 方案 | 不足之处 |
| 甲 | ______ |
| 乙 | ______ |
(4)在上述(3)的评价基础上,请设计一个合理方案:______________________。
(5)A部分装置中发生反应生成氯气的离子方程式为___________________________,若生成标准状况下的氯气22.4L,需要10mol·L-1的浓盐酸的体积______400mL(填大于、小于或等于)。
-
无水氯化铝是一种重要的化工原料,某研究性学习小组查阅资料后利用图1所示装置制备无水氯化铝(反应温度为450℃-500℃)。资料显示:氯化铝为无色透明晶体或白色而微带浅黄色的结晶性粉末,在178℃ 升华,在空气中能吸收水分,发生水解。
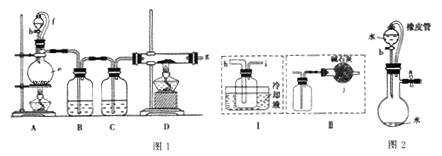
回答下列问题:
(1)某同学检验装置A部分的气密性,如图2所示,关闭图装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:A部分装置是否漏气?____________ (填“漏气”、“不漏气”或“无法确定”),判断理由:____________。
(2)装置e的名称是_______________,装置B的作用是____________。
(3)某学习小组设计了以下两种实验方案:方案甲:g接装置I;方案乙:g接装置II。但是甲乙两个方案中虚线内装置均有不足之处,请你评价后填写下表。
| 方案 | 不足之处 |
| 甲 | ____________ |
| 乙 | ____________ |
(4)在上述(3)的评价基础上,请设计一个合理方案:_________________。
(5)A部分装置中发生反应生成氯气的离子方程式为______________,若生成标准状况下的氯气22.4L,需要10mol·L-1的浓盐酸的体积______400mL(填大于、小于或等于)。
-
无水三氯化铬 在工业上主要用作媒染剂和催化剂。某化学小组在氮气的氛围下用
在工业上主要用作媒染剂和催化剂。某化学小组在氮气的氛围下用 和
和 在高温下制备无水三氯化铬,并测定所制得产品中三氯化铬的质量分数。
在高温下制备无水三氯化铬,并测定所制得产品中三氯化铬的质量分数。
实验原理:
已知:① 熔点为83℃,易潮解,易升华,易溶于水,高温下易被氧气氧化;
熔点为83℃,易潮解,易升华,易溶于水,高温下易被氧气氧化;
② 沸点为57.6℃;
沸点为57.6℃;
③在碱性条件下, 能把
能把 氧化为
氧化为 ;
;
在酸性条件下, 能把
能把 还原为
还原为 。
。
回答下列问题:
Ⅰ.氮气的制备
(1)利用工业氮气(混有 、
、 、
、 )制取纯净干燥的氮气的实验装置如图1。按气流方向(用小写字母表示)写出其合理的连接顺序:a→________。
)制取纯净干燥的氮气的实验装置如图1。按气流方向(用小写字母表示)写出其合理的连接顺序:a→________。
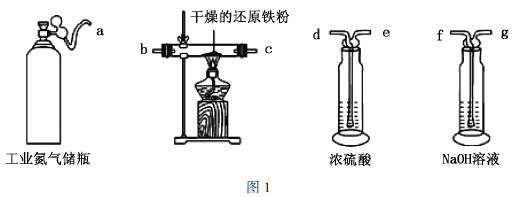
Ⅱ.无水三氯化铬的制备
实验装置如图2所示(加热、夹持等装置已略去)。
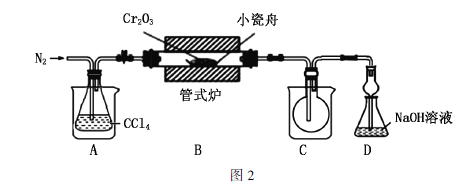
(2)通入 的作用是_____________(写出2点)。
的作用是_____________(写出2点)。
(3)装置A和装置C的烧杯中分别盛放________、________。
(4)制备 时生成的气体
时生成的气体 (俗称光气)有毒,
(俗称光气)有毒, 遇水发生水解,反应方程式为
遇水发生水解,反应方程式为 。为了防止污染环境,用足量的NaOH溶液吸收光气,其化学方程式为________________。
。为了防止污染环境,用足量的NaOH溶液吸收光气,其化学方程式为________________。
(5)图2装置中有设计不合理的地方,你认为应该改进的措施有______________。
Ⅲ.产品中 质量分数的测定
质量分数的测定
a.称取
 产品,在强碱性条件下,加入过量的30%
产品,在强碱性条件下,加入过量的30% 溶液,小火加热使
溶液,小火加热使 完全转化为
完全转化为 ,继续加热一段时间;
,继续加热一段时间;
b.冷却后加适量的蒸馏水,再滴入适量的浓 和浓
和浓 ,使
,使 转化为
转化为 ;
;
c.用新配制的 硫酸亚铁铵标准溶液滴至橙红色变浅(反应原理:
硫酸亚铁铵标准溶液滴至橙红色变浅(反应原理: ),加入5滴二苯胺磺酸钠指示剂,继续滴定至溶液由紫蓝色转变为亮绿色且半分钟内不变色即为终点。重复实验3次,平均消耗标准溶液18.00mL。
),加入5滴二苯胺磺酸钠指示剂,继续滴定至溶液由紫蓝色转变为亮绿色且半分钟内不变色即为终点。重复实验3次,平均消耗标准溶液18.00mL。
回答下列问题:
(6)①上述操作a中“继续加热一段时间”的目的是________。
②加浓 的目的是为了防止指示剂提前变色。若不加浓
的目的是为了防止指示剂提前变色。若不加浓 ,则测得的
,则测得的 的质量分数将________(填“偏低”、“偏高”或“不变”)。
的质量分数将________(填“偏低”、“偏高”或“不变”)。
③产品中 的质量分数为________%(保留一位小数)。
的质量分数为________%(保留一位小数)。
-
无水FeCl3呈棕红色,在空气中极易潮解100℃左右时升华,工业上常用作有机合成催化剂。某学习小组利用下图装置(夹持仪器略去)制备并收集无水FeCl3。
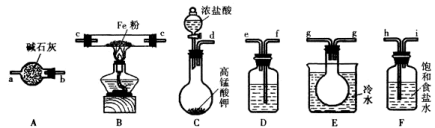
请回答:
(1)按气流方向各装置依次连接的合理顺序为 (填仪器接口的字母编号)
(2)连接好各装置进行实验,实验步骤如下:检查装置气密性后,装入药品, (请按正确的顺序填入下列步骤的序号)。
①加热Fe粉反应一段时间 ②打开分液漏斗活塞通一段时间气体
③关闭分液漏斗活塞 ④停止加热,充分冷却
(3)装置A的作用为 。
(4)装置C中反应的化学方程式为 。
(5)装置D中盛有的试剂为 (写名称);装置E 中冷水浴的作用为 。
(6)从实验安全考虑,整套装置存在一处明显不足,请指出 。
-
无水 是一种重要的化工原料。某课外探究小组尝试制取无水
是一种重要的化工原料。某课外探究小组尝试制取无水 ,查阅资料获得下列信息:无水
,查阅资料获得下列信息:无水 在
在 升华,极易潮解,遇到水蒸气会产生白色烟雾。
升华,极易潮解,遇到水蒸气会产生白色烟雾。
探究一 无水 的实验室制备
的实验室制备
利用如图装置,用干燥、纯净的氯气在加热条件下与铝粉 已除去氧化膜
已除去氧化膜 反应制取无水AlCl3。供选择的药品:①铝粉 ②浓硫酸 ③稀盐酸 ④饱和食盐水 ⑤二氧化锰粉末 ⑥无水氯化钙 ⑦稀硫酸 ⑧浓盐酸 ⑨氢氧化钠溶液
反应制取无水AlCl3。供选择的药品:①铝粉 ②浓硫酸 ③稀盐酸 ④饱和食盐水 ⑤二氧化锰粉末 ⑥无水氯化钙 ⑦稀硫酸 ⑧浓盐酸 ⑨氢氧化钠溶液
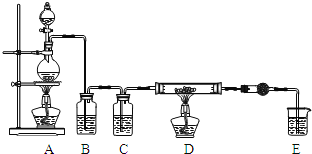
(1)写出装置A烧瓶中发生的反应方程式 ______ 。
(2)实验开始前,先检查装置气密性,然后装入药品,接下来的步骤依次是 ______  填序号
填序号 。
。
 加热D中硬质玻璃管
加热D中硬质玻璃管
 往A烧瓶中加入液体
往A烧瓶中加入液体
 点燃A中的酒精灯
点燃A中的酒精灯
(3)上述供选药品中本实验无需用到的是 ______  填数字序号
填数字序号 。
。
(4)写出无水 与水蒸气反应的化学方程式 ______ 。
与水蒸气反应的化学方程式 ______ 。
探究二 无水 的含量测定及结果分析
的含量测定及结果分析
取D中反应后所得固体 ,与足量氢氧化钠溶液反应,测定生成气体的体积
,与足量氢氧化钠溶液反应,测定生成气体的体积 体积均换算成标准状况
体积均换算成标准状况 ,重复测定三次,数据如下:
,重复测定三次,数据如下:
| 第一次实验 | 第二次实验 | 第三次实验 |
| D中固体用量 | 
| 
| 
|
| 氢气的体积 | 
| 
| 
|
(5)根据表中数据,计算所得固体中无水 的质量分数 ______ 。
的质量分数 ______ 。
(6)有同学认为测得的无水 的质量分数偏低,你认为可能的原因有 ______ 。
的质量分数偏低,你认为可能的原因有 ______ 。
探究三 离子浓度对氯气制备的影响
二氧化锰粉末和浓盐酸的反应随着盐酸的浓度降低,反应停止不再产生氯气。探究小组对盐酸浓度降低影响氯气生成的原因进行如下探究:
(7)提出假设 假设1: 浓度降低影响氯气的生成
浓度降低影响氯气的生成
假设2: ______ 。
(8)设计方案进行实验。限选试剂:浓 、NaCl固体、
、NaCl固体、 固体、稀盐酸。
固体、稀盐酸。
| 步骤 | 实验操作 | 预测现象和结论 |
| 
| 往不再产生氯气的装置中,加入 ______ ,继续加热 | 若有黄绿色气体生成,则假设1成立 |
| 
| ______ | 若有黄绿色气体生成,则假设2成立 |
-
某实验小组利用氯气与金属铁反应制备无水三氯化铁,经查阅资料得知:无水FeCl3在空气中易潮解,加热到100℃左右时易升华。下图是两个学生设计的实验装置,左边的反应装置相同,而右边的产品收集装置不同,分别如(I)和(Ⅱ)所示,试回答:
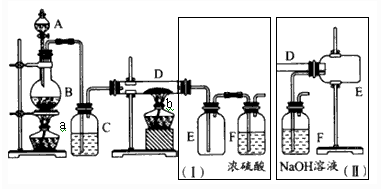
(1)B中反应的离子方程式为__ __;
(2)实验中a与b两个酒精灯应先点燃 ,目的是 ;
(3)收集装置(Ⅰ)的主要缺点是: ;装置(Ⅱ)也有缺点,必须采取的改进措施是:___ _。
(4)b酒精灯加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管D右端,要使沉积的FeCl3 进入收集器,操作是 。
(5)实验中还缺少一个除杂装置,目的是除去 ;应选择 做除杂剂。
A.饱和NaHCO3 B.水 C.饱和食盐水 D.NaOH溶液
为紫色单斜晶体,极易潮解和升华,常用作其他铬盐的合成原料。某课题小组利用
浅绿色粉末
、木炭粉和
制备无水
并测定其纯度,制备时用到的实验装置如下。

上述装置的连接顺序为
________
填装置接口处的小写字母
。
试剂X、Y可分别选用下列试剂中的________、________
填序号
。装置丁中酒精灯的作用是________。
溶液
无水
碱石灰
酸性
溶液
饱和食盐水
装置乙中使用粗导管的原因为________。
装置丙中发生反应的化学方程式为________。
实验结束后,装置乙中的实验现象为________。
测定样品中三氯化铬的含量。
样品溶于水配制成
溶液,取
所得溶液于锥形瓶中,加入
的
溶液,充分反应后,加入指示剂,用
的
标准溶液滴定至终点时,消耗标准溶液的体积为
已知:
、
。
该样品中
的质量分数为________
计算结果精确到
。
若滴定至终点时,发现滴定管尖嘴处有气泡,则测定结果________
填“偏高”“偏低”或“无影响”
。