原电池是将_____能转化成_____能的一种装置。一种利用原电池原理制备NH3的装置如图所示,陶瓷在高温时可以传输H+。该设备中,电极____(填“a”或“b”)作负极,其电极反应式为:_____。当电路中通过1.2mol的电子时,可生成NH3____mol。
高二化学综合题中等难度题
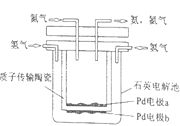
原电池是将_____能转化成_____能的一种装置。一种利用原电池原理制备NH3的装置如图所示,陶瓷在高温时可以传输H+。该设备中,电极____(填“a”或“b”)作负极,其电极反应式为:_____。当电路中通过1.2mol的电子时,可生成NH3____mol。

高二化学综合题中等难度题
原电池是将_____能转化成_____能的一种装置。一种利用原电池原理制备NH3的装置如图所示,陶瓷在高温时可以传输H+。该设备中,电极____(填“a”或“b”)作负极,其电极反应式为:_____。当电路中通过1.2mol的电子时,可生成NH3____mol。

高二化学综合题中等难度题查看答案及解析
一种电化学制备NH3的装置如图所示,图中陶瓷在高温时可以传输H+。下列叙述错误的是

A.Pd电极b为阴极
B.阴极的反应式为:N2+6H++6e−2NH3
C.H+由阳极向阴极迁移
D.陶瓷可以隔离N2和H2
高二化学单选题困难题查看答案及解析
下列关于电化学的说法中错误的是( )
A.原电池的负极、电解池的阳极均发生氧化反应
B.原电池将化学能转化为电能,电解池将电能转化为化学能
C.利用原电池原理可制备化学电源,利用电解池原理可制备化学物质
D.电解水制取H2和O2时,为了增强导电性,可加入NaCl、H2SO4
高二化学单选题简单题查看答案及解析
(12分)氯碱工业是高耗能产业,为了提高原料的利用率,将电解的Y气体作为燃料电池燃料,为电解池供电;X气体作为钛的冶炼原料,在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中氯碱工业装置中的电极未标出,所用的离子交换膜只允许阳离于通过。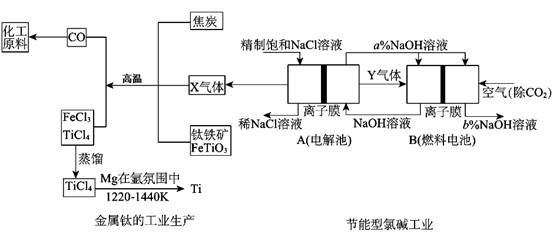
(1)①上图中的节能型氯碱工业部分,X、Y分别是________ 、________ (填化学式),分析比较图示中NaOH质量分数a%与b%的大小 ________;
②写出燃料电池B中正极上发生的电极反应: ________;
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式 ________;
(3) TiCl4暴露在潮湿空气中冒白烟,白烟主要为白色的二氧化钛的水合物H2TiO3,写出该反应的化学方程式________;
(4)已知:①Mg(s)+Cl2(g)=MgCl2(s) △H=-641kJ·mol-1。
②1/2Ti(s)+ Cl2(g) =1/2TiCl4(1) △H=-385 kJ·mol-1。
则2Mg(s)+TiCl4(1)=2MgCl2(s)+Ti(s)的反应热为________
高二化学填空题中等难度题查看答案及解析
用如图所示装置,可由乙二醛制备乙二酸,反应原理为OHC-CHOHOOC-COOH
下列说法正确的是
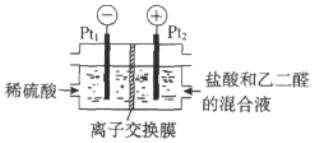
A. 该装置利用上述反应将化学能转化为电能
B. 电极的反应式为
C. 盐酸除增强溶液导电性的作用,还提供参与电极反应
D. 理论上每得到乙二酸,将有
从右室迁移到左室
高二化学单选题困难题查看答案及解析
膜技术原理在化工生产中有着广泛的应用。有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5,装置图如下。
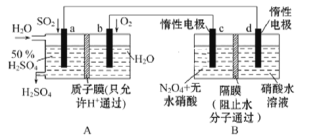
(1)A装置是________(填“原电池”或“电解池”),A装置中通入SO2一极的电极反应式为________________________________________。
(2)N2O5在电解池的________(填“c极”或“d极”)区生成,其电极反应式为____________。
高二化学填空题中等难度题查看答案及解析
膜技术原理在化工生产中有着广泛的应用。有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5,装置图如下。
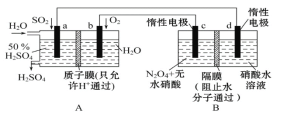
(1)A装置是__________,B装置是_____________(填“原电池”或“电解池”)。
(2)N2O5在电解池的_____(填“c极”或“d极”)区生成,其电极反应式为______________。
(3)A装置中通入O2的一极是____极,其电极反应式为_________________;通入SO2的一极是_____极,其电极反应式为_________________。
高二化学填空题中等难度题查看答案及解析
全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示。下列说法不正确的是


A.放电过程中右槽溶液颜色逐渐由紫色变为绿色
B.放电过程中氢离子的作用之一是参与正极反应
C.充电过程中左槽溶液逐渐由蓝变黄
D.充电时若转移的电子数为3.011023个,左槽溶液中n(H+)的变化量为1mol
高二化学单选题中等难度题查看答案及解析
全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图1所示.
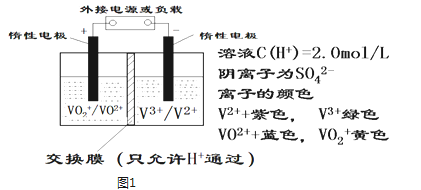
①当左槽溶液逐渐由黄变蓝,其电极反应式为 ___ .
②充电过程中,右槽溶液颜色逐渐___ 色变为___ 色.
③放电过程中氢离子的作用是___ ___ ;充电时若转移的电子数为3.01×1023个,左槽溶液中n(H+)的变化量为 ___ .
(1)若负载是镀铜的电镀槽,则纯铜应该连接___ 槽(填左或右)中的电极.
(2)若负载是用石墨作电极,用3mol/L KCl和0.5mol/L Al2(SO4)3的混合溶液作电解液的电解池时,图2电解变化的曲线合理的是___
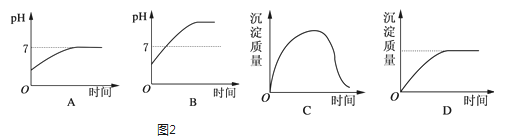
(3)电解法处理污水已经得到广泛的应用.若负载是酸性介质中将有毒的Cr2O72﹣转变为Cr3+的电解池.装置如图3所示,请用文字描述其工作原理___
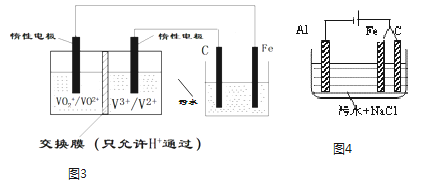
(4)若负载是进行三电极法污水处理的电解池原理如图4所示,增加的铁电极的可能作用是___
高二化学综合题困难题查看答案及解析
电解NO制备NH4NO3的工作原理如图所示,X、Y均为Pt电极,为使电解产物全部转化为NH4NO3,需补充物质A。下列说法正确的是( )

A.物质A为HNO3
B.X电极为阳极
C.利用该装置电解2molNO理论上可生成1.25molNH4NO3
D.Y电极反应式为NO-3e-+4OH-=NO3-+2H2O
高二化学单选题中等难度题查看答案及解析