-
请按要求回答下列问题:
(1)25 ℃时,向纯水中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为_____________,由水电离出的c(OH-)=________mol·L-1。
(2)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25 ℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25 ℃时,有等pH的a.NaCN溶液、b.Na2CO3溶液和c.CH3COONa溶液,三溶液的浓度由大到小的顺序为___________________________。(用a b c表示)
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为_________。
(3)室温时,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
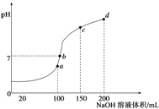
试分析图中a、b、c、d四个点,水的电离程度最大的是________;在b点,溶液中各离子浓度由大到小的排列顺序是_____________________________。
-
请按要求回答下列问题:
(1)纯水在100℃时pH=6,该温度下1mol·L-1的NaOH溶液中,由水电离出的c(OH-)=__mol·L-1。
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为__,由水电离出的c(OH-)=___mol·L-1。
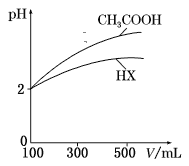
(3)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离常数___(填“大于”“小于”或“等于”)CH3COOH的电离常数。理由是___。
(4)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25℃时,有等pH的a.NaCN溶液、b.Na2CO3溶液和c.CH3COONa溶液,三溶液的浓度由大到小的顺序为___。(用a、b、c表示)
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为___。
③25℃时,等浓度的HCN和NaCN混合溶液显___性。(酸、碱、中)
(5)室温时,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
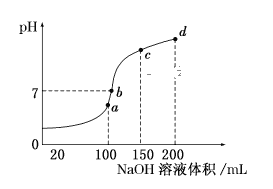
试分析图中a、b、c、d四个点,水的电离程度最大的是__;在b点,溶液中各离子浓度由大到小的排列顺序是__。
-
下列说法中,正确的是
A.一定温度下,向纯水中加入少量盐酸,[H+]增大,Kw将增大
B.25℃时,将pH=9的烧碱溶液稀释1000倍所得到的溶液,PH=6
C.25℃时,水的离子积常数Kw为1×10﹣14mol2•L﹣2
D.100℃时,纯水的pH=6,此时溶液呈酸性
-
下列说法中,正确的是
A.一定温度下,向纯水中加入少量盐酸,[H+]增大,Kw将增大
B.25℃时,将pH=9的烧碱溶液稀释1000倍所得到的溶液,PH=6
C.25℃时,水的离子积常数Kw为1×10﹣14mol2•L﹣2
D.100℃时,纯水的pH=6,此时溶液呈酸性
-
在25 ℃时,向纯水中加入少量的KHSO4固体,则( )
A.溶液c(H+)减小 B.水的离子积常数Kw减小
C.水的电离平衡向正方向移动 D.溶液的c(OH-)减小
-
水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在100℃时,pH=6,该温度下0.1mol•L-1的NaOH溶液中,溶液的pH= .
(2)25℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为 , 由水电离出的c(OH-)= mol·L-1.
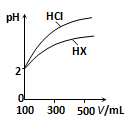
(3)体积均为100mL、pH均为2的盐酸与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX是 (填“强酸”或“弱酸”),理由是 .
-
下列叙述中,错误的是( )
A. 虽然固体氯化钠不能导电,但氯化钠是电解质
B. 纯水的pH随温度的升高而减小
C. 在醋酸钠溶液中加入少量氢氧化钠,溶液中c(OH-)增大
D. 在纯水中加入少量硫酸铵,可抑制水的电离
-
(8分)按要求回答下列问题:
(1)NaHCO3的电离方程式是 。
(2)FeCl3水解的离子方程式是 。
(3)硫代硫酸钠(Na2S2O3)溶液与稀硫酸反应的化学方程式是 。
(4)将TiCl4加入热水中生成TiO2.xH2O的化学方程式是 。
-
(1)室温时纯水中c(H+)=c(OH-),向纯水中加入少量下列固体物质:
A.NaOH B.Na2SO4 C.NH4Cl
试回答如下问题:
I.溶液中H+、OH-浓度变化情况(填“变大”“减小”或“不变”)
II. c(H+)与c(OH-)大小比较(填“>”“<”或“=”)
III.溶液的酸碱性(填“酸性”“碱性”或“中性”)
请按上述要求补完整表中相关内容
| A.NaOH | a Na2SO4 | C.NH4C1 |
| c(H+) | 减少 | ①________ | 增大 |
| c(OH-) | ②_______ | 不变 | ③_____ |
| c(H+)与c(OH-)的大小比较 | ④_______ | = | > |
| 溶液的酸碱性 | 碱性 | ⑤_______ | 酸性 |
(2)己知25℃合成氨反应中,1 mol N2完全转化为NH3时释放的能量为92.4 kJ。X现将1 molN2和3 mol H2混合置于2 L密闭容器中,反应进行到2 s末测得NH3为0.4mol。试回答:
①该反应的热化学方方程式为 ________________________。
②该反应达到平衡后,升髙温度平衡向_____(填“正”或“逆”)反应方向移动;增大压强平衡向_____ (填“正”或“逆”)反应方向移动;加入催化剂平衡________(填“能”或“不能”)移动。
③前2 s内v(H2)为_____________。
-
(10分)现有25℃时0.1 mol/L的氨水。请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中 (增大、减小、不变)
(增大、减小、不变)
(2)若向氨水中加入稀硫酸,使其恰好中和,写出反应的离子方程式:
所得溶液的pH 7(填“>”“<”或“=”)。
(3)若向该氨水中加入氢氧化钠固体,则该电离平衡向 方向移动(分子化、离子化),电离平衡常数 。(增大、减小或不变)



