-
(8分)按要求回答下列问题:
(1)NaHCO3的电离方程式是 。
(2)FeCl3水解的离子方程式是 。
(3)硫代硫酸钠(Na2S2O3)溶液与稀硫酸反应的化学方程式是 。
(4)将TiCl4加入热水中生成TiO2.xH2O的化学方程式是 。
高二化学填空题中等难度题查看答案及解析
-
请按照下列要求回答问题:
(1)硫化钠水解的离子方程式:______。
(2)浓的Al2(SO4)3溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理______。
(3)将25℃下pH=12的Ba(OH)2溶液a L与pH=1的HCl溶液b L混合,若所得混合液为中性,则a:b=_____。(溶液体积变化忽略不计)。
(4)pH=3的NH4Cl溶液,由水电离出的c(H+)=__。
(5)常温时,Fe(OH)3的溶度积常数Ksp=1×10-38,要使溶液中的Fe3+沉淀完全(残留的c(Fe3+)<10-5 mol·L-1),则溶液的pH应大于____。
(6)用如图装置进行模拟电解NO2气体实验,可回收硝酸。
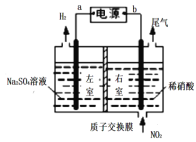
①外接电源a极为_____极,左室发生的电极反应式为_______。
②若有标准状况下2.24 LNO2被吸收,通过质子交换膜(只允许质子通过)的H+为__mol。
(7)在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。

①Ag2CrO4的Ksp为______。
②由Y点变到Z点的方法______。
高二化学综合题中等难度题查看答案及解析
-
下列化学反应式书写正确的是
A.制取氢氧化铁胶体的化学方程式为FeCl3+3H2O
Fe(OH)3(胶体)+3HCl
B.亚硫酸在溶液中的电离方程式为H2SO
2H++SO32-
C.NaHCO3水解的离子方程式为HCO3-+H2O
CO32-+H3O+
D.电子工业印刷电路反应式为2Fe3++Cu=Cu2++2Fe2+
高二化学选择题中等难度题查看答案及解析
-
下列化学反应式书写正确的是( )
A. 制取氢氧化铁胶体的化学方程式为FeCl3+3H2O
Fe(OH)↓+3HCl
B. 亚硫酸在溶液中的电离方程式为H2SO3
2H++SO32-
C. NaHCO3 水解的离子方程式为HCO3-+H2O
CO32-+ H3O+
D. 泡沫灭火器工作原理离子方程式为Al3++3HCO3-=3CO2↑+Al(OH)3↓
高二化学null简单题查看答案及解析
-
(1)根据氯化铁溶液回答下列问题:
①向FeCl3溶液中加入少量NaHCO3。产生的现象为___。用离子方程式表示其原因___。
②不断加热FeCl3溶液蒸干其水分并灼烧,得到的固体是___。
③在配制FeCl3溶液时,为防止溶液变浑浊,应加入___。
(2)利用反应Cu+H2O2+H2SO4=CuSO4+2H2O设计一个原电池,回答下列问题:
①负极材料为___;正极反应式为___。
②反应过程中SO
向____极移动。
③当电路中转移0.1mol电子时,电解液质量(不含电极)增加了___克。
(3)已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
化学式
CH3COOH
H2CO3
HClO
电离平衡常数
Ka=1.8×10-5
Ka1=4.3×10-7
Ka2=5.6×10-11
Ka=3.0×10-8
①物质的量浓度均为0.1mol•L-1的四种溶液:pH由小到大排列的顺序是__(用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
②常温下,0.1mol•L-1CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是___(填字母)
A.c(H+) B.
C.c(H+)•c(OH-) D.
E.
③写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:____。
④25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=____(填准确数值)。
⑤标准状况下,将1.12LCO2通入100mL1mol•L-1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+____。
高二化学综合题中等难度题查看答案及解析
-
NaHCO3在水溶液中,HCO3-的电离程度小于HCO3-的水解程度。回答下列有关问题:
⑴H2CO3的电离方程式为________;
⑵NaHCO3溶液显碱性,原因是(用离子方程式表示)
________;
⑶在该溶液中,c(Na+)、c(H+)、c(HCO3-)、c(OH-)的大小关系为
________;
⑷根据电荷守恒原理,该溶液中离子浓度关系有:
c(Na+)+c(H+)=________;
⑸根据物料守恒原理,该溶液中离子浓度关系有:
c(Na+)=。
高二化学填空题简单题查看答案及解析
-
物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡。请根据所学知识回答下列问题:
常温时,FeCl3的水溶液呈___(填“酸”“中”或“碱”)性,原因是___(用离子方程式表示);实验室配制0.01mol·L-1FeCl3的溶液时,为了抑制FeCl3的水解使溶液中不产生沉淀可加入少量的盐酸至溶液pH不大于___;若把配制的FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是___。(常温下Fe(OH)3的溶度积Ksp=1.0×10-38)
高二化学填空题中等难度题查看答案及解析
-
在生产生活和科学研究中,人们常常根据需要促进或抑制盐的水解.试回答下列问题:
(1)FeCl3溶液呈______ (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):______;实验室在配制FeCl3溶液时,常将FeCl3固体先溶于较浓的盐酸中,以______ (填“促进”、“抑制”)其水解,然后再用蒸馏水稀释到所需的浓度.
(2)用离子方程式表示硫酸铝溶液和碳酸氢钠溶液混合时发生的主要反应______.
(3)为证明盐的水解是吸热的,四位同学分别设计了如下方案,其中正确的是______.
A.甲同学:在盐酸中加入氨水,混合液温度上升,说明盐类水解是吸热的.
B.乙同学:将硝酸铵晶体溶于水,水温降低,说明盐类水解是吸热的.
C.丙同学:在氨水加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热的.
D.丁同学:在醋酸钠溶液中滴加2滴酚酞试剂,加热后红色加深,说明盐类水解是吸热的.
(4)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是______.高二化学解答题中等难度题查看答案及解析
-
按要求完成下列化学反应式
(1)硫酸氢钠在水溶液中的电离方程式 ________ ;
(2)Na2CO3溶液水解的离子方程式 ________ ;
(3)Al2(SO4)3溶液与NaHCO3溶液混合反应的离子方程式 ________ ;
(4)Mg3N2与水反应的化学方程式 ________ ;
高二化学填空题中等难度题查看答案及解析
-
按要求回答下列问题:
(1)配制FeCl3溶液时,需将固体溶于较浓的盐酸后按需要进行稀释,用离子方程式解释其原因 。
(2)用离子方程式表示出泡沫灭火器的原理 。
(3)实验室中常用NaOH溶液来进行洗气和提纯,当100mL 3mol·L-1的NaOH溶液吸收标准状况下4.48LCO2时,所得溶液中离子浓度由大到小的顺序为 。
(4)常温下,浓度均为0.1mol/L的下列五种溶液的PH值如下表所示:
溶质
CH3COONa
NaHCO3
Na2CO3
NaClO
NaCN
pH
8.8
9.7
11.6
10.3
11.1
①根据表中数据,将浓度均为0.01mol· L-1的下列四种酸的溶液分别稀释100倍,pH变化最小的是 。
A.HCN B.HClO C.H2CO3 D.CH3COOH
②根据以上数据,判断下列反应可以成立的是 。
A.CH3COOH+Na2CO3═NaHCO3+CH3COONa
B.CH3COOH+NaCN═CH3COONa+HCN
C.CO2+H2O+2NaClO═Na2CO3+2HClO
D.NaHCO3+HCN═NaCN+H2O+CO2
(5)已知在Cu2+、Mg2+、Fe2+浓度相同的溶液中,其开始沉淀时的pH如下:
离子
Fe2+
Cu2+
Mg2+
pH
7.6
5.2
10.4
若向该溶液中滴加NaOH溶液,则先沉淀的是 (填离子符号),
判断Ksp[Fe(OH)2] Ksp[Mg(OH)2](填“>”、“=”或“<”)。
已知Ksp[Cu(OH)2]=2.5×10-20,若向该溶液中加入生石灰调节其pH,当pH= 时,溶液中Cu2+沉淀完全。[已知1g2=0.3]
高二化学填空题简单题查看答案及解析