为防治碘缺乏病,通常在食盐中添加少量的碘酸钾()。碘酸钾和碘化钾在溶液中能发生如下反应:
。下列有关叙述正确的是( )
A.该反应中氧化剂为,还原剂为
B.该反应中,每生成3mol时转移的电子数目为5NA
C.上述反应中,氧化产物与还原产物的质量之比为1:5
D.直接向食盐中加入淀粉溶液,可以判断该食盐是否为加碘食盐
高三化学单选题中等难度题
为防治碘缺乏病,通常在食盐中添加少量的碘酸钾()。碘酸钾和碘化钾在溶液中能发生如下反应:
。下列有关叙述正确的是( )
A.该反应中氧化剂为,还原剂为
B.该反应中,每生成3mol时转移的电子数目为5NA
C.上述反应中,氧化产物与还原产物的质量之比为1:5
D.直接向食盐中加入淀粉溶液,可以判断该食盐是否为加碘食盐
高三化学单选题中等难度题
为防治碘缺乏病,通常在食盐中添加少量的碘酸钾()。碘酸钾和碘化钾在溶液中能发生如下反应:
。下列有关叙述正确的是( )
A.该反应中氧化剂为,还原剂为
B.该反应中,每生成3mol时转移的电子数目为5NA
C.上述反应中,氧化产物与还原产物的质量之比为1:5
D.直接向食盐中加入淀粉溶液,可以判断该食盐是否为加碘食盐
高三化学单选题中等难度题查看答案及解析
下列叙述正确的是( )
A. 金属单质与盐溶液的反应都是置换反应
B.加碘食盐中添加碘酸钾而不用碘化钾,是因为碘酸钾能溶于水而碘化钾难溶于水
C. 与强酸、强碱都反应的物质只有两性氧化物和两性氢氧化物
D.氯气可用作消毒剂和漂白剂,是因为氯气与水反应生成的次氯酸具有强氧化性
高三化学选择题中等难度题查看答案及解析
我国碘缺乏病病区人口约亿多,缼碘地区几乎覆盖全国,为此我国采用在食盐中添加含碘物质制成含碘食盐,该物质是
A.碘酸钾 B.碘化钾 C.碘单质 D.络合碘
高三化学单选题简单题查看答案及解析
(12分) 为防止碘缺乏病,通常在食盐中加入KIO3。
(1)用淀粉碘化钾溶液和稀硫酸可定性检验出食盐中的IO3-,表示该反应的离子方程
式是________________________________________,
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液
将I2还原,又可以回收四氯化碳。Na2SO3稀溶液与I2反应的离子方程式是 ________。
(3)已知:I2+2S2O32-=2I-+S4O62-。
某课外活动小组为测定混有MgCl2的食用加碘盐中所含MgCl2、KIO3的含量,按下图所示实验步骤进行实验。
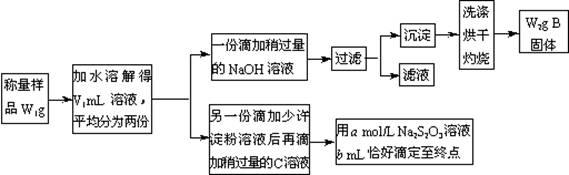
请回答下列问题:
①写出B和C的化学式:B________,C________。
②滴定时,判断滴定达到终点的现象是________。
③KIO3的质量分数是________(列出计算式)。
④使所测MgCl2的质量分数可能偏高的操作是(填写字母)________
A 过滤后未洗涤所得沉淀,直接烘干灼烧
B 在敞口容器中用托盘天平称量样品时,操作时间过长
C 沉淀灼烧不彻底
高三化学实验题中等难度题查看答案及解析
含碘食盐中的碘是以碘酸钾形式存在的。已知在酸性溶液中
和
发生下列反应
。现有下列物质①稀硫酸;②
试纸;③淀粉碘化钾溶液;④淀粉溶液。利用上述反应,可用来检验含碘食盐中含有
的是
A.②④ B.①③ C.②③ D.①④
高三化学单选题中等难度题查看答案及解析
含碘食盐中的碘是以碘酸钾(KIO3)形式存在的。已知在酸性溶液中IO3-和I-发生下列反应IO3-+5I-+6H+=3I2+3H2O。现有下列物质①稀硫酸;②pH试纸;③淀粉碘化钾溶液;④淀粉溶液。利用上述反应,可用来检验含碘食盐中含有IO3-的是( )
A、②④ B、①③ C、②③ D、①④
高三化学选择题简单题查看答案及解析
为实现消除碘缺乏病的目标,国家卫生部规定食盐必须加碘,其中碘以碘酸钾或碘化钾的形式存在。
(1)有人烹调时,分别含有碘化钾和碘酸钾的加碘食盐混合,当滴食醋时,产生紫色蒸气,反应的离子方程式为_______________。
(2)可以利用Na2S2O3滴定I2来测定食盐中的含碘量,发生的反应如下: I2+2Na2S2O3===2NaI+Na2S4O6,判断滴定终点的现象是___________________,该滴定实验必须在中性或弱酸性溶液中进行。因为在碱性溶液中,I2会发生反应(已知IO3-比IO-更稳定),其离子方程式为_________________________________________,而且I2与S2O32-发生副发应,其离子方程式为______________________________。
(3)若在强酸性溶液中,Na2S2O3会发生分解,其离子方程式为____________,同时I离子容易与空气中的氧气发生反应,其反应的离子方程为____________。
高三化学填空题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析
碘酸钾作为食盐—碘添加剂,而碘化钾则是化工生产中一种重要原料。还原法生产碘化钾是由碘与氢氧化钾反应生成碘酸钾后,用甲酸还原而得,其主要流程如图。
请回答下列问题:
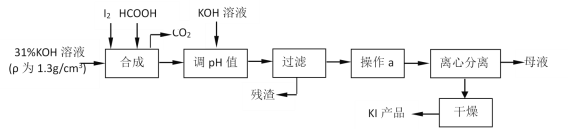
(1)判断“合成”过程中,碘是否已完全反应的方法是___。
(2)实验室中,过滤操作要求“一贴二低三靠”,其中“三靠”是指盛有被过滤液体的烧杯注液口紧靠玻璃棒、___、___。
操作a包括“蒸发浓缩、冷却结晶”是依据KI具有何种性质:___。
(3)写出“合成”过程中,HCOOH参与的离子反应方程式:___。
(4)测定产品中KI含量的方法是:
a.称取3.340g样品、溶解,在250mL容量瓶中定容;
b.量取25.00mL溶液于锥形瓶中,加入足量KIO3,用少量稀硫酸酸化所,使KIO3与KI反应完全;
c.以淀粉为指示剂,用0.2400mol/L的Na2S2O3溶液滴定,消耗溶液体积平均值为10.00mL。
已知:IO3-+I-+H+→I2+H2O(未配平),I2+2S2O32-→2I-+S4O62-。
①测定过程所需仪器在使用前必须检查是否漏液的有___。
②该样品中KI的质量分数为___。(保留3位有效数字)
(5)有学生选用家庭厨房中的有关调料(如黄酒、白醋、酱油、味精等),用简便方法来检测是否是加碘食盐。通过实践,发现厂商只要在食盐包装的封口处夹一条碘化钾淀粉试纸,并在袋上注明使用方法就能鉴别真伪。现请你写出检测使用说明书___。
高三化学工业流程中等难度题查看答案及解析
(8分)市场销售的某种食用精制盐包装袋上有如下说明(部分):
| 产品标准 | |
| 产品等级 | 一级 |
| 配料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处):________+________
+________
4 = ________
+________
+________
(2)上述反应生成的可用四氯化碳检验。向碘的四氯化碳溶液中加入
稀溶液,将
还原,以回收四氯化碳。
①稀溶液与
反应的离子方程式是________
②某学生设计回收四氯化碳的操作步骤为:
a、将碘的四氯化碳溶液置于分液漏斗中; b、加入适量稀溶液;
c、分离出下层液体。
以上设计中遗漏的操作及在上述操作中的位置是________
(3)已知:
某学生测定食用精制盐的碘含量,其步骤为:
a、准确称取食盐,加适量蒸馏水使其完全溶解;
b、用稀硫酸酸化所得溶液,加入足量溶液,使食用盐中
与
反应完全;
c、以淀粉溶液为指示剂,逐滴加入物质的量浓度为的
溶液
,恰好反应完全。
①判断c中反应恰好完全依据的现象是________
②根据以上实验和包装说明,所测精盐的碘含量是________
高三化学实验题简单题查看答案及解析