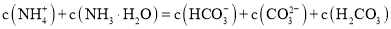-
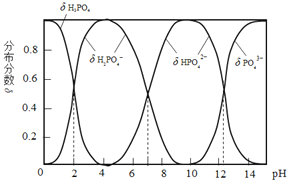
磷酸(H3PO4)是一种中强酸,常温下,H3PO4水溶液中含磷微粒的分布分数(平衡时某微粒的浓度占各含磷微粒总浓度的分数)与pH的关系如图,下列说法正确的是( )
A.H3PO4的电离方程式为:H3PO4 3H++ PO43−
3H++ PO43−
B.pH=2时,溶液中大量存在的微粒有:H3PO4、H2PO4−、HPO42−、PO43−
C.滴加NaOH溶液至pH=7,溶液中c(Na+)= c(H2PO4−)+2c(HPO42−)+3c(PO43−)
D.滴加少量Na2CO3溶液,3Na2CO3+2H3PO4 =2Na3PO4+3H2O+3CO2↑
-
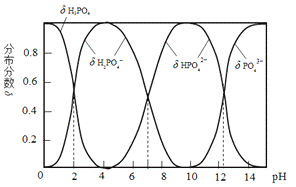
磷酸(H3PO4)是一种中强酸,常温下,H3PO4水溶液中含磷微粒的分布分数(平衡时某微粒的浓度占各含磷微粒总浓度的分数)与pH的关系如图,下列说法正确的是( )

A.H3PO4的电离方程式为:H3PO4 3H++PO43-
3H++PO43-
B.pH=2时,溶液中大量存在的微粒有:H3PO4、H2PO4-、HPO42-、PO43-
C.滴加NaOH溶液至pH=7,溶液中c(Na+)=c(H2PO4-)+2c(HPO42-)+3c(PO43-)
D.滴加少量Na2CO3溶液,3Na2CO3+2H3PO4=2Na3PO4+3H2O+3CO2↑
-
H3PO4是三元酸,如图是在常温下溶液中含磷微粒的物质的量分数(δ)随pH变化示意图。下列说法不正确的是( )
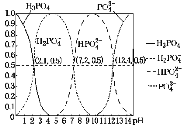
A.磷酸的第二级电离平衡常数约为10-7.2
B.在NaH2PO4溶液中:c(HPO42-)>c(H3PO4-)
C.在磷酸中滴加NaOH溶液至pH=7,c(Na+)=2c(HPO42)+c(H2PO4)
D.Na3PO4溶液中:c(Na+)=3c(PO43-)+3c(HPO42-)+3c(H2PO4-)+3c(H3PO4)
-
已知H3PO4是一种三元中强酸。25℃时,某浓度H3PO4溶液中逐滴加入NaOH溶液,滴加过程中各种含磷微粒的物质的量分数δ随溶液pH的变化曲线如下图所示。下列说法正确的是
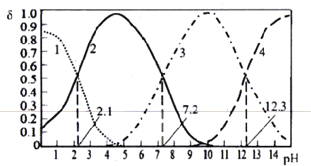
A. 曲线2和曲线4分别表示δ(HPO42-)和δ(PO43-)变化
B. 25℃时,H3PO4的电离常数K1:K2=105.1
C. pH=7.2时,溶液中由水电离出的c(H+)=10-7.2mol/L
D. pH=12.3时,溶液中2c(Na+)=5c(H2PO4-)+5c(HPO42-)+5c(PO43-)+5c(H3PO4)
-
已知H3PO4是一种三元中强酸。25℃时,某浓度H3PO4溶液中逐滴加入NaOH溶液,滴加过程中各种含磷微粒的物质的量分数δ随溶液pH的变化曲线如下图所示。下列说法正确的是
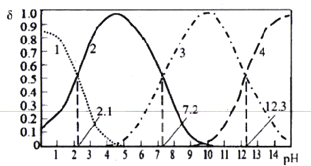
A. 曲线2和曲线4分别表示δ(HPO42-)和δ(PO43-)变化
B. 25℃时,H3PO4的电离常数K1:K2=105.1
C. pH=7.2时,溶液中由水电离出的c(H+)=10-7.2mol/L
D. pH=12.3时,溶液中2c(Na+)=5c(H2PO4-)+5c(HPO42-)+5c(PO43-)+5c(H3PO4)
-
通常认为残留在溶液中的离子浓度小于1×10-5mol/L时,离子不存在。图为H3PO4 (图中用H3A 表示) 在加入强酸或强碱溶液后,平衡时溶液中各微粒浓度的对数值(lgc)-pH图。下列说法不正确的是( )
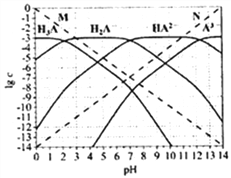
A. H3PO4 、H2PO4-、HPO42-、PO43-不能在同一溶液中大量共存
B. H3PO4电离平衡常数Ka2≈1×10-7
C. 图中虚线M、N 分别代表H+和OH-
D. pH=10时,溶液中存在关系:c(HPO42-) >c(OH-) >c(PO43-) >c(H2PO4-) >c(H3PO4)>c(H+)
-
通常认为残留在溶液中的离子浓度小于1×10-5mol/L时,离子不存在。图为H3PO4 (图中用H3A 表示) 在加入强酸或强碱溶液后,平衡时溶液中各微粒浓度的对数值(lgc)-pH图。下列说法不正确的是
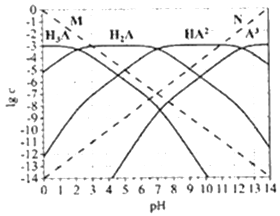
A. H3PO4、H2PO4-、HPO42-、PO43-不能在同一溶液中大量共存
B. H3PO4电离平衡常数Ka2≈1×10-7
C. 图中虚线M、N 分别代表H+和OH-
D. pH=10时,溶液中存在关系:c(HPO42-)>c(OH-)>c(PO43-)>c(H2PO4-)>c(H3PO4)>c(H+)
-
常温下,现有 的
的 溶液,
溶液, 已知含氮
已知含氮 或含碳
或含碳 各微粒的分布分数
各微粒的分布分数 平衡时某种微粒的浓度占各种微粒浓度之和的分数
平衡时某种微粒的浓度占各种微粒浓度之和的分数 与pH的关系如图所示。下列说法不正确的是
与pH的关系如图所示。下列说法不正确的是
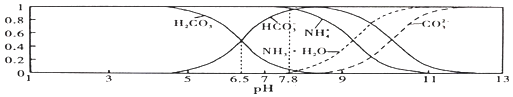
A.常温下
B.向 的上述溶液中逐滴滴加NaOH溶液时,
的上述溶液中逐滴滴加NaOH溶液时, 和
和 浓度都逐渐减小
浓度都逐渐减小
C. 溶液中存在下列守恒关系:
溶液中存在下列守恒关系: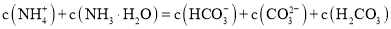
D.当溶液的 时,溶液中存在下列关系:
时,溶液中存在下列关系:
-
常温下,现有 溶液,
溶液, 已知含氮
已知含氮 或含碳
或含碳 各微粒的分布分数
各微粒的分布分数 平衡时,各微粒浓度占总微粒浓度之和的分数
平衡时,各微粒浓度占总微粒浓度之和的分数 与pH 的关系如图所示。下列说法正确的是
与pH 的关系如图所示。下列说法正确的是
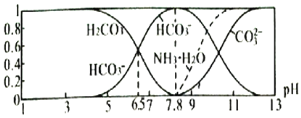
A.当 时,溶液中存在下列关系:
时,溶液中存在下列关系:

B. 溶液中存在下列关系:
溶液中存在下列关系:
C.向 的上述溶液中逐滴滴加氢氧化钠溶液时,
的上述溶液中逐滴滴加氢氧化钠溶液时, 和
和 浓度逐渐减小
浓度逐渐减小
D.分析可知,常温下水解平衡常数 的数量级为
的数量级为
-
常温下,现有 溶液,
溶液, 已知含氮
已知含氮 或含碳
或含碳 各微粒的分布分数
各微粒的分布分数 平衡时,各微粒浓度占总微粒浓度之和的分数
平衡时,各微粒浓度占总微粒浓度之和的分数 与pH 的关系如图所示。下列说法正确的是
与pH 的关系如图所示。下列说法正确的是

A.当 时,溶液中存在下列关系:
时,溶液中存在下列关系:

B. 溶液中存在下列关系:
溶液中存在下列关系:
C.向 的上述溶液中逐滴滴加氢氧化钠溶液时,
的上述溶液中逐滴滴加氢氧化钠溶液时, 和
和 浓度逐渐减小
浓度逐渐减小
D.分析可知,常温下水解平衡常数 的数量级为
的数量级为

3H++PO43-