常温下,0.2mol/L Na2CrO4溶液中,H2CrO4、CrO42-、Cr2O72-和HCrO4-的分布曲线如图所示.下列叙述错误的是( )

(已知:2CrO42-+2H+⇌Cr2O72-+H2O)
A.曲线M表示pH与CrO42-的变化关系
B.Ka2(H2CrO4)的数量级为10-1
C.HCrO4-的电离程度大于水解程度
D.pH=2和pH=5时,2HCrO4-⇌Cr2O72-+H2O的平衡常数相等
高三化学单选题中等难度题
常温下,0.2mol/L Na2CrO4溶液中,H2CrO4、CrO42-、Cr2O72-和HCrO4-的分布曲线如图所示.下列叙述错误的是( )

(已知:2CrO42-+2H+⇌Cr2O72-+H2O)
A.曲线M表示pH与CrO42-的变化关系
B.Ka2(H2CrO4)的数量级为10-1
C.HCrO4-的电离程度大于水解程度
D.pH=2和pH=5时,2HCrO4-⇌Cr2O72-+H2O的平衡常数相等
高三化学单选题中等难度题
常温下,0.2mol/L Na2CrO4溶液中,H2CrO4、CrO42-、Cr2O72-和HCrO4-的分布曲线如图所示.下列叙述错误的是( )

(已知:2CrO42-+2H+⇌Cr2O72-+H2O)
A.曲线M表示pH与CrO42-的变化关系
B.Ka2(H2CrO4)的数量级为10-1
C.HCrO4-的电离程度大于水解程度
D.pH=2和pH=5时,2HCrO4-⇌Cr2O72-+H2O的平衡常数相等
高三化学单选题中等难度题查看答案及解析
下表是某铬酸(H2CrO4)溶液中离子浓度(mol.L-1)与pH的关系,下列说法不正确的是
| pH | c(CrO42-) | c(HCrO4-) | c( Cr2O72-)] | c(H2CrO4) |
| 4 | 0.0003 | 0.1040 | 0.4480 | 0 |
| 6 | 0.0319 | 0.0999 | 0.4370 | 0 |
| 7 | 0.2745 | 0.0860 | 0.3195 | 0 |
| 9 | 0.9960 | 0.0031 | 0.0004 | 0 |
A.铬酸的第一步电离是完全电离
B.铬酸的第二步电离是部分电离,且存在两种电离方式
C.当电离达到平衡时,2(Cr2O72-)=
(HCrO4-)
D.pH越大,电离出的CrO42-浓度越大
高三化学选择题简单题查看答案及解析
下表是不同pH环境时某浓度铬酸(H2CrO4)溶液中,离子浓度(mol/L)与pH的关系,下列说法错误的是
| pH | c(CrO42—) | c(HCrO4—) | c(Cr2O72—) | c(H2CrO4) |
| 4 | 0.0003 | 0.1040 | 0.4480 | 0 |
| 6 | 0.0319 | 0.0999 | 0.4370 | 0 |
| 7 | 0.2745 | 0.0860 | 0.3195 | 0 |
| 9 | 0.9960 | 0.0031 | 0.0004 | 0 |
A.铬酸第一级电离方程式为H2CrO4 H++HCrO4—
B.要得到CrO42—应控制溶液的pH>9
C.当电离达到平衡时,2v(正)(HCrO4—)= v(逆)(Cr2O72—)
D.该铬酸溶液的物质的量浓度约为1.00mol/L
高三化学选择题困难题查看答案及解析
已知:2CrO42-+2H+⇌Cr2O72-+H2O。25℃时,调节初始浓度为1.0mol⋅L-1的Na2CrO4溶液的pH,测定平衡时溶液中c(Cr2O72-)和c(H+),获得如图所示的曲线。下列说法不正确的是( )

A.平衡时,pH越小,c(Cr2O72-)越大
B.A点CrO42-的平衡转化率为50%
C.A点CrO42-转化为Cr2O72-反应的平衡常数K=1014
D.平衡时,若溶液中c(Cr2O72-)=c(Cr2O42-),则c(H+)>2.0×10-7mol⋅L-1
高三化学单选题中等难度题查看答案及解析
已知:2CrO42-+2H+Cr2O72-+H2O。 25℃时,调节初始浓度为1.0 mol·L-1的Na2CrO4溶液的pH,测定平衡时溶液中c(Cr2O72-)和c(H+),获得如下曲线。下列说法不正确的是( )
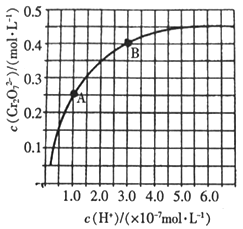
A. 平衡时,pH越小,c(Cr2O72-)越大
B. A、B两点c(CrO42-)之比为5:2
C. B点CrO42-的平衡转化率为40%
D. 平衡时,若溶液中c(CrO42-)=2c(Cr2O72-),则c(H+)=1.0×10-7mol·L-1
高三化学单选题中等难度题查看答案及解析
已知:溶液中存在2CrO42- +2H+Cr2O72- + H2O。25℃时,调节初始浓度为1.0mol·L-1 Na2CrO4溶液的pH(溶液体积变化忽略不计),溶液中-lgc(Cr2O72-)与-lg[c(CrO42-)·c(H+)]的关系如图所示。下列说法错误的是
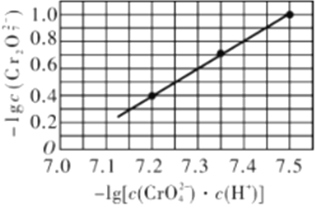
A.若将原溶液加少量水稀释,溶液中的值增大
B.当c(Cr2O72-)=c(CrO42- )时溶液的pH<7
C.反应的平衡常数K=1×1014
D.若只升高温度,c(CrO42-)增大,则该反应的∆H<0
高三化学单选题中等难度题查看答案及解析
某同学设计如下图所示装置,用电解法把Na2CrO4溶液转变为Na2Cr2O7溶液(2CrO42-+2H+=Cr2O72-+H2O)。下列说法正确的是

A. A为正极,B为负极
B. 电解过程中,电解槽左侧溶液pH增大
C. 电解过程中,Na+在电解槽中自左向右迁移
D. 当电路中通过lmol电子时,阴极生成0.5mol Na2Cr2O7
高三化学选择题困难题查看答案及解析
根据反应2CrO42-+2H+Cr2O72-+H2O 用惰性电极电解Na2CrO4溶液制取Na2Cr2O7,下列说法不正确的是
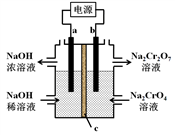
A. a连接电源负极
B. b极反应式:2H2O-4e-=O2↑+4H+
C. c为阳离子交换膜
D. 通过2 mol电子时生成1 mol Cr2O72-
高三化学选择题中等难度题查看答案及解析
还原沉淀法是处理含铬(Cr2O72- 和CrO42-)废水常用方法,过程如下: 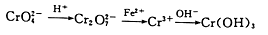
已知废水中Cr的含量为26.0g·L-1,当溶液中离子浓度小于10-5mol/L时认为离子已经沉淀完全。常温下, KSP[Cr(OH)3]=1×10-32。有关叙述中不正确的是
A.上述三个转化中只有一个涉及氧化还原反应
B.第二步离子方程式为:Cr2O72-+14H++6Fe2+=2Cr3++7H2O+6Fe3+
C.处理含铬废水可使用强碱Ba(OH)2,也可以使用弱碱氨水
D.当PH≥5时,废水中铬元素沉淀完全
高三化学选择题中等难度题查看答案及解析
还原沉淀法是处理含铬(Cr2O72-和CrO42-)废水常用方法,过程如下:
,已知废水中Cr的含量为26.0g·L-1,当溶液中离子浓度小于10-5mol/L时认为离子已经沉淀完全。常温下Ksp[Cr(OH)3]= 1×10-32。有关叙述中不正确的是( )
A.上述三个转化中只有一个涉及氧化还原反应
B.第二步离子方程式为:Cr2O72-+14H++6Fe2+=2Cr3++7H2O+6Fe3+
C.处理含铬废水可使用强碱Ba(OH)2,也可以使用弱碱氨水
D.当pH≥5时,废水中铬元素沉淀完全
高三化学选择题困难题查看答案及解析