-
Ⅰ.已知NH3•H2O与醋酸的电离度在同温同浓度下相等。向少量Mg(OH)2悬浊液中加入适量的饱和氯化铵溶液,结果固体完全溶解。
甲同学的解释是:
Mg(OH)2 (固) Mg2++2OH- (1)
Mg2++2OH- (1)
NH4++H2O NH3H2O+H+ (2)
NH3H2O+H+ (2)
H++OH- H2O (3)
H2O (3)
由于(3)的发生,使平衡(1)右移,沉淀溶解。
乙同学的解释是:
Mg(OH)2 (固) Mg2++2OH- (1)
Mg2++2OH- (1)
NH4Cl=NH4++Cl- (2)
NH4++OH- NH3H2O (3)
NH3H2O (3)
由于(3)的发生,使平衡(1)右移,沉淀溶解。
丙同学不能肯定哪位同学的解释合理,于是选用下列的一种试剂,来证明甲、乙两位同学的解释只有一种正确。
(1)他选用的试剂是__________(填写编号)。
A. NH4NO3 B. CH3COONH4 C. Na2CO3 D. NH3•H2O
(2)实验步骤:____________________________;
(3)实验结论:____________________________。
Ⅱ.关于“电解氯化铜溶液时的pH变化”问题,化学界有两种不同的观点。
观点一:“理论派”认为电解氯化铜溶液后溶液的pH升高;
观点二:“实验派”经过反复、多次、精确的实验测定,证明电解氯化铜溶液时的pH的变化如图。请回答下列问题:
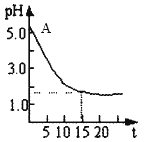
(1)用离子方程式表示电解前氯化铜溶液的pH处于A点的原因:______________。
(2)“理论派”所持观点的理论依据是:_______________________。
(3)你支持哪种观点:_________(理论派、实验派)。其理由是_____________。
-
已知氨水与醋酸的电离程度在同温同浓度下相等,溶有一定量氨的氯化铵溶液呈碱性。现向少量的Mg(OH)2悬浊液中加入适量的饱和氯化铵溶液,固体完全溶解。
甲同学的解释是:
Mg(OH)2(s) Mg2+(aq)+2OH-(aq)①
Mg2+(aq)+2OH-(aq)①
N+H2O NH3·H2O+H+②
NH3·H2O+H+②
H++OH- H2O③
H2O③
由于N水解显酸性,H+与OH-反应生成水,导致反应①平衡右移,沉淀溶解;
乙同学的解释是:
Mg(OH)2(s) Mg2+(aq)+2OH-(aq)①
Mg2+(aq)+2OH-(aq)①
N+OH- NH3·H2O②
NH3·H2O②
由于NH4Cl电离出的N与Mg(OH)2电离出的OH-结合,生成了弱电解质NH3·H2O,导致反应①的平衡右移,Mg(OH)2沉淀溶解。
(1)丙同学不能肯定哪位同学的解释合理,于是选用下列的一种试剂,来证明甲、乙两位同学解释只有一种正确,他选用的试剂是 (填写编号)。
A.NH4NO3 B.CH3COONH4
C.Na2CO3 D.NH3·H2O
(2)请你说明丙同学作出该选择的理由是 。
(3)丙同学将所选试剂滴入Mg(OH)2悬浊液中,Mg(OH)2溶解;由此推知,甲和乙哪位同学的解释更合理 (填“甲”或“乙”);写出NH4Cl饱和溶液使Mg(OH)2悬浊液溶解的离子方程式 。
-
向少量Mg(OH)2悬浊液中加入适量的饱和NH4Cl溶液,结果固体完全溶解。对此甲、乙两同学各自作了自己的解释:
甲:Mg(OH)2(s)  Mg2++2OH- ①,NH4++H2O
Mg2++2OH- ①,NH4++H2O NH3·H2O+H+ ②,H++OH-=H2O ③,由于③反应的发生,使平衡①右移,Mg(OH)2溶解。
NH3·H2O+H+ ②,H++OH-=H2O ③,由于③反应的发生,使平衡①右移,Mg(OH)2溶解。
乙:Mg(OH)2(s)  Mg2++2OH-①,NH4++ OH-
Mg2++2OH-①,NH4++ OH- NH3·H2O②,由于②反应的发生,使平衡①右移,沉淀溶解。
NH3·H2O②,由于②反应的发生,使平衡①右移,沉淀溶解。
(1)丙同学不能肯定哪位同学的解释合理,于是用下面的一种试剂重做了该实验,证明甲、乙的解释只有一种正确。他用的试剂是________。
A.NH4NO3 B.CH3COONH4 C.(NH4)2SO4 D.氨水
(2)丙同学将所选试剂滴入Mg(OH)2的浊液中,Mg(OH)2溶解;由此推知,甲和乙哪位同学的解释更合理____(填“甲”或“乙”);完成NH4Cl饱和溶液使Mg(OH)2悬浊溶解的离子方程式______。
-
下列叙述正确的是
A.盐酸中滴加氨水至中性,溶液中溶质为氯化铵
B.稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小
C.饱和石灰水中加入少量CaO,恢复至室温后溶液的pH不变
D.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强
-
下列叙述正确的是
A.盐酸中滴加氨水至中性,溶液中溶质为氯化铵
B.稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小
C.饱和石灰水中加入少量CaO,恢复至室温后溶液的pH不变
D.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强
-
下列叙述正确的是
A.盐酸中滴加氨水至中性,溶液中溶质为氯化铵
B.稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小
C.饱和石灰水中加入少量CaO,恢复至室温后溶液的pH值不变
D.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强
-
下列叙述正确的是( )
A. 盐酸中滴加氨水至中性,溶液中溶质为氯化铵
B. 稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小
C. 饱和石灰水中加入少量CaO,恢复至室温后溶液的pH不变
D. 同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7
-
欲使醋酸溶液中的CH3COO-浓度增大,电离平衡向右移动,且不放出气体,可向醋酸溶液中加入少量固体
A.NaOH B.NaHCO3 C.CH3COOK D.Mg
-
对于难溶电解质的沉淀溶解平衡,下列说法正确的是( )
A.Ksp数值越小,难溶电解质的溶解度一定越小
B.在氯化银饱和溶液中,增大Ag+浓度,AgCl的溶度积增大
C.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)不变
D.向AgCl饱和溶液中加入NaCl固体,Ksp不变,有固体析出
-
下列叙述中,错误的是
A.虽然固体氯化钠不能导电,但氯化钠是电解质
B.纯水的pH随温度的升高而减小
C.在醋酸钠溶液中加入少量氢氧化钠,溶液中c(OH—)增大
D.在纯水中加入少量硫酸铵,可抑制水的电离
Mg2++2OH- (1)
NH3H2O+H+ (2)
H2O (3)
Mg2++2OH- (1)
NH3H2O (3)
