-
过渡元素铁可形成多种配合物,如黄血盐[K4Fe(CN)6]、普鲁士蓝、血红素等
(1)已知:3K4Fe(CN)6]=2KCN + Fe3C + 3C + (CN)2↑ +2N2↑
①(CN)2分子中σ键和π键的数目比为n(σ)﹕n(π)=____。
②(CN)2在一定条件下氢化可以得到乙二胺(H2NCH2CH2NH2),乙二胺易溶于水,除因为是极性分子外,还可能的原因是____。
(2)普鲁士蓝的化学式为Fe4[Fe(CN)6]3,写出外界离子基态核外电子排布式____。
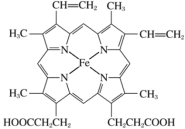
(3)血红素(如图)是血红蛋白的合成原料之一,血红色中的N原子的杂化类型为____,请用“→”在图中标出Fe2+的配位键_________。
-
过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等.
(1)Fe2+基态核外电子排布式为 。
(2)科学研究表明用TiO2作光催化剂可将废水中CN-转化为OCN-、并最终氧化为N2、
CO2。OCN-中三种元素的电负性由大到小的顺序为 。
(3)与CN-互为等电子体的一种离子为 (填化学式);1mol [Fe(CN)6]4-中含有σ键的数目为 。
(4)铁的另一种配合物Fe(CO)5熔点为﹣20.5℃,沸点为 103℃,易溶于CCl4,据此可以判断Fe(CO)5晶体属于 (填晶体类型)。
103℃,易溶于CCl4,据此可以判断Fe(CO)5晶体属于 (填晶体类型)。
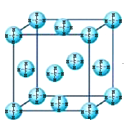
(5)铁铝合金的一种晶体属于面心立方结构,其晶胞可看成由8个小体心立方结构堆砌而成.已知小立方体如图所示.该合金的化学式为 。

-
元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同.
(1)第四周期过渡元素的明显特征是形成多种多样的配合物.
①CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5]、羰基镍[Ni(CO)4].CO分子中C原子上有一对孤对电子,C,O原子都符合8电子稳定结构,CO的结构式为__,与CO互为等电子体的离子为__(填化学式).
②金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子.423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉.试推测Ni(CO)4易溶于下列___________.
a.水 b.四氯化碳 c.苯 d.硫酸镍溶液
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的.镓的基态原子的电子排布式是__,Ga的第一电离能却明显低于Zn,原因是__.
(3)用价层电子对互斥理论预测H2Se和BBr3的立体结构,两个结论都正确的是__.
a.直线形;三角锥形 b.V形;三角锥形
c.直线形;平面三角形 d.V形;平面三角形.
-
元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
(1)第四周期过渡元素的明显特征是形成多种多样的配合物
① CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5].羰基镍[Ni(CO)4]。CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO的结构式为 ,与CO互为等电子体的离子为 (填化学式)。
② 金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子。423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测Ni(CO)4易溶于下列 。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。镓的基态原子的电子排布式是 ,Ga的第一电离能却明显低于Zn,原因是 。
(3)用价层电子对互斥 理论预测H2Se和BBr3的立体结构,两个结论都正确的是 。
理论预测H2Se和BBr3的立体结构,两个结论都正确的是 。
A.直线形;三角锥形
B.V形;三角锥形
C.直线形;平面三角形
D.V形;平面三角形
-
元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
(1)第四周期过渡元素的明显特征是形成多种多样的配合物
① CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5].羰基镍[Ni(CO)4]。CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO的结构式为 ,与CO互为等电子体的离子为 (填化学式)。
② 金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子。423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测Ni(CO)4易溶于下列 。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。镓的基态原子的电子排布式是 ,Ga的第一电离能却明显低于Zn,原因是 。
(3)用价层电子对互斥 理论预测H2Se和BBr3的立体结构,两个结论都正确的是 。
理论预测H2Se和BBr3的立体结构,两个结论都正确的是 。
A.直线形;三角锥形
B.V形;三角锥形
C.直线形;平面三角形
D.V形;平面三角形
-
元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同.
(1)第四周期过渡元素的明显特征是形成多种多样的配合物
①CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5].羰基镍[Ni(CO)4].CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO的结构式为 ,与CO互为等电子体的离子为 (填化学式).
②金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子.423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉.试推测Ni(CO)4易溶于下列 .
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的.镓的基态原子的电子排布式是 ,Ga的第一电离能却明显低于Zn,原因是 .
(3)用价层电子对互斥理论预测H2Se和BBr3的立体结构,两个结论都正确的是 .
A.直线形;三角锥形
B.V形;三角锥形
C.直线形;平面三角形
D.V形;平面三角形.
-
(12分)元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
⑴第四周期过渡元素的明显特征是形成多种多样的配合物。
①CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5]、羰基镍[Ni(CO)4]。CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO的结构式为,与CO互为等电子体的离子为 ________(填化学式)。
②金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子。423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测Ni(CO)4易溶于下列 ________ 。
a.水 b.四氯化碳 c.苯 d.硫酸镍溶液
⑵第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。镓的基态原子的电子排布式是,Ga的第一电离能却明显低于Zn,原因是。
⑶用价层电子对互斥理论预测H2Se和BBr3的立体结构,两个结论都正确的是。
a.直线形;三角锥形 b.V形;三角锥形
c.直线形;平面三角形 d.V形;平面三角形
⑷Fe、Co、Ni、Cu等金属能形成配合物与这些金属原子的电子层结构有关。
①Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于________(填晶体类型)。
②CuSO4·5H2O(胆矾)中含有水合铜离子因而呈蓝色,写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来)________。
-
第四周期过渡金属元素的特征是能形成多种多样的配合物。
(1)CO可以和很多过渡金属形成配合物。CO和N2的价电子总数相同,它们的分子中都存在三个共价键,其中包含______个σ键,______个π键。
(2)下表为CO和N2的有关信息。
| 键的类型 | A—B | AB | AB |
| 键能 | CO | 351 | 803 | 1071 |
| N2 | 159 | 418 | 946 |
根据表中数据,说明CO比N2活泼的原因是________________________。
(3)Fe能与CO反应的原因与其电子层结构有关。基态Fe原子的电子排布式为________________。
Fe(CO)5常温下为黄色液体,熔点为251 K,沸点为376 K,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于________(填晶体类型);Fe(CO)5是配合物,配位体是________。
(4)一般地,第四周期过渡金属元素的第一电离能随原子序数的增大而增大,而31Ga的第一电离能却明显低于30Zn,原因是________________________________________________________________________。
-
(12分)Co、Cu、Zn都是过渡元素,可作为中心原子形成多种配合物
(1)下列不能作为配合物配位体的是( )
A.H2O B.NH3 C.CH4 D.Cl-
(2)用氢键表示式写出氨水中NH3分子与水分子间形成的可能存在的氢键 。
(3)Cu元素可形成[Cu(NH3)4]SO4,其中存在的化学键类型有___ __(填序号)。
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
(4)若[Cu(H2O)4]2+具有对称的空间构型,且当其中的两个NH3被两个Cl-取代时,能得到两种不同结构的产物,则[Cu(H2O4]2+的空间构型为______(填字母)。
a.平面正方形 b.正四面体 c.三角锥型 d.V形
在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,最后沉淀溶解形成深蓝色的溶液。写出此蓝色沉淀溶解的离子方程式:___________________;
(5)把CoCl2溶解于水后加氨水直到先生成的Co(OH)2沉淀又溶解后,再继续加氨水,使之生成 [Co(NH3)6]2+。此时向溶液中通入空气,得到的产物中有一种的组成可用CoCl3·5NH3表示,把分离出的CoCl3·5NH3溶于水后立即加硝酸银溶液,则析出AgCl沉淀。经测定每1 mol CoCl3·5NH3只生成2 mol AgCl。请写出表示此配合物结构的结构简式:_____ ____。
-
(1)Co、Cu、Zn都是过渡元素,可作为中心原子形成多种配合物,下列不能作为配合物配位体的是______;
A.H2O B.NH3 C.CH4 D.Cl﹣
(2)用氢键表示式写出氨水中NH3分子与水分子间可能存在的氢键____;
(3)Cu元素可形成[Cu(NH3)4]SO4,其中存在的化学键类型有______(填序号);
①配位键 ②氢键 ③极性共价键 ④非极性共价键 ⑤离子键
(4)甲烷晶体的晶胞结构如下图,下列有关说法正确的是_______。
A.甲烷在常温下呈气态,说明甲烷晶体属于分子晶体
B.晶体中1个CH4分子有12个紧邻的甲烷分子
C.CH4晶体熔化时需克服共价键
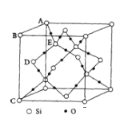
(5)下图表示的是SiO2的晶胞结构(白圈代表硅原子,黑点代表氧原子),判断在30g二氧化硅晶体中含______mol Si-O键。如果该立方体的边长为a cm,用NA 表示阿伏加德罗常数,则SiO2晶体的密度表达式为__________________g/cm3 。