已知25 ℃下,醋酸溶液中各微粒存在下述关系:K==1.75×10-5,下列有关说法可能成立的是( )
A.25 ℃下,向该溶液中加入一定量的盐酸时,K=8×10-5
B.25 ℃下,向该溶液中加入一定量的NaOH时,K=2×10-4
C.标准状况下,醋酸溶液中K=1.75×10-5
D.升高到一定温度,K=7.2×10-5
高二化学单选题简单题
已知25 ℃下,醋酸溶液中各微粒存在下述关系:K==1.75×10-5,下列有关说法可能成立的是( )
A.25 ℃下,向该溶液中加入一定量的盐酸时,K=8×10-5
B.25 ℃下,向该溶液中加入一定量的NaOH时,K=2×10-4
C.标准状况下,醋酸溶液中K=1.75×10-5
D.升高到一定温度,K=7.2×10-5
高二化学单选题简单题
已知25 ℃下,醋酸溶液中各微粒存在下述关系:K==1.75×10-5,下列有关说法可能成立的是( )
A.25 ℃下,向该溶液中加入一定量的盐酸时,K=8×10-5
B.25 ℃下,向该溶液中加入一定量的NaOH时,K=2×10-4
C.标准状况下,醋酸溶液中K=1.75×10-5
D.升高到一定温度,K=7.2×10-5
高二化学单选题简单题查看答案及解析
已知25℃,醋酸溶液中存在下述关系:K==1.75×10-5,则有关K的下列说法正确的是( )
A. 当向该溶液中加入一定量的硫酸时,K值增大 B. 升高温度,K值增大
C. 向醋酸溶液中加水,K增大 D. 向醋酸溶液中加氢氧化钠,K增大
高二化学单选题中等难度题查看答案及解析
已知25 ℃下,醋酸溶液中存在下述关系:K== 1.75×10-5 ,其中的数值是该温度下醋酸的电离平衡常数。有关K的下列说法正确的是
A、当向该溶液中加入一定量的硫酸时,K值增大
B、升高温度,K值增大
C、向醋酸溶液中加水,K增大
D、向醋酸溶液中加氢氧化钠,K增大
高二化学选择题中等难度题查看答案及解析
已知25 ℃下,醋酸溶液中存在下述关系:K=c(H+)·c(CH3COO-)/c(CH3COOH)=1.75×10-5,其中K是该温度下醋酸的电离平衡常数。有关K的下列说法正确的是
A. 当向该溶液中加入一定量的硫酸时,K值增大
B. 升高温度,K值增大
C. 向醋酸溶液中加水,K值增大
D. 向醋酸溶液中加氢氧化钠,恢复到25 ℃时,K值增大
高二化学单选题中等难度题查看答案及解析
已知25 ℃下,醋酸溶液中存在下述关系:K=c(H+)c(CH3COO-)/c(CH3COOH)=1.75×10-5,其中K的数值是该温度下醋酸的电离平衡常数。有关K的下列说法正确的是( )
A. 当向该溶液中加入一定量的硫酸时,K值增大
B. 升高温度,K值增大
C. 向醋酸溶液中加水,K值增大
D. 向醋酸溶液中加醋酸钠,K值减小
高二化学单选题中等难度题查看答案及解析
已知25℃下,醋酸稀溶液中存在CH3COOH H+ + CH3COO-,Ka=1.75×10-5。下列有关说法错误的是
A.加入冰醋酸Ka变小
B.升高温度Ka变大
C.通入HCl气体醋酸电离程度变小
D.加入少量NaOH固体,Ka不变
高二化学选择题中等难度题查看答案及解析
已知25℃下,醋酸稀溶液中存在CH3COOH⇌H++CH3COO﹣,Ka=1.75×10﹣5.下列有关说法错误的是
A.加入冰醋酸Ka变小
B.升高温度Ka变大
C.通入HCl气体醋酸电离程度变小
D.加入少量NaOH固体,Ka不变
高二化学选择题中等难度题查看答案及解析
已知25℃时,醋酸溶液中存在下述关系: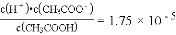
(1)当向该溶液中加入一定量盐酸时,上式中的数值是否发生变化_________ ?为什么_________?
(2)若醋酸的起始浓度为0.010 mol • L-1,平衡时c(H+)是多少_________?
高二化学填空题简单题查看答案及解析
向25mL0.1mol/LNaOH溶液中逐滴加入0.2mol/L醋酸溶液,曲线如下图所示。下列有关溶液中粒子浓度关系的描述中,错误的是( )

A. 在A、B间可能存在:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B. 在B点:a =12.5,且有c(Na+)=c(CH3COO-)
C. 在C点:c(CH3COO-) > c(Na+) >c(H+)>c(OH-)
D. 在D点:c(CH3COO-) + c(CH3COOH) = 2c(Na+)
高二化学单选题中等难度题查看答案及解析
25oC时,向25mL 一定浓度的 NaOH溶液中逐滴加入某浓度的 CH3COOH溶液,溶液pH和加入的醋酸溶液的体积关系曲线如图所示。下列有关混合溶液说法错误的是
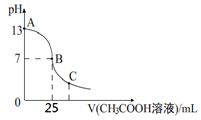
A.A、B间的溶液中可能有:c(Na+) > c(CH3COO-) > c(OH-) >c(H+)
B.B点: c(CH3COO-)=c(Na+)>c(OH-)=c(H+)
C.C点: c(CH3COO-)> c(Na+)> c(H+) > c(OH-)
D.NaOH溶液和醋酸溶液的浓度都恰好为0.1 mol·L-1
高二化学选择题中等难度题查看答案及解析