-
乙酸是生物油的主要成分之一,乙酸制氢具有重要意义:
热裂解反应:CH3COOH(g)→2CO(g)+2H2(g) △H=+213.7 kJ·mol-1
脱酸基反应 CH3COOH(g)→2CH4(g)+CO2(g) △H=-33.5 kJ·mol-1
(1)请写出CO与H2甲烷化的热化学方程式__________________________________。
(2)在密闭溶液中,利用乙酸制氢,选择的压强为________(填“较大”或“常压”)。
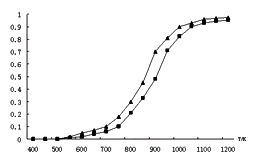
其中温度与气体产率的关系如图:
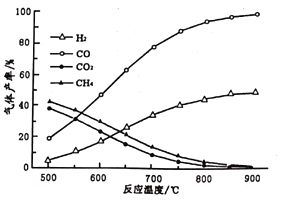
①约650℃之前,脱酸基反应活化能低速率快,故氢气产率低于甲烷;650℃之后氢气产率高于甲烷,理由是随着温度升高后,热裂解反应速率加快,同时_________________。
②保持其他条件不变,在乙酸气中掺杂一定量的水,氢气产率显著提高而CO的产率下降,请用化学方程式表示:____________________。
(3)若利用合适的催化剂控制其他的副反应,温度为T K时达到平衡,总压强为P kPa,热裂解反应消耗乙酸20%,脱酸基反应消耗乙酸60%,乙酸体积分数为________(计算结果保留1位小数);脱酸基反应的平衡常数Kp分别为________________kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
-
乙酸是生物油的主要成分之一,乙酸制氢具有重要意义:
热裂解反应:CH3COOH(g)→2CO(g)+2H2(g) △H=+213.7 kJ·mol-1
脱酸基反应 CH3COOH(g)→2CH4(g)+CO2(g) △H=-33.5 kJ·mol-1
(1)请写出CO与H2甲烷化的热化学方程式__________________________________。
(2)在密闭溶液中,利用乙酸制氢,选择的压强为________(填“较大”或“常压”)。
其中温度与气体产率的关系如图:
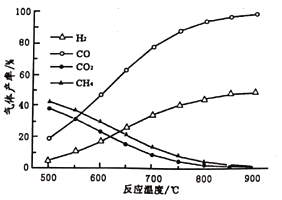
①约650℃之前,脱酸基反应活化能低速率快,故氢气产率低于甲烷;650℃之后氢气产率高于甲烷,理由是随着温度升高后,热裂解反应速率加快,同时_________________。
②保持其他条件不变,在乙酸气中掺杂一定量的水,氢气产率显著提高而CO的产率下降,请用化学方程式表示:____________________。
(3)若利用合适的催化剂控制其他的副反应,温度为T K时达到平衡,总压强为P kPa,热裂解反应消耗乙酸20%,脱酸基反应消耗乙酸60%,乙酸体积分数为________(计算结果保留1位小数);脱酸基反应的平衡常数Kp分别为________________kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
-
乙酸是生物油的主要成分之一,乙酸制氢具有重要意义:
热裂解反应CH3COOH(g)→2CO(g)+2H2(g) △H=+2l3.7KJ·mol-1
脱酸基反应CH3COOH(g)→CH4(g)+CO2(g) △H=-33.5KJ·mol-1
(1)请写出CO与H2甲烷化的热化学方程式_________________________________。
(2)在密闭容器中,利用乙酸制氢,选择的压强为___________(填“较大”或“常压”)。其中温度与气体产率的关系如图:
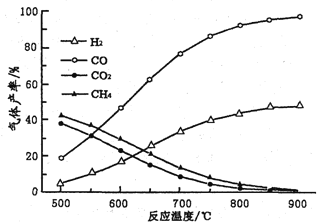
①约650℃之前,脱酸基反应活化能低速率快,故氢气产率低于甲烷;650℃之后氢气产率高于甲烷,理由是随着温度升高后,热裂解反应速率加快,同时______________________。
②保持其他条件不变,在乙酸气中掺杂一定量水,氢气产率显著提高而CO的产率下降,请用化学方程式表示:_________________________________。
(3)若利用合适的催化剂控制其他的副反应,温度为TK时达到平衡,总压强为PkPa,热裂解反应消耗乙酸20%,脱酸基反应消耗乙酸60%,乙酸体积分数为___________(计算结果保留l位小数);脱酸基反应的平衡常数Kp为___________kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
-
乙酸制氢具有重要意义:
热裂解反应:CH3COOH(g)=2CO(g)+2H2(g) ∆H=+213.7kJ·mol-1
脱羧基反应:CH3COOH(g)=CH4(g)+CO2(g) ∆H=−33.5kJ·mol-1
(1)2CO(g)+2H2(g)=CH4(g)+CO2(g) ∆H=____kJ·mol-1。
(2)在密闭容器中,利用乙酸制氢,选择的压强为_____(填“高压”或“常压”)。其中温度与气体产率的关系如图:
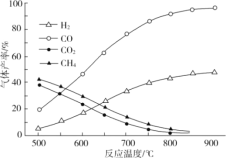
①约650℃之前,脱羧基反应活化能低,反应速率快,很快达到平衡,故氢气产率低于甲烷;650℃之后氢气产率高于甲烷,理由是____。
②保持其他条件不变,在乙酸气中掺杂一定量的水,氢气产率显著提高而CO的产率下降,请用化学方程式表示____。
(3)保持温度为T℃,压强为pkPa不变的条件下,在密闭容器中投入一定量的醋酸发生上述两个反应,达到平衡时热裂解反应消耗乙酸20%,脱羧基反应消耗乙酸60%,则平衡时乙酸体积分数为____(结果保留1位小数);脱羧基反应的平衡常数Kp为____kPa(结果保留1位小数)。
(4)光催化反应技术使用CH4和____(填化学式)直接合成乙酸,且符合“绿色化学”的要求(原子利用率100%)。
(5)若室温下将amol/L的CH3COOH溶液和bmo/LBa(OH)2溶液等体积混合,恢复室温后有2c(Ba2+)=c(CH3COO-),则乙酸的电离平衡常数Ka=____(用含a和b的代数式表示)。
-
甲烷以天然气和可燃冰两种主要形式存在于地球上,储量巨大,充分利用甲烷对人类的未来发展具有重要意义。
(1)乙炔(CH≡CH)是重要的化工原料。工业上可用甲烷裂解法制取乙炔,反应为:2CH4(g) C2H2(g)+ 3H2(g)。甲烷裂解时还发生副反应: 2CH4(g)
C2H2(g)+ 3H2(g)。甲烷裂解时还发生副反应: 2CH4(g) C2H4(g)+2H2(g)。甲烷裂解时,几种气体平衡时分压(Pa)的对数即lgP与温度(℃)之间的关系如图所示。
C2H4(g)+2H2(g)。甲烷裂解时,几种气体平衡时分压(Pa)的对数即lgP与温度(℃)之间的关系如图所示。
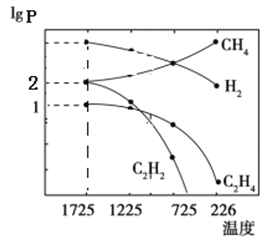
①1725℃时,向恒容密闭容器中充入CH4,达到平衡时CH4生成C2H2的平衡转化率为_______。
②1725℃时,若图中H2的lgP=5,则反应2CH4(g) C2H2(g)+ 3H2(g)的平衡常数Kp=_________(注:用平衡分压Pa代替平衡浓度mol/L进行计算)。
C2H2(g)+ 3H2(g)的平衡常数Kp=_________(注:用平衡分压Pa代替平衡浓度mol/L进行计算)。
③根据图判断,2CH4(g) C2H2(g)+3H2(g)△H_____0(填“>”或“<”)。由图可知,甲烷裂解制乙炔过程中有副产物乙烯生成。为提高甲烷制乙炔的产率,除改变温度外,还可采取的措施有_______。
C2H2(g)+3H2(g)△H_____0(填“>”或“<”)。由图可知,甲烷裂解制乙炔过程中有副产物乙烯生成。为提高甲烷制乙炔的产率,除改变温度外,还可采取的措施有_______。
(2)工业上用甲烷和水蒸气在高温和催化剂存在的条件下制得合成气(CO、H2),发生反应为:CH4(g)+H2O(g)  CO(g)+3H2(g) △H>0
CO(g)+3H2(g) △H>0
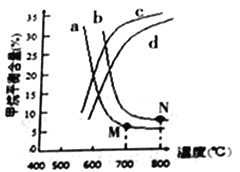
图中a、b、c、d四条曲线中的两条代表压强分别为1MPa、2MPa时甲烷含量曲线,其中表示1MPa的是________(填字母)。在实际生产中采用图中M点而不是N点对应的反应条件,运用化学反应速率和平衡知识,同时考虑实际生产,说明选择该反应条件的主要原因是__________。
(3)利用CH4、CO2在一定条件下重整的技术可得到富含CO的气体,在能源和环境上具有双重重大意义。重整过程中的催化转化原理如图所示:
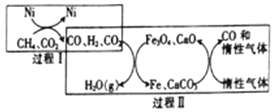
已知: CH4(g)+ H2O(g)  CO (g )+ 3H2(g) △H =+206.2 kJ/mol
CO (g )+ 3H2(g) △H =+206.2 kJ/mol
CH4(g)+ 2H2O(g)  CO2(g )+4H2(g) △H =+158.6 kJ/mol
CO2(g )+4H2(g) △H =+158.6 kJ/mol
则:
①过程II中第二步反应的化学方程式为__________。
②只有过程I投料比 =______,过程II中催化剂组成才会保持不变。
=______,过程II中催化剂组成才会保持不变。
③该技术总反应的热化学方程式为_______________。
-
(1)以甲醇为原料制取高纯H2具有重要的应用价值。甲醇水蒸气重整制氢主要发生以下两个反应:
主反应: ∆H=+49kJ∙mol-1
∆H=+49kJ∙mol-1
副反应: ∆H=+41kJ∙mol-1
∆H=+41kJ∙mol-1
①甲醇蒸气在催化剂作用下裂解可得到H2和CO,则该反应的热化学方程式为_________________,既能加快反应速率又能提高CH3OH平衡转化率的一种措施是______________。
②分析适当增大水醇比 对甲醇水蒸气重整制氢的好处是__________。
对甲醇水蒸气重整制氢的好处是__________。
③某温度下,将n(H2O):n(CH3OH)=1:1的原料气充入恒容密闭容器中,初始压强为P1,反应达平衡时总压强为P2,则平衡时甲醇的转化率为________________(忽略副反应,用含P1、P2的式子表示)。
(2)工业上用CH4与水蒸气在一定条件下制取H2,原理为: ∆H=+203kJ∙mol-1
∆H=+203kJ∙mol-1
①该反应逆反应速率表达式为:v逆=k·c(CO)·c3(H2),k为速率常数,在某温度下测得实验数据如下表:
| c(CO)/mol·L-1 | c(H2)/mol·L-1 | v逆/mol·L-1·min-1 |
| 0.05 | c1 | 4.8 |
| c2 | c1 | 19.2 |
| c2 | 0.15 | 8.1 |
由上述数据可得该温度下,该反应的逆反应速率常数k为_________L3·mol-3·min-1。
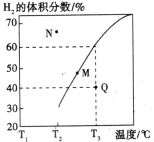
②在体积为3L的密闭容器中通入物质的量均为3mol的CH4和水蒸气,在一定条件下发生上述反应,测得平衡时H2的体积分数与温度关系如图所示:N点v正____________M点v逆(填“大于”或“小于”);Q点对应温度下该反应的平衡常数K=_______________mol2·L-2。平衡后再向容器中加入1molCH4和1molCO,平衡向_____________方向移动(填“正反应”或“逆反应”)。
-
已知:① 是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2
是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2 2CH3COOH;③已知乳酸E的结构简式为
2CH3COOH;③已知乳酸E的结构简式为 。现以A为主要原料合成乙酸乙酯,其合成路线如图所示:
。现以A为主要原料合成乙酸乙酯,其合成路线如图所示:
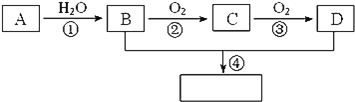
回答下列问题:
(1)A的电子式 ______,A结构简式______。
(2)B的结构简式 ______,D的结构简式 ______。
(3)B和D的分子中分别含 ______和______两种官能团(写名称)。
(4)写出下列反应的化学方程式并注明反应类型:
A→B ______; ______。
B→C______; ______。
B和D反应生成乙酸乙酯的反应并注明反应类型:______; ______。
-
CO2的回收利用对减少温室气体排放、改善人类生存环境具有重要意义。利用CO2和CH4重整可制合成气(主要成分CO、H2).重整过程中部分反应的热化学方程式为:
①CH4(g)=C(s)+2H2(g) △H=+75.0 kJ/mol
②CO2(g)+H2(g)=CO(g)+H2O(g) △H=+41.0 kJ/mol
③CO(g)+H2(g)=C(s)+H2O(g) △H=-131.0kJ/mol
(1)反应CO2(g)+CH4(g)=2CO(g) + 2H2(g)的△H=____________;
(2)固定n(CO2)= n(CH4),改变反应温度,CO2和CH4的平衡转化率见下左图。
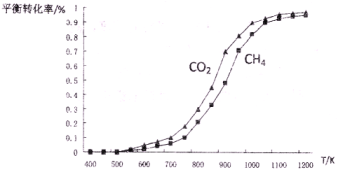
①同温度下CO2的平衡转化率____________(填“大于”或“小于”)CH4的平衡转化率,其原因是____________;
②高温下进行该反应时常会因反应①生成“积碳”(碳单质),造成催化剂中毒,高温下反应①能自发进行的原因是____________。
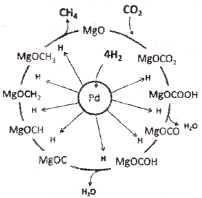
(3)一定条件下Pd-Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如上右图所示,该反应的化学方程式为____________,反应过程中碳元素的化合价为-2价的中间体是____________。
(4)卤水可在吸收烟道气中CO2的同时被净化,实现以废治废,其中涉及的一个反应是CaSO4 + Na2CO3=CaCO3 + Na2SO4,则达到平衡后,溶液中c(CO32-)/c(SO42-)=____________[用Ksp(CaSO4)和Ksp(CaCO3)表示]
-
CO2的回收利用对减少温室气体排放、改善人类生存环境具有重要意义。利用CO2和CH4重整可制合成气(主要成分CO、H2),重整过程中部分反应的热化学方程式为: ①CH4(g) = C(s) + 2H2(g) △H = +75.0 kJ·mol-1
②CO2(g) + H2(g) = CO(g) + H2O(g) △H = +41.0 kJ·mol-1
③CO(g) + H2(g) = C(s) + H2O(g) △H = -131.0 kJ·mol-1
(1)反应CO2(g) + CH4(g) = 2CO(g) + 2H2(g)的△H= ___________。
(2)固定n(CO2)= n(CH4),改变反应温度,CO2和CH4的平衡转化率见下图。
①同温度下CO2的平衡转化率 ____________(填“大于”或“小于”)于CH4的平衡转化率,其原因是 __________________________。
②高温下进行该反应时常会因反应①生成“积碳”(碳单质),造成催化剂中毒,高温下反应①能自发进行的原因是_________________。
(3)一定条件下Pd-Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如图所示,该反应的化学方程式为_____________________,反应过程中碳元素的化合价为-2价的中间体是__________。

(4)卤水可在吸收烟道气中CO2的同时被净化,实现以废治废,其中涉及的一个反应是CaSO4 + Na2CO3 == CaCO3 + Na2SO4,则达到平衡后,溶液中c(CO32-)/c(SO42-) = __________。【用Ksp(CaSO4)和Ksp(CaCO3)表示】
-
(16分)实现反应CH4(g)+CO2(g) 2CO(g)+2H2(g),△H0,对减少温室气体排放和减缓燃料危机具有重要意义。
2CO(g)+2H2(g),△H0,对减少温室气体排放和减缓燃料危机具有重要意义。
(1)已知:① 2CO(g)+O2(g)=2CO2(g) △H1=-566 kJ·mol-1
② 2H2(g)+O2(g)=2H2O(g) △H2=-484 kJ·mol-1
③ CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3=-802 kJ·mol-1
则△H0= kJ·mol-1
(2)在密闭容器中,通入2.5mol的CH4与2.5mol CO2,一定条件下发生反应:CH4(g)+CO2(g) 2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如图。
2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如图。
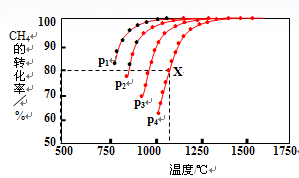
据图可知,p1、p2、 p3、p4由大到小的顺序 。
(3)CO和H2还可以通过反应C(s)+H2O(g) CO(g)+H2 (g) 制取。
CO(g)+H2 (g) 制取。
① 在恒温恒容下,若从反应物出发建立平衡,已达到平衡的是
A.体系压强不再变化 B.CO与H2的物质的量之比为1:1
C.混合气体的密度保持不变 D.每消耗1mol H2O(g)的同时生成1mol H2
② 恒温下,在2L的密闭容器中同时投入四种物质,10min时达到平衡,测得容器中有1mol H2O(g)、1mol CO(g)、2molH2(g)和2molC(s),反应的平衡常数K= 。
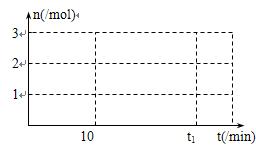
若此时增大压强,平衡将向 (填“正”、“逆”)反应方向移动,t1min时达到新的平衡。
③ 请画出增大压强后10min~t1min时容器中H2物质的量n随时间变化的曲线图。