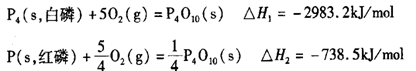-
(1)已知拆开1mo1H-H键、1molN≡N键、lmolN-H键分别需要吸收的能量为436kJ、946kJ、391kJ。则生成1mo1 NH3时反应放出______________kJ 的热量。
(2)天然气既是高效洁净的能源,也是重要的化工原料。
①甲烷分子的结构式为_________,空间构型为_______________。
②甲烷高温分解生成氢气和炭黑。在密闭容器中进行此反应时要通入适量空气使部分甲烷燃烧,其目的是__________________________________________。
(3)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的的是________(填序号)。
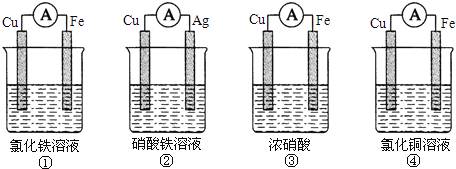
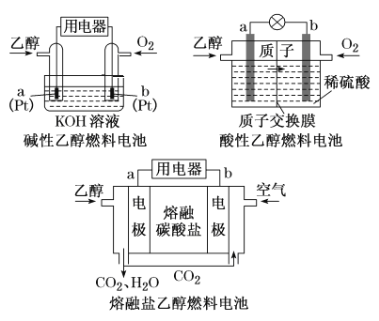
(4)直接乙醇燃料电池(DEFC)具有很多优点,引起了人们的研究兴趣。现有以下三种乙醇燃料电池。
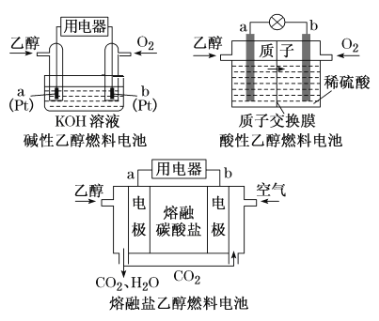
①三种乙醇燃料电池中正极反应物均为______________________;
②碱性乙醇燃料电池中,电极a上发生的电极反应式为_______________________;
③熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电池工作时,电极b上发生的电极反应式为_______________________________________________。
-
(1)已知拆开1mo1H-H键、1molN≡N键、lmolN-H键分别需要吸收的能量为436kJ、946kJ、391kJ。则生成1mo1 NH3时反应放出______________kJ 的热量。
(2)天然气既是高效洁净的能源,也是重要的化工原料。
①甲烷分子的结构式为_________,空间构型为_______________。
②甲烷高温分解生成氢气和炭黑。在密闭容器中进行此反应时要通入适量空气使部分甲烷燃烧,其目的是__________________________________________。
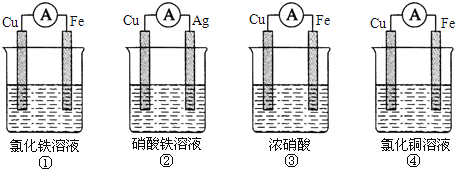
(3)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的的是________(填序号)。
(4)直接乙醇燃料电池(DEFC)具有很多优点,引起了人们的研究兴趣。现有以下三种乙醇燃料电池。
①三种乙醇燃料电池中正极反应物均为______________________;
②碱性乙醇燃料电池中,电极a上发生的电极反应式为_______________________;
③熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电池工作时,电极b上发生的电极反应式为_______________________________________________。
-
拆开1molH-H键、1molN-H键、1mol氮氮三键分别需要能量436kJ、391kJ、946kJ,
则(1)1molN2生成NH3的反应热是 ________,
(2)1molH2生成NH3的反应热是 ________。
-
按要求回答下列问题
(1)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为____________________。
(2)已知碳的燃烧热ΔH1= a kJ·mol-1,S(s)+2K(s)=K2S(s);ΔH2= b kJ·mol-12K(s)+N2(g)+3O2(g)=2KNO3(s) ΔH3= c kJ·mol-1,则S(s)+2KNO3(s)+3C(s)=K2S(s)
+N2(g)+3CO2(g) ΔH=____________________。
(3)已知:C(s)+O2(g)=CO2(g) ΔH=-437.3 kJ·mol一1,H2(g)+1/2O2(g)=H2O(g) ΔH=-285.8 kJ·mol一1,CO(g)+1/2O2(g)=CO2(g) ΔH=-283.0 kJ·mol一1,写出煤气化(碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式________,计算10m3(标况)水煤气完全燃烧放出的热量为_________kJ(结果保留到小数点后一位)。
-
(6分)(1)已知拆开1molH-H键,lmolN-H键,1mol 键分别需要的能是436kJ、39lkJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________________。
键分别需要的能是436kJ、39lkJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________________。
(2)科学家盖斯曾提出:“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的。”利用盖斯定律可测某些特别反应的热效应。已知:
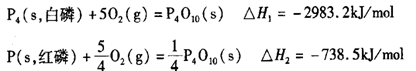
则白磷的稳定性比红磷_____________(填“高”或“低”),理由是________________
__________________________________________________________________________。
-
断开1 mol H—H键, 1 mol N—H键、1 mol N≡N键分别需要吸收的能量为436 kJ、391 kJ、946 kJ,求:
(1)1 mol N2生成NH3需_____ (填“吸收”或“放出”)能量_____ kJ。
(2)1 mol H2生成NH3需_____ (填“吸收”或“放出”)能量_____ kJ。
-
合成氨的能量示意图如下:
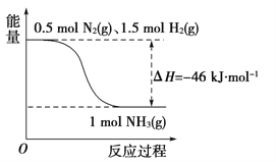
(1)已知分别破坏1 mol N N键、1 mol H-H键时需要吸收的能量为946 kJ、436 kJ,则破坏1 mol N-H键需要吸收的能量为________ kJ。
N键、1 mol H-H键时需要吸收的能量为946 kJ、436 kJ,则破坏1 mol N-H键需要吸收的能量为________ kJ。
(2)N2H4可视为NH3分子中的H被—NH2取代的产物。发射卫星时以N2H4(g)为燃料、NO2为氧化剂,二者反应生成N2和H2O(g)。
已知:N2(g)+2O2(g)===2NO2(g)ΔH1=+67.7 kJ·mol-1
N2H4(g)+O2(g)===N2(g)+2H2O(g)ΔH2=-534 kJ·mol-1
则1 mol N2H4与NO2完全反应的热化学方程式为____________________________________。
-
已知拆开 1mol H-H键、1mol I-I、1mol H-I 键分别需要吸收的能量为436kJ、151kJ、299k J.则由氢气和碘反应生成 1mol HI需要________(填“放出”或“吸收”)________k J的热量.
-
(1)已知断开 1mol H2中的化学键需吸收436kJ热量,断开1mol Cl2中的化学键需要吸收243kJ能量,而形成1mol HCl分子中的化学键要释放431kJ能量,试求1mol H2与1mol Cl2反应的能量变化.△H=______.
(2)已知常温时,0.1mol/L某一元酸HA在水中有0.1%发生电离,则该溶液的PH=______,此酸的电离平衡常数K=______,由HA电离出来的H+的浓度约为水电离出来的H+的浓度的______倍.
-
氨气在产生、生活中都有广泛用途,所以,化学学习中对氨气认识十分重要。
(1)已知H-H键、N-H键、N≡N键的键能分别是436kJ/mol、391kJ/mol、946kJ/mol,合成氨的热化学方程式为_____________。
(2)下列方法可以证明 N2(g)+3H2(g) 2NH3(g)已达平衡状态的是____。
2NH3(g)已达平衡状态的是____。
①单位时间内生成n mol H2同时生成n molNH3
②单位时间内3molH—H键断裂同时有6 mol H—N键断裂
③温度和体积一定时,容器内压强不再变化
④c(N2)︰c(H2)︰c(NH3)=1︰3︰2
⑤反应速率2v(H2)= 3v(NH3)
⑥条件一定,混合气体的平均相对分子质量不再变化
⑦温度和体积一定时,混合气体的密度不再变化
(3) 25 ℃时,将工业生产中产生的NH3溶于水得0.1mol/L氨水20.0 mL,测得pH=11,则该条件下,NH3•H2O的电离平衡常数约为__________。向此溶液中加入少量的氯化铵固体时,[c(NH3•H2O) • c(H+)] / c(NH4+)值将______(“增大”“减小”或“不变”)。
(4)若向该氨水中逐滴加入等浓度的盐酸,溶液中pH与pOH(pOH=-lg[OH-])的变化关系如图所示。
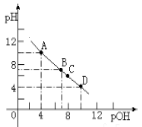
B点所加盐酸的体积_____(填“>”、“=”或“<”) 20.0 mL。C点溶液中离子浓度大小顺序为_____>____>_____>_____。
(5)常温下,向0.001mol/LAlCl3溶液中通入NH3直至过量,当pH=_________时,开始生成沉淀(已知:Ksp[Al(OH)3]=1.0×10-33)。