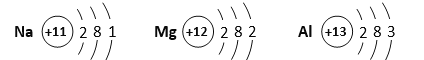-
化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)电动汽车上用的铅蓄电池是以一组充满海绵状态铜的铅板和另一组结构相似的充满二氧化铅的铅板组成,用H2SO4作电解液。放电时总反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。
①写出放电时负极的电极反应式:__。
②铅蓄电池放电时,溶液的pH将_(填增大、减小或不变);当外电路上有0.5mol电子通过时,溶液中消耗H2SO4的物质的量为__。
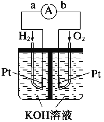
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。其正极反应方程式为___;若将负极材料改为CH4,写出其负极反应方程式__。
(3)法国格勒诺布尔(Grenoble)约瑟夫﹒傅立叶大学的研究小组发明了第一块可植入人体为人造器官提供电能的葡萄糖生物燃料电池,其基本原理是葡萄糖和氧气在人体中酶(蛋白质)的作用下发生反应:C6H12O6+6O2 6CO2+6H2O(酸性环境)。下列有关该电池的说法正确的是__。
6CO2+6H2O(酸性环境)。下列有关该电池的说法正确的是__。
A.该生物燃料电池不能在高温下工作
B.该电池负极的电极反应式为:C6H12O6+6H2O-24e-=6CO2↑+24H+
C.消耗1mol氧气时转移4mol电子,H+向负极移动
D.提高葡萄糖生物燃料电池的效率,可使其在将来为更多可植入医疗设备提供电能
(4)1958年世界上第一个心脏起搏器在瑞典植入人体成功,使用寿命长达10年之久。这种能源起搏器中安装寿命最长、可靠性最高的锂—碳电池,这种电池容量大,电压稳定,能在-56.7~71.1℃温度范围内正常工作。现已在火箭、移动电话、笔记本电脑中广泛使用。它采用锂和石墨作电极,四氯化铝锂(LiAlCl4)溶解在亚硫酰氯中(SOCl2)组成电解质溶液。电池总反应为:8Li+3SOCl2=6LiCl+Li2SO3+2S,此电池中___作正极,负极的电极反应为__。
-
化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据构成原电池的本质判断,下列化学反应方程式正确且能设计成原电池的是_________。
A.KOH + HCl = KCl + H2O B. Cu + Fe3+ = Fe2+ + Cu2+
C.Na2O + H2O = 2NaOH D.Fe + H2SO4 = FeSO4 + H2↑
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(如下图)。有关实验现象,下列说法正确的是:______。
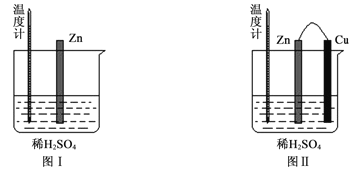
A.图I中温度计的示数高于图II的示数
B.图I和图II中温度计的示数相等,且均高于室温
C.图I和图II的气泡均产生于锌棒表面
D.图II中产生气体的速度比I慢
(3)电动汽车上用的铅蓄电池是以一组充满海绵状态铜的铅板和另一组结构相似的充满二氧化铅的铅板组成,用H2SO4作电解质溶液。放电时总反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O
①写出放电时正极的电极反应式:___________;
②铅蓄电池放电时,负极质量将_______(填“增大”、“减小”或“不变”)。当外电路上有2mol电子通过时,溶液中消耗H2SO4的物质的量为_________。
-
化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据构成原电池的本质判断,下列方程式正确且能设计成原电池的是________。
A.KOH+HCl=KCl+H2O
B.Cu+Fe3+=Fe2++Cu2+
C.Na2O+H2O=2NaOH
D.Fe+H2SO4=FeSO4+H2
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(图Ⅰ、图Ⅱ中除连接的铜棒不同外,其他均相同)。有关实验现象,下列说法正确的是___________。

A.图Ⅰ中温度计的示数高于图Ⅱ的示数
B.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温
C.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面
D.图Ⅱ中产生气体的速度比Ⅰ快
(3)将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80,工作一段时间后,取出二者洗净,干燥后称重,总质量为54g,则产生氢气的体积_____mL(标准状况)
(4)将铝片和镁片放入氢氧化钠溶液中,负极的电极反应式为:______________
-
根据已经学过的化学知识,回答下列问题。
I.金属及其化合物在生产生活中有着广泛的应用,
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现_______性;_______(填“能”或“不能”)用氢氧化钠溶液代替。
(2)将Cu与稀硫酸混合,二者不能反应,滴入H2O2后,溶液很快变成蓝色,该反应的化学方程式为____________________________________________。
(3)NaHSO4是一种酸式盐,写出NaHSO4在水中的电离方程式_________________________。
II.物质的量是学习化学的基础。
(1)14.4 g CO和CO2的混合气体在标准状况下所占的体积为8.96 L,其中CO的质量为_____。
(2)市售浓H2SO4的质量分数为98%、密度为1.84g/cm3,其浓度为________mol·L-1。
(3)19g某二价金属的氯化物ACl2中含有0.4mo1Cl-离子,金属A的相对原子质量是_______。
(4)根据反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知当有2.5 mol FeS2参加反应时,被氧化的硫的物质的量为_______mol。
-
(14分)铁、铝、铜、硅及其合金材料在生产生活中有着广泛的应用。请回答下列有关问题。
(1)目前已冶炼出纯度达99.9999%的铁。下列关于纯铁的叙述错误的是
(填字母)。
A.硬度比钢小,熔点比钢高 B.不能与盐酸反应
C.与不锈钢成分相同 D.在冷的浓硫酸中钝化
E.在潮湿的空气中放置不易生锈
(2)铝热反应可用于焊接钢轨、冶炼熔点较高的金属。请写出用V2O5冶炼钒的化学方程式:
(3)①铜在干燥的空气中性质稳定,在潮湿的空气里会被锈蚀形成一层绿色的铜锈,反应的化学方程式是
②工业上常以黄铜矿为原料,采用火法溶炼工艺生产铜。该工艺的中间过程会发生反应:2Cu2O+Cu2S 6Cu+SO2↑,该反应的氧化剂是
6Cu+SO2↑,该反应的氧化剂是
③将铜粉放入稀硫酸中加热并不断鼓入空气,铜溶解,产物只有硫酸铜与水 。
该反应的化学方程式: ,
此法比直接用浓硫酸与铜反应有两个明显的优点:
。
(4)制备高纯硅的流程如下图:

写出石英砂制备粗硅的化学方程式:
。
-
金属铝在生产生活中有着广泛的用途。回答下列问题:
(1)铝元素在周期表中的位置是_______________。
(2)比较原子结构示意图:它们的共同之处是___________ 选填编号,下同
选填编号,下同 ;不同之处是___________。
;不同之处是___________。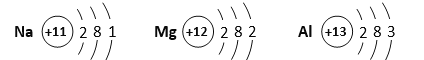
a.电子层数 b.次外层电子数 c.最外层电子数 d.质子数
(3)常温下铝制容器可以用来盛放浓硫酸而不被溶解,这种现象称为___________。
氢氧化铝和盐酸反应的化学方程式为_________________________________。
能把溶液中的铁离子和铝离子分离开的试剂是___________。 选填编号
选填编号
a.盐酸 b.硫酸铜溶液 c.氨水 d.氢氧化钠溶液
-
化学在生活中有着广泛的应用,下列对应关系正确的个数是( )
①Na2O2吸收CO2产生O2,可用作呼吸面具供氧剂 ②ClO2具有还原性,可用于自来水的杀菌消毒 ③SiO2硬度大,用于制造光导纤维 ④NH3易溶于水,可用作制冷剂 ⑤次氯酸盐具有氧化性,因而能漂白织物 ⑥二氧化硅是酸性氧化物,它不溶于任何酸 ⑦SO2具有还原性,可用于漂白纸浆 ⑧晶体硅是半导体材料,可做晶体管
A. 1 B. 2 C. 3 D. 4
-
化学知识在生产、生活中有着广泛的应用。下列说法中不正确的是
A. 用杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,作家庭燃气
B. 手机中使用的锂离子电池属于二次电池
C. 大力发展火力发电,解决电力紧张问题
D. 开发高效氢能、太阳能等新型电动汽车,以解决城市机动车尾气排放问题
-
铝及其化合物在生产生活中具有重要的作用。
(1)铝属于活泼金属却能在空气中稳定存在,原因是(用化学用语及相关文字说明)___。
(2)铝电池性能优越,在现代生产、生活中有广泛的应用。铝—空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。
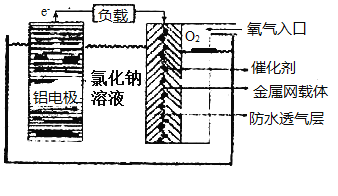
该电池的正极反应方程式为___,当铝电极质量减少9克,则另一极通入的氧气的体积在标准状况下为___。
(3)AlCl3与NaN3在高温下反应可制得高温结构陶瓷氮化铝(AlN),且生成N2。写出反应化学方程式为___。
(4)在元素周期表中,砷位于铝的下一周期,与氮元素同主族,写出AsH3分子的电子式为___,相同压强下,AsH3的沸点___NH3(填“大于”或“小于”)。
-
铅蓄电池是广泛应用于汽车、柴油机车等的启动电源。产生电能时的电极反应分别为:
Pb+SO42―–2e―=PbSO4 ①
PbO2+4H++SO42―+2e―=PbSO4+2H2O ②
下列有关铅蓄电池的说法不正确的是:
A.①式表示负极反应,②式表示正极反应
B.铅蓄电池的电解质溶液是硫酸溶液,在放电过程中,它的浓度逐渐降低
C.铅蓄电池在放电时,电子从Pb通过导线流向PbO2
D.铅蓄电池在充电时,原来负极发生的反应是:Pb+SO42―–2e―=PbSO4