-
(1)已知2 mol氢气燃烧生成液态水时放出572 kJ热量,反应方程式是
2H2(g)+O2(g)==2H2O(l)
(l)请回答下列问题:
①该反应的生成物能量总和________(填“大于”、“小于”或“等于”)反应物能量总和。
②若2 mol氢气完全燃烧生成水蒸气,则放出的热量________(填“>”、“<”或“=”)572 kJ。
③与化石燃料相比,利用氢能源有很多优点,请说出其中一点______________________。
(2)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g) 2SO3(g) ΔH1=-197 kJ·mol-1;
2SO3(g) ΔH1=-197 kJ·mol-1;
H2O(g)===H2O(l) ΔH2=-44 kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)===2H2SO4(l)ΔH3=-545 kJ·mol-1
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是_________________________________________。
-
按要求回答问题:
(1)氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)=2H2O(1),生成2mol液态水放出572kJ的能量,请回答下列问题:
①生成物能量总和___(填“大于”“小于”或“等于”)反应物能量总和。
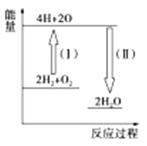
②反应2H2+O2 2H2O的能量变化如图所示。已知拆开1mol H2、1mol O2和1mol H—O中的化学键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)____(填“吸收”或“放出”)___kJ。
2H2O的能量变化如图所示。已知拆开1mol H2、1mol O2和1mol H—O中的化学键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)____(填“吸收”或“放出”)___kJ。
(2)一定温度下,在容积为2L的密闭容器中进行反应:aN(g) bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
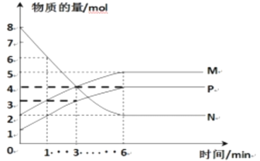
①反应化学方程式中各物质的系数比为a:b:c=____。
②1min到3min这段时刻,以M的浓度变化表示的平均反应速率为:_______。
③下列叙述中能说明上述反应达到平衡状态的是_________。
A 反应中当M与N的物质的量相等时
B P的质量不随时间变化而变化
C 混合气体的总物质的量不随时间变化而变化
D 单位时间内每消耗a mol N,同时消耗b mol M
E 混合气体的压强不随时间的变化而变化
M 的物质的量浓度保持不变
-
已知 1g 氢气燃烧生成液态水放出 142.9 kJ 热量,下列热化学方程式书写正确的是
A. 2H2(g) + O2(g) = 2H2O(l) △H = -142.9 kJ· mol-1
B. H2O(l) = H2(g) + 1/2O2(g) △H = 285.8 kJ· mol-1
C. 2H2 + O2 = 2H2O △H = -571.6 kJ· mol-1
D. H2(g) + 1/2O2(g) = H2O(g) △H = -285.8 kJ· mol-1
-
(6分)氢气燃烧生成液态水的热化学方程式是:2H2(g)+O2(g) ===2H2O(l);ΔH=-572kJ/mol 请回答下列问题:
(1)生成物能量总和 (填“大于”、“小于”或“等于”)反应物能量总和。
(2)若2 mol氢气完全燃烧生成水蒸气,则放出的热量________572 kJ (填“>”、“<”或“=”)。
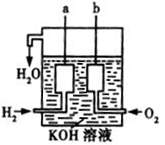
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示,a、b两个电极均由多孔的碳块组成。它是将 ________ 能转化为 能的装置。
-
(4分)氢气燃烧生成液态水的热化学方程式是:
2H2(g)+O2(g) ===2H2O(l) ΔH=-572kJ/mol
请回答下列问题:
(1)生成物能量总和 (填“大于”、“小于”或“等于”)反应物能量总和。
(2)若2 mol氢气完全燃烧生成水蒸气,则放出的热量________(填“>”、“<”或“=”)572 kJ。
-
Ⅰ.氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ/mol 请回答下列问题:
(1)生成物能量总和 (填“大于”、“小于”或“等于”)反应物能量总和
(2)若2 mol氢气完全燃烧生成水蒸气,则放出的热量________572 kJ(填“>”、“<”或“=”)
Ⅱ.已知1molCu(s)与适量O2(g)发生反应,生成CuO(s),放出157kJ热量。写出该反应的热化学方程式________。
-
水是生命之源,也是化学反应中的主角。请回答下列问题:
Ⅰ、氢气燃烧生成液态水热化学方程式是2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ/mol。
(1)生成物能量总和(填“大于”、“小于”或“等于”)反应物能量总和。
(2)若2 mol氢气完全燃烧生成水蒸气,则放出的热量________572 kJ(填“>”、“<”或“=”)。
(3)氢气热值为________。
Ⅱ、氢气和氧气反应生成水,将化学能转化为电能,其构造如图所示:a、b两个电极均由多孔的碳块组成。
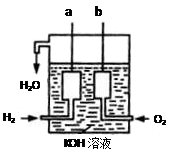
(1)a电极反应式是________
(2)b电极反应式是________
Ⅲ、如图表示一个电解池。X、Y都是惰性电极,电解液a是饱和食盐水,同时在两边各滴入几滴酚酞试液。
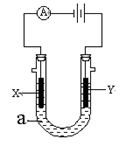
(1)X极上的电极反应式为________,
在X极附近观察到的现象是________。
(2)Y极上的电极反应式为,
检验该电极反应产物的方法是________。
-
氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)═2H2O(l)△H=-572kJ/mol
请回答下列问题:
(1)生成物能量总和______(填“大于”、“小于”或“等于”)反应物能量总和.
(2)若2mol氢气完全燃烧生成水蒸气,则放出的热量______(填“>”、“<”或“=”)572kJ.
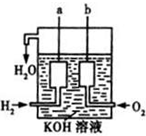
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如右图所示:a、b两个电极均由多孔的碳块组成.它的负极反应物为______,当正极消耗5.6L(标准状况)气体时,外电路转移的电子数为______.
-
氢气燃烧生成液态水的热化学方程式是:2H2(g)+O2(g)═2H2O(l)△H=-572kJ/mol请回答下列问题:
(1)生成物能量总和________(填“大于”、“小于”或“等于”)反应物能量总和.
(2)若2mol氢气完全燃烧生成水蒸气,则放出的热量________(填“>”、“<”或“=”)572kJ.
-
水是生命之源,也是化学反应中的主角.请回答下列问题:
Ⅰ、氢气燃烧生成液态水热化学方程式是2H2(g)+O2(g)═2H2O(l)△H=-572kJ/mol,
(1)生成物能量总和________(填“大于”、“小于”或“等于”)反应物能量总和.
(2)若2mol氢气完全燃烧生成水蒸气,则放出的热量________572kJ(填“>”、“<”或“=”).
(3)氢气热值为________.
Ⅱ、氢气和氧气反应生成水,将化学能转化为电能,其构造如图1所示:a、b两个电极均由多孔的碳块组成,
(1)a电极反应式是________
(2)b电极反应式是________
Ⅲ、图2表示一个电解池.X、Y都是惰性电极,电解液a是饱和食盐水,同时在两边各滴入几滴酚酞试液.
(1)X极上的电极反应式为________,在X极附近观察到的现象是________.
(2)Y极上的电极反应式为________,检验该电极反应产物的方法是________.

2SO3(g) ΔH1=-197 kJ·mol-1;






