-
[化学——选修3:物质结构与性质]
技术人员晒制蓝图时,用K3Fe(C2O4)3]·H2O(三草酸合铁酸钾)作感光剂,再以K3[Fe(CN)6]氰合铁酸钾)溶液作显影剂。请回答以下问题:
(1)铁元素在周期表中位置为___________,Fe3+的基态价电子排布图为___________。
(2)在上述两种钾盐中第一电离能最大的元素为___________,电负性最小的元素为___________。
(3)H2C2O4分子屮碳原子的杂化类型是___________,与C2O42-互为等电子体的分子的化学式为___________(写一种)。
(4)在分析化学中F-常用于Fe3+的掩蔽剂,因为生成的FeF63-十分稳定,但Fe3+却不能与I-形成配合物,其原因是______________________(用离子方程式来表示)。
(5)已知C60分子结构和C60晶胞如右图所示:
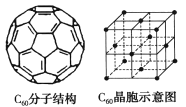
①1个C60分子中含有π键的数目为___________。
②晶胞中C60的配位数为___________。
③已知C60晶胞参数为apm,则该晶胞密度的表达式是___________g·cm-3(NA代表阿伏加德罗常数)。
-
[化学——选修3:物质结构与性质]
技术人员晒制蓝图时,用K3Fe(C2O4)3]·H2O(三草酸合铁酸钾)作感光剂,再以K3[Fe(CN)6]氰合铁酸钾)溶液作显影剂。请回答以下问题:
(1)铁元素在周期表中位置为___________,Fe3+的基态价电子排布图为___________。
(2)在上述两种钾盐中第一电离能最大的元素为___________,电负性最小的元素为___________。
(3)H2C2O4分子屮碳原子的杂化类型是___________,与C2O42-互为等电子体的分子的化学式为___________(写一种)。
(4)在分析化学中F-常用于Fe3+的掩蔽剂,因为生成的FeF63-十分稳定,但Fe3+却不能与I-形成配合物,其原因是______________________(用离子方程式来表示)。
(5)已知C60分子结构和C60晶胞如右图所示:
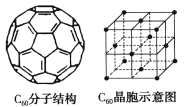
①1个C60分子中含有π键的数目为___________。
②晶胞中C60的配位数为___________。
③已知C60晶胞参数为apm,则该晶胞密度的表达式是___________g·cm-3(NA代表阿伏加德罗常数)。
-
[化学——选修3:物质结构与性质]
决定物质性质的重要因素是物质结构。请回答下列问题。
(1)+3价Cr的配合物K[Cr(C2O4)2(H2O)2]中,配体是___________,与C2O42-互为等电子体的分子是(填化学式)_______________。

(2)CaO晶胞如图所示,与每一个钙离子距离最近并且距离相等的钙离子有_________个 ;CaO晶体和NaCl晶体的晶格能分别为:CaO:3401 kJ/mol、NaCl:786 kJ/mol。 导致两者晶格能差异的主要原因__________________。
(3)Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)反应过程中,断裂的化学键类型是__________,则形成的化学键类型是 。
(4)从不同角度观察MoS2的晶体结构见图。已知:Mo位于第五周 期VIB族。
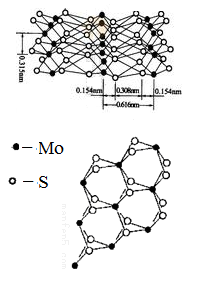
①下列说法正确的是__________
A.晶体硅中硅原子的轨道杂化类型为sp2
B.电负性:C<S
C.晶体硅和C60比较,熔点较高的是C60
D.Mo元素基态原子的价电子排布式为4d55s1
E.MoS2的晶体中每个Mo原子周围距离最近的S原子数目为4
F.MoS2的晶体中Mo-S之间的化学键为极性键、配位键、范德华力
②根据MoS2的晶体结构回答:MoS2纳米粒子具有优异的润滑性能,其原因是_____________ .
-
文献表明:工业上,向炽热铁屑中通入HCl生产无水FeCl2;相同条件下,草酸根(C2O42-)的还原性强于Fe2+。某化学研究性小组进行以下实验检验这一结论并测定三草酸合铁酸钾晶体[K3Fe(C2O4)3・xH2O]中草酸根含量和结晶水含量。用如图所示装置制取无水FeCl2
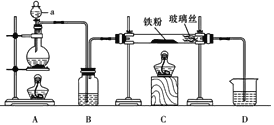
(1)仪器a的名称为___________,B中的试剂为___________。
(2)欲制得纯净的FeCl2,实验过程需先点燃A处酒精灯,原因是__________________。
(3)若用D的装置进行尾气处理,存在的问题是_______________、_________________。
(4)某小组设计使用如图装置直接比较Fe2+和C2O42-的还原性强弱,并达到了预期的目的。
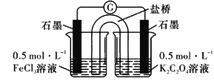
左池石墨电极为_________极,写出右池电极反应式:_______________。
(5)为测定三草酸合铁酸钾晶体中草酸根的含量和结晶水的含量,进行了如下实验:
滴定过程:①称量m g三草酸合铁酸钾晶体样品,配制成250mL溶液。
②取所配溶液25.00mL于锥形瓶中,滴加酸性KMnO4溶液滴定,恰好消耗V mL a mol•L-1KMnO4溶液。C2O42-被全部转化的现象是__________。
③该晶体中C2O42-的质量分数为_____________。
误差若盛放酸性KMnO4溶液的滴定管未用标准液润洗,会使结晶水x的数值_______。(填“偏高”“偏低”“无影响”)
-
文献表明:工业上,向炽热铁屑中通入HCl生产无水FeCl2;相同条件下,草酸根(C2O42-)的还原性强于Fe2+。某化学研究性小组进行以下实验检验这一结论并测定三草酸合铁酸钾晶体[K3Fe(C2O4)3・xH2O]中草酸根含量和结晶水含量。用如图所示装置制取无水FeCl2
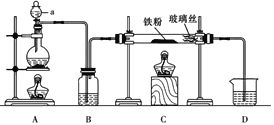
(1)仪器a的名称为___________,B中的试剂为___________。
(2)欲制得纯净的FeCl2,实验过程需先点燃A处酒精灯,原因是__________________。
(3)若用D的装置进行尾气处理,存在的问题是_______________、_________________。
(4)某小组设计使用如图装置直接比较Fe2+和C2O42-的还原性强弱,并达到了预期的目的。
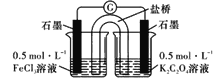
左池石墨电极为_________极,写出右池电极反应式:_______________。
(5)为测定三草酸合铁酸钾晶体中草酸根的含量和结晶水的含量,进行了如下实验:
滴定过程:①称量m g三草酸合铁酸钾晶体样品,配制成250mL溶液。
②取所配溶液25.00mL于锥形瓶中,滴加酸性KMnO4溶液滴定,恰好消耗V mL a mol•L-1KMnO4溶液。C2O42-被全部转化的现象是__________。
③该晶体中C2O42-的质量分数为_____________。
误差若盛放酸性KMnO4溶液的滴定管未用标准液润洗,会使结晶水x的数值_______。(填“偏高”“偏低”“无影响”)
-
文献表明,相同条件下,草酸根(C2O42-)的还原性强于Fe2+,为检验这一结论,完成如下实验.
资料:i.草酸(H2C2O4)为二元弱酸
ii.三水三草酸合铁酸钾[K3Fe(C2O4)3·3H2O]为翠绿色晶体,光照易分解,其水溶液中存在: Fe(C2O4)33- Fe3++3C2O42-K=6.3×10-21
Fe3++3C2O42-K=6.3×10-21
iii.FeC2O4·2H2O为黄色固体,微溶于水,可溶于强酸
(实验1)通过Fe3+和C2O42—在溶液中的反应比较Fe2+和C2O42-的还原性强弱。

(1)C2O42-中碳元素的化合价是___________。
(2)取实验 1 中少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。继续加入硫酸,溶液变红,说明晶体中含有+3价的铁元素。加硫酸后溶液变红的原因是________
(3)经检验,翠绿色晶体为K3Fe(C2O4)3·3H2O。设计实验,确认实验1中没有发生氧化还原反应的操作和现象是_________。实验1中未发生氧化还原反应的原因是_________
(4)取实验1中的翠绿色溶液光照一段时间,产生黄色浑浊且有气泡产生。补全反应的离子方程式:
________Fe(C2O4)33-+________H2O FeC2O4·2H2O↓+_______+_______。
FeC2O4·2H2O↓+_______+_______。
(实验2)通过比较H2O2与Fe2+、C2O42-反应的难易,判断二者还原性的强弱。
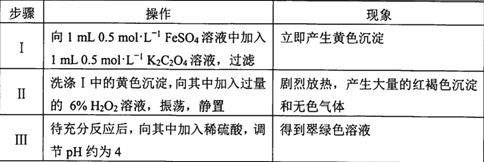
(5)证明Fe2+被氧化的实验现象是_________________________________。
(6)以上现象能否说明C2O42-没有被氧化。请判断并说明理由:_____________。
(实验3)通过其他实验方案比较Fe2+和C2O42-的还原性强弱。
(7)用FeCl3溶液、K2C2O4溶液和其他试剂,设计实验方案比较Fe2+和C2O42-的还原性强弱。画出装置图并描述预期现象:____________________________ 。
-
K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3] 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________。
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。
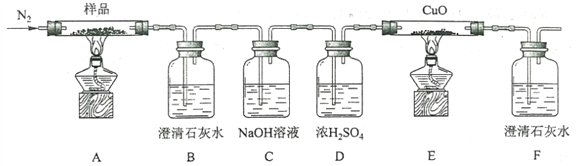
①通入氮气的目的是________________________________________。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有___________、___________。
③为防止倒吸,停止实验时应进行的操作是_____________________________。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:________________。
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是___________________________。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为________________________________。
-
K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3] 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________。
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。
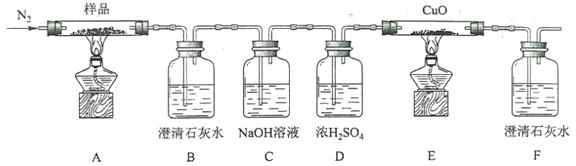
①通入氮气的目的是________________________________________。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有___________、___________。
③为防止倒吸,停止实验时应进行的操作是_____________________________。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:________________。
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是___________________________。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为________________________________。
-
K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3] 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________。
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。
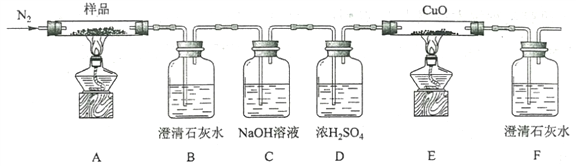
①通入氮气的目的是________________________________________。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有___________、___________。
③为防止倒吸,停止实验时应进行的操作是_____________________________。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:________________。
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是___________________________。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为________________________________。
-
实验室中,通常以草酸钠(Na2C2O4)为标准液,通过氧化还原滴定来测定高锰酸钾溶液的浓度,其反应的化学方程式为:C2O42-+MnO4-+H+-Mn2++CO2↑+H2O(未配平)下列有关草酸钠滴定高锰酸钾实验的叙述,正确的是( )
A.滴定过程中,高锰酸钾被氧化,草酸钠被还原
B.温度需超过100℃,草酸钠与高锰酸钾才会反应
C.反应中,消耗的草酸钠与高锰酸钾的物质的量之比为5:2
D.为便于滴定终点的判断,滴定时必须往体系中加入指示剂












