25℃时,用HCl气体或NaOH固体调节0.01mol·L-1二元酸(以H2A表示)溶液的pH(忽略溶液体积的变化),溶液中H2A、HA-、A2-、H+、OH-浓度的对数值(lgc)变化如下图所示:
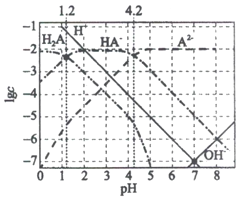
下列说法错误的是
A. 25℃时,H2A的Ka1数量级为10-2
B. pH=1.2时,调节溶液pH用的是HCl气体
C. pH=7时,溶液中:c(Na+)=c(HA-)+c(A2-)
D. pH=8时,溶液中:c(A2-)>c(HA-)>c(H2A)
高三化学单选题困难题
25℃时,用HCl气体或NaOH固体调节0.01mol·L-1二元酸(以H2A表示)溶液的pH(忽略溶液体积的变化),溶液中H2A、HA-、A2-、H+、OH-浓度的对数值(lgc)变化如下图所示:

下列说法错误的是
A. 25℃时,H2A的Ka1数量级为10-2
B. pH=1.2时,调节溶液pH用的是HCl气体
C. pH=7时,溶液中:c(Na+)=c(HA-)+c(A2-)
D. pH=8时,溶液中:c(A2-)>c(HA-)>c(H2A)
高三化学单选题困难题
25℃时,用HCl气体或NaOH固体调节0.01mol·L-1二元酸(以H2A表示)溶液的pH(忽略溶液体积的变化),溶液中H2A、HA-、A2-、H+、OH-浓度的对数值(lgc)变化如下图所示:

下列说法错误的是
A. 25℃时,H2A的Ka1数量级为10-2
B. pH=1.2时,调节溶液pH用的是HCl气体
C. pH=7时,溶液中:c(Na+)=c(HA-)+c(A2-)
D. pH=8时,溶液中:c(A2-)>c(HA-)>c(H2A)
高三化学单选题困难题查看答案及解析
已知:H2A为二元弱酸,25℃时,在0.1mol/L 50 mL的H2A溶液中,H2A、HA-、A2-的物质的量浓度随溶液pH变化的关系如图所示(注:溶液的pH用NaOH固体调节,体积变化忽略不计)。
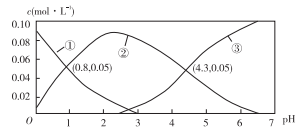
下列说法不正确的是
A. 在 pH = 3 时,c(HA-)>c(A2-)>c(H2A)
B. 在pH在0~7中,c(HA-)+c(A2-)+c(H2A)=0.1mol/L
C. 在pH 3→6的过程中,主要发生反应HA-+OH-==A2-+ H2O
D. 在 pH = 4.3 时,c(Na+)+c(H+)=c(OH-) + 2c(HA-)
高三化学选择题困难题查看答案及解析
常温下,向100 mL 0.1 mol·L-1 H2A(二元酸)溶液中逐滴加入0.2 mol·L-1 NaOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。下列有关说法正确的是( )
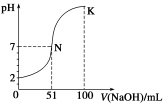
A.H2A为二元强酸
B.N点对应溶液有:c(Na+)=c(A2-)+c(HA-)
C.K点对应溶液中离子浓度由大到小的顺序为c(A2-)>c(Na+)>c(OH-)>c(H+)
D.K点时加水稀释溶液,c(H+)增大
高三化学选择题中等难度题查看答案及解析
研究硫元素及其化合物的性质具有重要意义
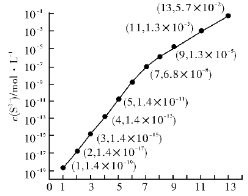
(1)25 ℃,在0.10 mol • L-1HA溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如右图(忽略溶液体积的变化、H2S的挥发)。
①pH=11 时,溶液中的 c(H2S)+c(HS-)= mol•L-1。(保留3位有效数字)
②某溶液含0.010 mol • L-1 Fe2+、未知浓度的Mn2+和0.10 mol•L-1H2S,当溶液pH= 时,Fe2+开始沉淀;当Mn2+开始沉淀时,溶液中= 。
[已知:Ksp(FeS)=1.4×10-19,Ksp(MnS)=2.8×10-13]
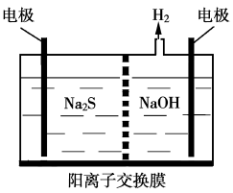
(2)硫化氢的转化是资源利用和环境保护的重要研究课题。由硫化氢获得硫单质有多种方法。其中一种是将烧碱吸收H2S后的溶液加入到如图所示的电解池 的阳极区进行电解。请写出阳极的电极反应式 ,同时阳极区还发生(n—1)S+S2-=Sn2-。电解后阳极区的溶液用稀硫酸酸化,产生淡黄色浑浊,其离子方程式为 。
(3)25℃,两种酸的电离平衡常数如下表。
| Ka | Ka2 | |
| H2SO3 | 1.3X10-2 | 6.3X10-8 |
| H2CO3 | 4.2X10-7 | 5.6X10-11 |
实验室常用饱和NaHCO3溶液除去CO2中少量的SO2,请写出SO2和NaHCO3溶液反应的主要离子方程式 。[
高三化学填空题简单题查看答案及解析
25℃,在100mL0.1mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图(忽略溶液体积的变化和H2S的挥发)。下列说法正确的是( )
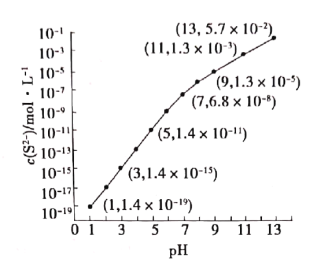
A.当c(H2S)+c(HS-)=0.043mol·L-1时,pH=13
B.pH=1时,c(H+)=c(Cl-)+c(HS-)+ c(S2-)+c(OH-)
C.向该溶液中加入NaOH固体至中性时c(Na+)>c(HS-)>c(S2-)>c(H+)=c(OH-)
D.已知:Ksp(MnS)=2.8×10-13,某溶液含amol·L-1Mn2+、0.10mol·L-1H2S,当溶液pH=5时,Mn2+开始沉淀,则a=0.2
高三化学单选题困难题查看答案及解析
某温度下,向0.10mol/L的HCOONH4溶液中通入HCl或加入NaOH固体调节溶液pH(忽略溶液体积变化),部分粒子的浓度随pH的变化关系如图所示。其中[NH3]表示溶液中NH3与NH3·H2O的浓度之和,M点的坐标为(6.5,-4)。下列说法不正确的是
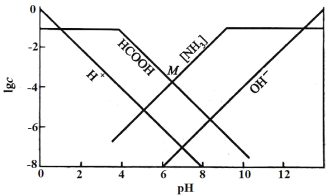
A.此温度下,Kw=1.0×10-14
B.pH<12时,溶液中[NH3]>c(OH-)
C.M点有c(HCOO-)>c(HCOOH)>c(NH4+)>c(H+)>c(OH-)
D.Ka(HCOOH)的数量级为10-4
高三化学单选题困难题查看答案及解析
25℃时,将不同浓度的二元弱酸H2A和NaOH溶液等体积混合(体积变化忽略不计),设反应后溶液的pH如下表:
| 实验编号 | 起始浓度/mol·L—1 | 反应后溶液的pH | |
| c(H2A) | c (NaOH) | ||
| ① | x | 0.10 | 9 |
| ② | 0.10 | 0.10 | 5 |
下列判断不正确的是
A. x﹤0.10
B. HA—的电离程度大于水解程度
C. 实验②所得溶液:c(Na+)=c(A2—)+c(HA—)+c(H2A)
D. 将实验①所得溶液加水稀释后,c(A2—)/c(HA—)变大
高三化学选择题困难题查看答案及解析
25℃时,将不同浓度的二元弱酸H2A和NaOH溶液等体积混合(体积变化忽略不计),设反应后溶液的pH如下表:
| 实验编号 | 起始浓度/mol·L—1 | 反应后溶液的pH | |
| c(H2A) | c | ||
| ① | x | 0.10 | 9 |
| ② | 0.10 | 0.10 | 5 |
下列判断不正确的是
A.x﹤0.10
B.HA—的电离程度大于水解程度
C.实验②所得溶液:c(Na+)=c(A2—)+c(HA—)+c(H2A)
D.将实验①所得溶液加水稀释后,c(A2—)/c(HA—)变大
高三化学选择题简单题查看答案及解析
25时,将不同浓度的二元弱酸H2A和NaOH溶液等体积混合(体积变化忽略不计),测得反应后溶液的pH如下表:
| 实验编号 | 起始浓度/mol·L-1 | 反应后溶液的pH | |
| c(H2A) | c(NaOH) | ||
| ① | X | 0.10 | 9 |
| ② | 0.10 | 0.10 | 5 |
下列判断不正确的是
A.X <0.1
B.HA-的电离程度大于水解程度
C.将实验①所得溶液加水稀释后,c(A2-)/c(HA-)变大
D.实验②所得溶液:c(Na+)=c(A2-)+c(HA-)+c(H2A)
高三化学选择题困难题查看答案及解析
常温下用0.1mol·L-1NaOH溶液滴定10.00mL二元弱酸H2A溶液,滴定曲线如图所示,d点恰好中和。假设混合时溶液体积变化忽略不计,下列说法不正确的是
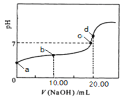
A.a点pH>1
B.c点时c(Na+)=c(H2A)+2c(A2-)+c(HA-)
C.b点时:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
D.滴定过程中c(Na+)+c(A2-)+c(HA-)+c(H2A)=0.1mol/L
高三化学单选题中等难度题查看答案及解析