-
[2017天津]用沉淀滴定法快速测定NaI等碘化物溶液中c(I−),实验过程包括准备标准溶液和滴定待测溶液。
Ⅰ.准备标准溶液
a.准确称取AgNO3基准物4.2468 g(0.0250 mol)后,配制成250 mL标准溶液,放在棕色试剂瓶中避光保存,备用。
b.配制并标定100 mL 0.1000 mol·L−1 NH4SCN标准溶液,备用。
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00 mL于锥形瓶中。
b.加入25.00 mL 0.1000 mol·L−1 AgNO3溶液(过量),使I−完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.1000 mol·L−1 NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如下表:
实验序号
1
2
3
消耗NH4SCN标准溶液体积/mL
10.24
10.02
9.98
f.数据处理。
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有__________。
(2)AgNO3标准溶液放在棕色试剂瓶中避光保存的原因是___________________________。
(3)滴定应在pH<0.5的条件下进行,其原因是___________________________________。
(4)b和c两步操作是否可以颠倒________________,说明理由________________________。
(5)所消耗的NH4SCN标准溶液平均体积为_____mL,测得c(I−)=_________________ mol·L−1。
(6)在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为________________________。
(7)判断下列操作对c(I−)测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果_______________。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果____________________。
高三化学综合题困难题查看答案及解析
-
用沉淀滴定法快速测定NaI等碘化物溶液中c(I-),实验过程包括准备标准溶液和滴定待测溶液。
Ⅰ.准备标准溶液
a.准确称取AgNO3基准物4.2468g(0.0250mol)后,配制成250mL标准溶液,放在棕色试剂瓶中避光保存,备用。
b.配制并标定100mL0.1000mol·L-1NH4SCN标准溶液,备用。
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中。
b.加入25.00mL0.1000mol·L-1AgNO3溶液(过量),使I-完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.1000mol·L-1NH4SCN溶液滴定过量的Ag+,已知AgSCN为白色沉淀。
e.重复上述操作两次到三次测定数据如下表:
实验序号
1
2
3
消耗NH4SCN标准溶液体积/mL
10.24
10.02
9.98
f.数据处理。
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有________。制得AgNO3溶液的浓度为__________________;
(2)AgNO3标准溶液放在棕色试剂瓶中避光保存的原因是________________________。
(3)滴定应在pH<0.5的条件下进行,其原因是________。
(4)过程Ⅱ中b和c两步操作是否可以颠倒________,说明理由:___________。
(5)达到滴定终点时的现象________________________。
(6)由上述实验数据测得c(I-)=________mol·L-1。
(7)若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则对c(I-)测定结果的影响________(填“偏高”“偏低”或“无影响”)。
高三化学实验题困难题查看答案及解析
-
(18分)用沉淀滴定法快速测定NaI等碘化物溶液中c(I−),实验过程包括准备标准溶液和滴定待测溶液。
Ⅰ.准备标准溶液
a.准确称取AgNO3基准物4.2468 g(0.0250 mol)后,配制成250 mL标准溶液,放在棕色试剂瓶中避光保存,备用。
b.配制并标定100 mL 0.1000 mol·L−1 NH4SCN标准溶液,备用。
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00 mL于锥形瓶中。
b.加入25.00 mL 0.1000 mol·L−1 AgNO3溶液(过量),使I−完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.1000 mol·L−1NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如下表:
实验序号
1
2
3
消耗NH4SCN标准溶液体积/mL
10.24
10.02
9.98
f.数据处理。
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有__________。
(2)AgNO3标准溶液放在棕色试剂瓶中避光保存的原因是___________________________。
(3)滴定应在pH<0.5的条件下进行,其原因是___________________________________。
(4)b和c两步操作是否可以颠倒________________,说明理由________________________。
(5)所消耗的NH4SCN标准溶液平均体积为_____mL,测得c(I-)=_________________mol·L-1。
(6)在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为________________________。
(7)判断下列操作对c(I-)测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果_______________。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果____________________。
高三化学填空题中等难度题查看答案及解析
-
用沉淀滴定法快速测定NaI等碘化物溶液中c(I-),实验过程包括准备标准溶液和滴定待测溶液。
Ⅰ.准备标准溶液
a.准确称取AgNO3基准物4.246 8 g(0.0250 mol)后,配制成250 mL标准溶液,放在棕色试剂瓶中避光保存,备用。
b.配制并标定100 mL 0.100 0 mol·L-1NH4SCN标准溶液,备用。
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00 mL于锥形瓶中。
b.加入25.00 mL 0.100 0 mol·L-1AgNO3溶液(过量),使I-完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.100 0 mol·L-1NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,停止滴定。
e.重复上述操作两次。三次测定数据如表:

f.数据处理。
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有________。
(2)滴定应在pH<0.5的条件下进行,其原因是_____________________。
(3)b和c两步操作是否可以颠倒________,说明理由___________________________。
(4)滴定终点的现象为______________________________。测得c(I-)=________ mol·L-1。
(5)判断下列操作对c(I-)测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果________。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果________。
高三化学实验题困难题查看答案及解析
-
用沉淀滴定法快速测定NaI等碘化物溶液中c(I−),实验过程包括准备标准溶液和滴定待测溶液。
Ⅰ.准备标准溶液
a.准确称取AgNO3基准物4.2468 g(0.0250 mol)后,配制成250 mL标准溶液,放在棕色试剂瓶中避光保存,备用。
b.配制并标定100 mL 0.1000 mol·L−1 NH4SCN标准溶液,备用。
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00 mL于锥形瓶中。
b.加入25.00 mL 0.1000 mol·L−1 AgNO3溶液(过量),使I−完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.1000 mol·L−1NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如下表:
实验序号
1
2
3
消耗NH4SCN标准溶液体积/mL
10.24
10.02
9.98
f.数据处理。
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有_________。
(2)AgNO3标准溶液放在棕色试剂瓶中避光保存的原因是________________________。
(3)滴定应在pH<0.5的条件下进行,其原因是________________________________。
(4)b和c两步操作是否可以颠倒________________,说明理由___________________。
(5)所消耗的NH4SCN标准溶液平均体积为_____mL,测得c(I-)=_______________mol·L-1。
(6)在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为____________________。
(7)判断下列操作对c(I-)测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果_______________。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果____________________。
高三化学简答题困难题查看答案及解析
-
用沉淀滴定法快速测定NaI等碘化物溶液中c(I-),实验过程包括准备标准溶液和滴定待测溶液。
I.准备标准溶液
a.准确称取AgNO3基准物4.2468 g(0.0250 mol)后,配制成250 mL标准溶液,放在棕色试剂瓶中避光保存,备用。
b.配制并标定100mL. 0.1000mol/LNH4SCN标准溶液,备用。
II.漓定的主要步骤
a.取待测NaI溶液25.00 mL于锥形瓶中。
b.加入25.00 mL 0.1000mol/LAgNO3溶液(过量),使I-完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.1000mol/LNH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如下表:
实验序号
1
2
3
消耗NH4SCN标准溶液体积/mL
10.24
10.02
9.98
f.数据处理。
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有__________。
(2) AgNO3标准溶液放在棕色试剂瓶中避光保存的原因是__________。
(3)滴定应在pH<0.5的条件下进行,其目的是__________。
(4)测得c(I-)=____________mol/L。
(5)在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为__________。
(6)判断下列操作对c(I-)测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果__________。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果__________。
高三化学实验题中等难度题查看答案及解析
-
莫尔法是一种沉淀滴定法,以K2CrO4为指示剂,用标准硝酸银溶液滴定待测液,进行测定溶液中Cl-的浓度。已知:
银盐
性质
AgCl
AgBr
Ag2CrO4
颜色
白
浅黄
砖红
滴定终点的现象是______,终点现象对应的离子反应方程式为______。为了测定产品中(NH4)2Cr2O7的含量,称取样品0.1500g,置于锥形瓶中,加50mL水,再加入2g KI(过量)及稍过量的稀硫酸溶液,摇匀,暗处放置10min,然后加150mL蒸馏水并加入3mL 0.5%淀粉溶液,用0.1000mol/L Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液30.00mL,则上述产品中(NH4)2Cr2O7的纯度为______。(假定杂质不参加反应,已知:①Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,I2+2S2O32-=2I-+S4O62-;②(NH4)2Cr2O7的摩尔质量为252g/mol)。
高三化学实验题中等难度题查看答案及解析
-
某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
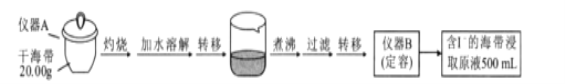
(实验一)碘含量的测定。取0.0100mol/L的AgNO3标准溶液装入滴定管,取100.00mL海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E)反映溶液中c(I-)的变化,部分数据如下表:
V(AgNO3)/mL
15.00
19.00
19.80
19.98
20.00
20.02
21.00
23.00
25.00
E/mV
-225
-200
-150
-100
50.0
175
275
300
325
回答下列问题:
(1)实验中“灼烧”是在__(填仪器名称)中完成的。
(2)用文字具体描述“定容”过程:__
(3)根据表中数据判断滴定终点时用去AgNO3溶液的体积为__mL,计算得海带中碘的质量百分含量为__%。
(实验二)碘的制取。另制海带浸取原液,甲、乙两种实验方案如下:
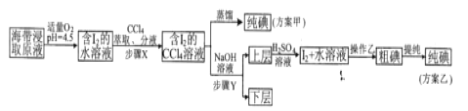
已知:3I2+6NaOH=5NaI+NaIO3+3H2O。
(4)“适量O2”中能代替O2的最佳物质对应的电子式为__
(5)若要测定“I2+水溶液”中碘的含量,可以选择__作指示剂,用Na2S2O3溶液滴定,滴定终点的现象是__。
(6)若得到“I2+水溶液”时加入硫酸溶液过多,用Na2S2O3溶液滴定时会产生明显的误差,产生此误差的原因为__(用离子方程式表示)。
高三化学实验题中等难度题查看答案及解析
-
用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2g 含有少量中性易溶杂质的样品,配成500mL 待测溶液。用0.1000mol·L-1的硫酸滴定,写出该中和反应的热化学方程式________________________________(中和热ΔH=-57.3 kJ/mol)。
(2)滴定过程中,眼睛应注视___________,若用酚酞作指示剂达到滴定终点的标志是_____________。
(3)根据下表数据,计算烧碱样品的纯度是___________(用百分数表示,保留小数点后两位)
滴定次数
待测溶液体积(mL)
标准酸体积
滴定前的刻度(mL)
滴定后的刻度(mL))
第一次
10. 00
0. 40
20. 50
第二次
10. 00
4. 10
24. 00
(4)下列实验操作会对滴定结果产生什么后果?(填“偏高”“偏低”或“无影响”)
①观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果____________。
②若将锥形瓶用待测液润洗,然后再加入10. 00mL待测液,则滴定结果____________。
高三化学综合题中等难度题查看答案及解析
-
某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取.
实验一:碘含量的测定
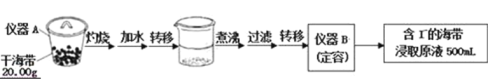
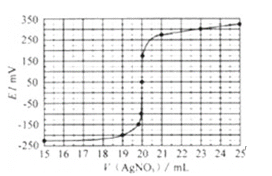
取0.0100mol/L的AgNO3标准溶液滴定100.00mL海带浸取原液,用电势滴定法测定碘的含量.测得的电动势(E)反映溶液中c(I﹣) 变化,用数字传感器绘制出滴定过程中曲线变化如图所示:
实验二:碘的制取
另取海带浸取原液,甲、乙两种实验方案如图所示:
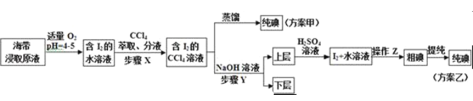
已知:3I2+6NaOH→5NaI+NaIO3+3H2O
请回答:
(1)实验一中的仪器名称:仪器A______,仪器B______;实验二中操作Z的名称______.
(2)根据表中曲线可知:此次滴定终点时用去AgNO3溶液的体积为______ml,计算该海带中碘的百分含量为______.
(3)步骤X中,萃取后分液漏斗内观察到的现象是______.
(4)下列有关步骤Y的说法,正确的是______
A.应控制NaOH溶液的浓度和体积 B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质 D.NaOH溶液可以由乙醇代替
方案乙中,上层液体加硫酸发生反应的离子方程式是______.
(5)方案甲中采用蒸馏不合理,理由是______.
高三化学综合题中等难度题查看答案及解析